
ĚâÄżÁбí(°üŔ¨´đ°¸şÍ˝âÎö)
7Ł®(8·Ö)
ÎŞ±Č˝ĎFe3+şÍCu2+¶ÔH2O2·Ö˝âµÄ´ß»ŻĐ§ąűĽ×ŇŇÁ˝×éͬѧ·Ö±đÉčĽĆÁËČçÍĽŇ»ˇ˘ÍĽ¶ţËůĘľµÄʵŃ顣
˘ĹÍĽŇ»żÉͨąýąŰ˛ěˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ¶¨ĐԱȽϵóö˝áÂۡŁ
ÓĐͬѧĚáłö˝«CuSO4¸ÄÎŞCuCl2¸üÎŞşĎŔíŁ¬ĆäŔíÓÉĘÇŁşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł¬ÄăČĎÎŞ»ążÉŇÔ×÷şÎ¸Ä˝řŁżˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ

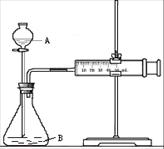
ÍĽŇ»ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ÍĽ¶ţ
˘ĆĽě˛éÍĽ¶ţ×°ÖĂĆřĂÜĐԵķ˝·¨Ęǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
ÍĽ¶ţËůʾʵŃéÖĐĐč˛âÁżµÄĘýľÝĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
6Ł®(7·Ö)˛čĘǶ«ÄĎŃǸ÷ąúČËĂńϲ°®µÄŇűĆ·Ł¬¸÷ÖÖ˛čҶƷÖÖÖĐ°˛ĎŞĚúąŰŇô×ʢĂűˇŁ˛čҶÖĐş¬ÓжŕÖÖÓĐŇćÓÚČËĚ彡żµµÄÓĐ»úłÉ·ÖÓë¶ŕÖÖ΢ÁżÔŞËءŁÄł»ŻŃ§ŃĐľżĐˇ×éÓűĚ˝ľż˛čҶÖиĆÔŞËصĺ¬ÁżŁ¬ÉčĽĆÁËĚ˝ľżĘµŃé·˝°¸ČçĎÂŁş(ŇŃÖŞ˛čҶÖеÄÂÁˇ˘ĚúÔŞËضԸĆŔë×ӵIJⶨÓĐÓ°Ďě)
˛˝Öč1ŁşłĆȡ500żË¸ÉÔďµÄ˛čҶŁ¬ÖĂÓÚͨ·çł÷ÖĐŁ¬łä·Ö×ĆÉŐĘą˛čҶ»Ň»ŻŁ¬ÔŮÓĂŃв§ÄĄĎ¸şóŇĆČëÉŐ±ÖĐŁ¬Č»şó˝«200mL 1 molˇ¤L-1ŃÎËáĽÓČë»ŇÖĐ˝Á°čˇ˘ąýÂˡ˘Ď´µÓˇŁ
˛˝Öč2ŁşĎň˛˝Öč1ËůµĂÂËŇşÖĐÖđµÎĽÓČëϡÇâŃő»ŻÄĆČÜŇşŁ¬µ÷˝ÚČÜŇşµÄpHÎŞ6-7×óÓŇŁ¬ĘąÂÁˇ˘ĚúµÄÇâŃő»ŻÎďÍęČ«łÁµíŁ¬ÔŮĽÓČČÖó·Đ30 minŁ¬ĽÓČë7.95 gÎŢˮ̼ËáÄĆŁ¬łä·Ö˝Á°čŁ¬´ýłÁµíÍęČ«şóŁ¬ąýÂËŁ¬Ď´µÓŁ¬ąýÂËşóµĂµ˝ÂËŇşşÍłÁµíˇŁ
˛˝Öč3Łş˝«˛˝Öč2ËůµĂµÄÂËҺϡĘÍÖÁ500 mLŁ¬ČˇĆäÖеÄ20.00 mLČÜŇşŇԼ׻ůłČ×÷ָʾĽÁŁ¬ÓĂ0.1000molˇ¤L-1µÄHCl±ę׼ČÜŇşµÎ¶¨Ł¬ÖŐµăʱĎűşÄŃÎËáµÄĚĺ»ýÎŞ20.00 mLˇŁÇë»Ř´đĎÂÁĐÎĘĚâ
˛˝Öč 1ÖĐŁ¬Ęą˛čҶ»Ň»ŻĐčŇŞČý˝ÇĽÜˇ˘ÄŕČý˝Çˇ˘ľĆľ«ĹçµĆˇ˘ˇˇˇˇˇˇˇˇ ˇ˘ŰáŰöÇŻµČŇÇĆ÷ˇŁ
˛˝Öč2ÖĐŁ¬¸ÄÓĂĘÔĽÁ________________Ŕ´µ÷˝ÚpH˝«¸üÎŞ·˝±ăŁ»ĹжϳÁµíŇѾϴµÓ¸Éľ»µÄ·˝·¨Ęǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
˛˝Öč3ÖĐŁ¬µÎ¶¨˛Ů×÷ʱŁ¬ŃŰľ¦×˘ĘÓˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇ ˇŁ±»µÎ¶¨µÄ20 mLÂËŇşÖĐ CO32ŁµÄÎďÖʵÄÁżÎŞ______________molŁ¬Ô˛čҶÖиĆŔë×ÓµÄÖĘÁż·ÖĘýÎŞ__________________ˇŁ
5Ł®(8·Ö)ÎŞĚ˝ľżCO2ÓëąýÁżµÄNaOHČÜҺȷʵ·˘ÉúÁË»ŻŃ§·´Ó¦Ł¬Ľ×ˇ˘Ňҡ˘±űČýλͬѧÉčĽĆÁËĎÂÁĐČýÖÖʵŃé×°ÖĂŁ¬Çë»Ř´đĎÂÁĐÎĘĚ⣺
 ˇˇ
ˇˇ
ˇˇˇˇˇˇˇˇˇˇ (Ľ×)ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (ŇŇ)ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇ (±ű)
(1)ÇëĐ´łöCO2ÓëąýÁżµÄNaOH·˘Éú·´Ó¦µÄŔë×Ó·˝łĚĘ˝Łş
ˇˇˇˇˇˇˇˇˇˇ___ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ _____ˇŁ
(2)ѡÔńČÎŇâŇ»ÖÖʵŃé×°ÖĂŁ¬ĽňĘöÔ¤ĽĆłöĎÖµÄʵŃéĎÖĎ󣬽âĘͲúÉú¸ĂʵŃéĎÖĎó
ˇˇˇˇ µÄÔŇňŁş ÄăѡÔńµÄʵŃé×°ÖĂĘǡˇˇˇ ˇˇŁ¬ĘµŃéĎÖĎóĘǡˇˇˇˇˇˇˇˇˇˇˇ ____ˇˇˇˇ ____ˇŁ
ˇˇˇˇ ˝âĘͲúÉú¸ĂʵŃéĎÖĎóµÄÔŇňŁşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇ ________ˇŁ
4Ł®(15·Ö)ÔÚʵŃéĘŇŔďżÉÓĂĎÂÍĽËůĘľ×°ÖĂÖĆȡÂČËáĽŘˇ˘´ÎÂČËáÄĆşÍĚ˝ľżÂČĆřµÄĐÔÖʡŁ
ˇˇˇˇ
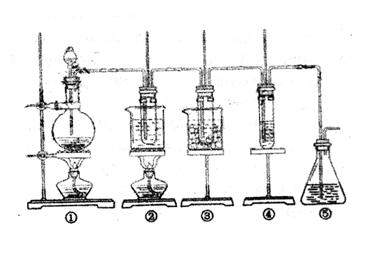
ÍĽÖĐŁş˘ŮÎŞÂČĆř·˘Éú×°ÖĂŁ»˘ÚµÄĘÔąÜŔďʢÓĐ15mL 30%KOHČÜŇşŁ¬˛˘ÖĂÓÚˮԡÖĐŁ»˘ŰµÄĘÔąÜŔďʢµäÓĐ15mL 8%NaOHČÜŇşŁ¬˛˘ÖĂÓÚ±ůˮԡÖĐŁ»˘ÜµÄĘÔąÜŔďĽÓÓĐÂČ»ŻŃÇĚúČÜŇş˘ÝΪβĆřÎüĘŐ×°ÖáŁ
ÇëĚîżŐĎÂÁпհףş
ˇˇ (1)ÖĆȡÂČĆřʱŁ¬ÔÚÉŐĆżŔďĽÓŇ»¶¨ÁżµÄ¶ţŃő»ŻĂĚŁ¬Í¨ąýˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇ(ĚîĐ´ŇÇĆ÷ĂűłĆ)ĎňÉŐĆżÖĐĽÓČëĘĘÁżµÄŨŃÎËᡣʵŃéʱΪÁËłýČĄÂČĆřÖеÄÂČ»ŻÇâĆřĚ壬żÉÔÚ˘ŮÓë˘ÚÖ®Ľä°˛×°Ę˘ÓСˇˇˇˇˇˇˇˇˇˇˇˇˇ (ĚîĐ´ĎÂÁбŕşĹ×Öĸ)µÄľ»»Ż×°ÖáŁ
AŁ®ĽîĘŻ»Ňˇˇˇˇ BŁ®±ĄşÍĘłŃÎË®ˇˇˇˇ CŁ®Ĺ¨ÁňËᡡˇˇ DŁ®±ĄşÍĚĽËáÇâÄĆČÜŇş
ˇˇ (2)±Č˝ĎÖĆȡÂČËáĽŘşÍ´ÎÂČËáÄƵÄĚőĽţŁ¬˛ĹŐߵIJîŇěĘÇŁş
ˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
ˇˇ (3)±ľĘµŃéÖĐÖĆȡÂČËáĽŘµÄŔë×Ó·˝łĚą¤Ęǡˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
ˇˇ (4)ʵŃéÖпɹ۲쵽˘ÜµÄĘÔąÜŔďČÜŇşµÄŃŐÉ«´ÓÇłÂĚÉ«Ö𽥱äÎŞˇˇˇˇˇˇˇˇˇˇˇˇˇˇ É«Ł¬ĆäÔŇňĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ( ÓĂŔë×Ó·˝łĚĘ˝˝âĘÍ)ˇŁÎŞÁËĽěŃéÉúłÉµÄÎďÖĘŁ¬żÉĽÓČ롡ˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
3Ł®(ą˛4·Ö)ˇˇˇˇ ijʵŃéС×éÎŞĚ˝ľżClOŁˇ˘I2ˇ˘SO42ŁÔÚËáĐÔĚőĽţϵÄŃő»ŻĐÔÇżČőŁ¬ÉčĽĆʵŃéČçĎÂŁş
ʵŃé˘ŮŁşÔÚµí·Űµâ»ŻĽŘČÜŇşÖĐĽÓČëÉŮÁż´ÎÂČËáÄĆČÜŇşŁ¬˛˘ĽÓČëÉŮÁżµÄϡÁňËᣬČÜŇşÁ˘Ľ´±äŔ¶Ł»
ʵŃé˘ÚŁşĎňʵŃé˘ŮµÄČÜŇşÖĐĽÓČë4 mL 0.5 mol/LµÄŃÇÁňËáÄĆČÜŇşŁ¬Ŕ¶É«ÇˇşĂÍęČ«ÍĘČĄˇŁ
ˇˇ ˇˇ (1)Đ´łöʵŃé˘ŮÖĐ·˘Éú·´Ó¦µÄŔë×Ó·˝łĚĘ˝ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
ˇˇ(2)ʵŃé˘ÚÖĐ»ŻŃ§·´Ó¦×ŞŇƵç×ÓµÄÎďÖʵÄÁżĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
ˇˇ(3)ŇÔÉĎʵŃé˵Ă÷Ł¬ÔÚËáĐÔĚőĽţĎÂClOŁˇ˘I2ˇ˘SO42ŁµÄŃő»ŻĐÔÓÉČőµ˝ÇżµÄËłĐňĘÇ_________________ˇŁ
2ˇ˘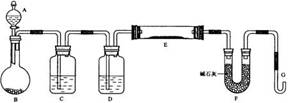 (12·Ö)ÄłżÎÍâС×éŔűÓĂH2»ąÔ»ĆÉ«µÄWO3·ŰÄ©˛â¶¨WµÄĎŕ¶ÔÔ×ÓÖĘÁżŁ¬ĎÂÍĽĘDzⶨװÖõÄĘľŇâÍĽŁ¬AÖеÄĘÔĽÁĘÇŃÎËᡣ
(12·Ö)ÄłżÎÍâС×éŔűÓĂH2»ąÔ»ĆÉ«µÄWO3·ŰÄ©˛â¶¨WµÄĎŕ¶ÔÔ×ÓÖĘÁżŁ¬ĎÂÍĽĘDzⶨװÖõÄĘľŇâÍĽŁ¬AÖеÄĘÔĽÁĘÇŃÎËᡣ
Çë»Ř´đĎÂÁĐÎĘĚ⡣
(1)ŇÇĆ÷ÖĐ×°ČëµÄĘÔĽÁŁş
Bˇˇˇˇˇˇˇˇˇˇ ˇˇˇ˘ Cˇˇˇˇˇˇˇˇ ˇˇˇˇˇ˘
Dˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
(2)Á¬˝ÓşĂ×°ÖĂşóÓ¦Ę×Ďȡˇˇˇˇˇˇˇ Ł¬
Ćä·˝·¨Ęǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
(3)ˇ°ĽÓČČ·´Ó¦ąÜEˇ±şÍˇ°´ÓAĆżÖđµÎµÎĽÓŇşĚ塱ŐâÁ˝˛˝˛Ů×÷Ó¦¸ĂĎČ˝řĐеÄĘǡˇˇˇˇˇ ˇŁÔÚŐâÁ˝˛˝Ö®Ľä»ąÓ¦˝řĐеIJŮ×÷Ęǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
(4)·´Ó¦ąýłĚÖĐGąÜŇÝłöµÄĆřĚĺĘÇ_______Ł¬Ćä´¦Ŕí·˝·¨ĘÇ__________________ˇŁ
(5)´ÓʵŃéÖвâµĂÁËĎÂÁĐĘýľÝŁş
˘ŮżŐEąÜµÄÖĘÁżaˇˇˇˇˇˇ ˘ÚEąÜşÍWO3µÄ×ÜÖĘÁżbˇˇˇˇ ˘Ű·´Ó¦şóEąÜşÍW·ŰµÄ×ÜÖĘÁżc(ŔäČ´µ˝ĘŇÎÂłĆÁż) ˘Ü·´Ó¦Ç°FąÜĽ°ÄÚʢÎďµÄ×ÜÖĘÁżdˇˇˇˇ ˘Ý·´Ó¦şóFąÜĽ°ÄÚʢÎďµÄ×ÜÖĘÁżeˇˇˇˇ ÓÉŇÔÉĎĘýľÝżÉŇÔÁĐłöĽĆËăWµÄĎŕ¶ÔÔ×ÓÖĘÁżµÄÁ˝¸ö˛»Í¬ĽĆËăĘ˝(łýWÍ⣬ĆäËűÉ漰µÄÔŞËصÄĎŕ¶ÔÔ×ÓÖĘÁżľůÎŞŇŃÖŞ)ŁşAr(W)Ł˝ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
2Ł®[˛ÂĎëII]ŁşÖ÷ŇŞłÉ·ÖÎŞÂČ»ŻĐżŁ»
[ŃéÖ¤(˛Ů×÷)ąýłĚ]Łşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇŁ»
[ʵŃéĎÖĎó]Łşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
[ĹжϲÂĎë]Łş˛ÂĎë˘ňłÉÁ˘Ł»ÓÉÉĎĘöʵŃéµĂłö˝áÂŰŁşÂËŇşÖеÄÖ÷ˇ˘´ÎłÉ·ÖŁşˇˇˇˇˇˇˇˇˇˇ ˇŁ
1Ł®[˛ÂĎëI]ŁşÖ÷ŇŞłÉ·ÖÎŞÂČ»Żď§Ł»
[ŃéÖ¤(˛Ů×÷)ąýłĚ]ŁşČˇÉŮÁżÂËŇşĽÓČëNaOHąĚĚ壬˛˘ĽÓČČŁ»
[ʵŃéĎÖĎó]ŁşÎŵ˝ÓĐÇá΢µÄ°±Î¶Ł»
[ĹжϲÂĎë]Łşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (Ě˛ÂĎëIłÉÁ˘ˇ±»ňˇ°˛ÂĎëI˛»łÉÁ˘ˇ±)Ł»
1Ł®(14·Ö)ijͬѧÓ÷ϸɵçłŘÄڵĺÚÉ«ąĚĚĺ(żÉÄÜş¬ÓĐMnO2ˇ˘NH4Clˇ˘ZnCl2µČÎďÖĘ)˝řĐĐČçÍĽËůʾʵŃ飺
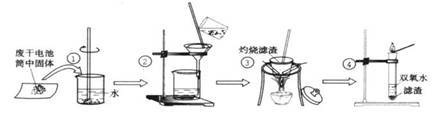
(1)˛Ů×÷˘Ű×ĆÉŐÂËÔüʱËůÓĂÖ÷ŇŞŇÇĆ÷Óоƾ«µĆˇ˘˛ŁÁ§°ôˇ˘ˇˇˇˇˇˇˇˇˇˇˇˇ ˇ˘ˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
(2)˛Ů×÷˘ÜµÄĘԹܼÓČë˘ŰÖĐËůµĂÂËÔüŁ¬ĘÔąÜÖĐѸËٲúÉúÄÜĘą´ř»đĐǵÄÄľĚő¸´ČĽµÄĆřĚ壬ÓÉ´ËÍƲâÂËÔüżÉÄÜÎŞMnO2Ł¬ĘÔąÜÖĐ·˘Éú·´Ó¦µÄ»ŻŃ§·˝łĚĘ˝Łşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł»
(3)˛Ů×÷˘Ű×ĆÉŐÂËÔüÖеĺÚÉ«ąĚĚĺʱŁ¬˛úÉúŇ»ÖÖĘąłÎÇĺĘŻ»ŇË®±ä»ë×ǵÄĆřĚ壬ÓÉ´ËÍƲâÂËÔüÖĐłýş¬ÓĐMnO2Í⣬»ą´ćÔÚµÄÎďÖĘÎŞŁşˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
(4)ŇŃÖŞÂČ»ŻĐżÓëϡ°±Ë®·´Ó¦ĎČÉúłÉZn(OH)2°×É«łÁµíŁ¬Zn(OH)2żÉŇÔČÜÓÚϡ°±Ë®ÉúłÉżÉČÜĐÔµÄZn(NH3)4(OH)2Ł»ĎÂÁĐĘǸĂͬѧ¶Ô˛Ů×÷˘ÚµÄÂËŇşÖ÷´ÎłÉ·Ö˝řĐĐĚ˝ľżµÄąýłĚŁş
23Ł®(23·Ö)ʵŃéĘŇÄŁÄâşĎłÉ°±şÍ°±´ß»ŻŃő»ŻµÄÁ÷łĚČçĎÂŁş
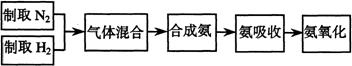
ŇŃ֪ʵŃéĘŇżÉÓñĄşÍŃÇĎőËáÄĆ(NaNO2)ČÜŇşÓ뱥şÍ
ÂČ»Żď§ČÜŇşľĽÓČČşó·´Ó¦ÖĆȡµŞĆřˇŁ
ˇˇ (1)´ÓÓŇÍĽÖĐѡÔńÖĆȡĆřĚĺµÄşĎĘĘ×°ÖĂŁş
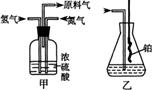 µŞĆřˇˇˇˇˇˇˇˇ
(2·Ö)ˇ˘ÇâĆřˇˇˇˇˇˇˇˇˇˇ
(2·Ö)
µŞĆřˇˇˇˇˇˇˇˇ
(2·Ö)ˇ˘ÇâĆřˇˇˇˇˇˇˇˇˇˇ
(2·Ö)
ˇˇ (2)µŞĆřşÍÇâĆřͨąýĽ××°ÖĂŁ¬Ľ××°ÖõÄ×÷ÓĂłýÁË˝«Ćř
Ěĺ»ěşĎÍ⣬»ąÓСˇˇˇˇˇˇˇˇˇˇˇ (2·Ö)ˇ˘
ˇˇˇˇˇˇˇˇˇˇ (2·Ö)
(3)°±şĎłÉĆ÷łöŔ´ľŔäČ´µÄĆřĚĺÁ¬ĐřͨČËŇŇ×°ÖõÄ
Ë®ÖĐÎüĘŐ°±Ł¬ˇˇˇˇˇˇˇˇ (2·Ö)(ˇ°»áˇ±»ň
ˇ°˛»»áˇ±)·˘ÉúµąÎüŁ¬ÔŇňĘÇŁşˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇˇˇˇˇ (2·Ö)ˇŁ
ˇˇ (4)ÓĂŇŇ×°ÖĂÎüĘŐŇ»¶ÎʱĽä°±şóŁ¬ÔŮͨČëżŐĆřŁ¬Í¬Ę±˝«ľĽÓČȵIJ¬Ëż˛ĺČëŇŇ×°ÖõÄ׶ĐÎĆżÄÚŁ¬ÄÜĘą˛¬Ëż±ŁłÖşěČȵÄÔŇňĘÇŁşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (2·Ö)Ł¬×¶ĐÎĆżÖĐ»ążÉąŰ˛ěµ˝µÄĎÖĎóĘÇŁşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ(2·Ö)
ˇˇ (5)Đ´łöŇŇ×°ÖĂÖĐ°±Ńő»ŻµÄ»ŻŃ§·˝łĚĘ˝Łşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ (3·Ö)
ˇˇ (6)·´Ó¦˝áĘřşó׶ĐÎĆżÄÚµÄČÜŇşÖĐş¬ÓĐH+ˇ˘OHŁˇ˘ˇˇˇˇˇˇˇˇ ˇ˘ˇˇˇˇˇˇ Ŕë×ÓˇŁ(¸÷2·Ö)
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com