
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
4.НЋЙ§СПЕФCO2ЭЈШыЯТСаШмвКжаЃЌзюжеГіЯжЛызЧЕФЪЧ
A.CaCl2ШмвКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.ЪЏЛвЫЎЁЁ
C.БЅКЭNa2CO3ШмвКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.ЫЎВЃСЇ
3.2MgOЁЄSiO2жаЕФЫсИљРызгЪЧЁЁ
A.SiO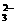 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.Si2O
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.Si2O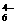
C.SiO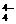 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.SiO
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.SiO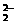
2.ЪЕбщЪвДцЗХЯТСаИїЪдМСЕФЦПШћБиаыгУЯ№ЦЄШћЕФЪЧЁЁ
A.ГЮЧхЪЏЛвЫЎЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.ЙшЫсФЦШмвКЁЁ
C.аТжЦТШЫЎЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.ТШЛЏИЦШмвК
1.(2002ФъШЋЙњИпПМЬт)вдЯТЫЕЗЈе§ШЗЕФЪЧЁЁ
A.ФЩУзВФСЯЪЧжИвЛжжГЦЮЊЁАФЩУзЁБЕФаТЮяжЪжЦГЩЕФВФСЯЁЁ
B.ТЬЩЋЪГЦЗЪЧжИВЛКЌШЮКЮЛЏбЇЮяжЪЕФЪГЦЗЁЁ
C.ЩњЮяЙЬЕЊЪЧжИжВЮяЭЈЙ§вЖУцЮќЪеПеЦјжаЕФЕЊЦјЁЁ
D.ЙтЕМЯЫЮЌЪЧвдЖўбѕЛЏЙшЮЊжївЊдСЯжЦГЩЕФЁЁ
4ЃЎЪЕеНбнСЗ
3ЃЎР§ЬтОЋНВ
[Р§1] ШлШкЧтбѕЛЏФЦЗДгІбЁгУЕФЦїУѓЪЧ [ ]
|
ЁЁAЃЎЬеДЩлслі |
ЁЁBЃЎЪЏгЂлслі |
|
ЁЁCЃЎЦеЭЈВЃСЇлслі |
ЁЁDЃЎЩњЬњлслі |
ЁЁ ЗжЮіЃКЬеДЩЕФГЩЗжжаКЌгаSiO2ЃЌЪЏгЂЕФГЩЗжОЭЪЧSiO2ЃЌВЃСЇЕФжївЊГЩЗжжавВКЌгаSiO2ЃЌЖјSiO2дкИпЮТЯТПЩвдИњNaOHЗЂЩњШчЯТЗДгІЃК
SiO2+2NaOH Na2SiO3
Na2SiO3
ЁЁЫљвдAЁЂBЁЂCЕФЦїУѓЖМВЛФмбЁгУЃЌжЛФмФкЩњЬњлсліЁЃ
ЁЁД№АИЃКD
ЁЁ[Р§2] ЯТСаШмвКжаПЩвдЪЂЗХдкВЃСЇЦПжаЃЌЕЋВЛФмгУФЅПкВЃСЇШћЕФЪЧ [ ]ЁЃ
|
ЁЁAЃЎЙшЫсФЦШмвК |
ЁЁBЃЎЧтЗњЫс |
|
ЁЁCЃЎЧтбѕЛЏФЦШмвК |
ЁЁDЃЎТШЛЏФЦШмвК |
ЁЁ ЗжЮіЃКВЃСЇЕФжївЊГЩЗжжЎвЛЖўбѕЛЏЙшЃЌЫќФмИњЧтЗњЫсбИЫйЗДгІЃЌЫљвдЃЌЧтЗњЫсВЛФмЪЂЗХдкВЃСЇЁЂЬеДЩШнЦїжаЃЌжЛФмБЃДцдкЧІУѓЛђЫмСЯЦПжаЁЃЧтбѕЛЏФЦШмвКгыЖўбѕЛЏЙшдкГЃЮТЯТЗДгІЪЎЗжЛКТ§ЃЌЫљвдПЩвдЪЂЗХдкВЃСЇЦПжаЃЌЕЋЦПЕФФЅПкДІЕФЖўбѕЛЏЙшИњЧтбѕЛЏФЦЛКТ§ЗДгІКѓЃЌЩњГЩЕФЙшЫсФЦЪЧвЛжжПѓЮяНКЃЌЪЙЦПШћгыЦППкеГдквЛЦ№ЃЌвђДЫВЛФмгУФЅПкВЃСЇШћЁЃЙшЫсФЦШмвКПЩвдгУВЃСЇЦПЪЂЗХЃЌжЛЪЧВЛФмгУФЅПкВЃСЇШћ(двђЭЌЧтбѕЛЏФЦШмвК)ЁЃТШЛЏФЦШмвКВЛИњВЃСЇжаИїжжГЩЗжЗДгІЁЃ
ЁЁД№АИЃКAC
ЁЁ[Р§3] ЦеЭЈВЃСЇЕФжївЊГЩЗжЮЊNa2SiO3ЁЄCaSiO3ЁЄ4SiO2
ЁЁ(1)ЪдМЦЫуЦеЭЈВЃСЇжаЯрЕБКЌгаNa2OЃЌCaOКЭSiO2ЕФжЪСПЗжЪ§ИїЪЧЖрЩйЃП
ЁЁ(2)жЦдь50kgЦеЭЈВЃСЇЃЌашвЊДПМюЁЂЬМЫсИЦКЭЖўбѕЛЏЙшИїЖрЩйЧЇПЫЃП
ЁЁЗжЮіЃКNa2SiO3ЁЄCaSiO3ЁЄ4SiO2ПЩгУЖўбѕЛЏЙшКЭН№ЪєбѕЛЏЮяЕФаЮЪНБэЪОЦфзщГЩЮЊЃКNa2OЁЄCaOЁЄ6SiO2ЁЃ
ЁЁ(1)Na2OЕФФІЖћжЪСПЮЊ62g/molЃЌCaOЕФФІЖћжЪСПЮЊ56g/molЃЌSiO2ЕФФІЖћжЪСПЮЊ60g/molЁЃ
ЁЁ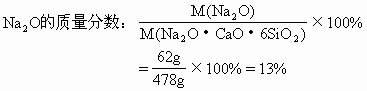
ЁЁ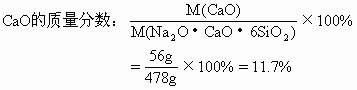
ЁЁ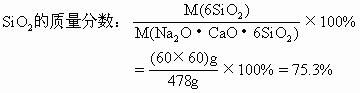
ЁЁ(2)гЩЕк(1)ЬтЧѓГіЦеЭЈВЃСЇжаИїбѕЛЏЮяЕФжЪСПЗжЪ§ЃЌПЩМЦЫу50kgЦеЭЈВЃСЇжаNa2OЁЂCaOКЭSiO2ЕФКЌСПЃК
ЁЁm(Na2O)ЃК50kgЁС13%=6.5kg
ЁЁm(CaO)ЃК50kgЁС11.7%=5.85kg
ЁЁm(SiO2)ЃК50kgЁС75.3%=37.65kg
ЁЁдйЧѓашДПМюЁЂЬМЫсИЦКЭЖўбѕЛЏЙшЕФжЪСПЃК
ЁЁ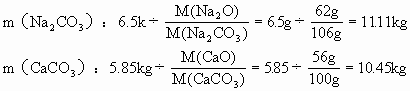
ЁЁm(SiO2)ЃК37.65kg
ЁЁ Д№АИЃК(1)ЦеЭЈВЃСЇжаNa2OЕФжЪСПЗжЪ§ЮЊ13%ЃЌCaOЕФжЪСПЗжЪ§ЮЊ11.7%ЃЌSiO2жЪСПЗжЪ§ЮЊ75.3%ЁЃ
ЁЁ(2)жЦдь50kgЦеЭЈВЃСЇЃЌашвЊДПМю11.11kgЁЂЬМЫсИЦ10.45kgЁЂЖўбѕЛЏЙш37.65kgЁЃ
ЁЁ [Р§4] гаAЁЂBЁЂCШ§жжВЛШмгкЫЎЕФЙЬЬхЁЃAЪЧФГдЊЫиЕФвЛжжЕЅжЪЃЌЫќдкбѕЦјжаЭъШЋШМЩеЕУЕНвЛжжЮоЩЋЦјЬхЃЌДЫЦјЬхФмЪЙГЮЧхЪЏЛвЫЎБфЛызЧЃЌСэЭтВтЕУетжжЦјЬхУмЖШЮЊЭЌЮТЁЂЭЌбЙЯТбѕЦјУмЖШЕФ1.375БЖЁЃBЙЬЬхФмШмгкШШЧтбѕЛЏФЦШмвКЃЌдйЭљЫљЕУШмвКжаМгШыЙ§СПбЮЫсЪБЃЌЮіГіАзЩЋНКзДГСЕэЁЃДЫГСЕэИЩдяКѓЃЌГЩЮЊВЛШмгкЫЎЕФАзЩЋЗлФЉЃЌетЪЧвЛжжБШЬМЫсЫсадЛЙШѕЕФЫсЁЃНЋBгыЪЏЛвЪЏЁЂДПМюАДБШР§ЛьКЯМгШШЕУЕНCЃЌCдкИпЮТЪБШэЛЏЃЌЮоЙЬЖЈШлЕуЁЃ
ЁЁИљОнвдЩЯЪТЪЕЃЌХаЖЯAЮЊФФжждЊЫиЕФЕЅжЪЃПBЁЂCИїЪЧЪВУДЮяжЪЃПаДГігаЙиЗДгІЕФЛЏбЇЗНГЬЪНЁЃ
ЁЁЗжЮіЃКЯШЧѓГіAШМЩеКѓЩњГЩЕФЦјЬхЕФЯрЖдЗжзгжЪСПЃЌИљОнИУЦјЬхЕФЯрЖдЗжзгжЪСПМАЦфЗДгІЯжЯѓПЩЭЦГіЕЅжЪAЃЛдйИљОнBЕФгаЙиЗДгІЯжЯѓПЩЭЦГіBЃЛзюКѓИљОнжЦШЁCЕФЗНЗЈМАCЕФаджЪПЩЭЦГіCЁЃ
ЁЁAЮяжЪШМЩеКѓЩњГЩЕФЦјЬхЕФЯрЖдЗжзгжЪСПЮЊЃК
32ЁС1.375=44
ЁЁИУЦјЬхФмЪЙГЮЧхЪЏЛвЫЎБфЛызЧЃЌЫљвдИУЦјЬхЮЊЖўбѕЛЏЬМЃЌAЮЊЬМдЊЫиЕФвЛжжЕЅжЪЁЃ
ЁЁИљОнBЮяжЪФмгыЧтбѕЛЏФЦЗДгІЃЌЧвФмМЬајгыЙ§СПЕФбЮЫсЗДгІЩњГЩвЛжжБШЬМЫсЛЙШѕЕФЫсЃЌПЩЭЦГіBЮяжЪЮЊЖўбѕЛЏЙшЁЃ
ЁЁCЮяжЪгЩЪЏЛвЪЏЁЂДПМюЁЂBЮяжЪ(ЖўбѕЛЏЙш)ЛьКЯМгШШЖјЕУЃЌНсКЯCЮяжЪдкИпЮТЪБШэЛЏЧвЮоЙЬЖЈШлЕуЃЌПЩЭЦжЊCЮяжЪЮЊЦеЭЈВЃСЇЁЃ
ЁЁД№АИЃКAЮЊЬМдЊЫиЕФвЛжжЕЅжЪЁЃ
C+O2 CO2
CO2
ЁЁBЮЊSiO2
ЁЁSiO2+2NaOH==Na2SiO3+H2O
ЁЁNa2SiO3+2HCl=2NaCl+H2SiO3Ё§
ЁЁCЮЊЦеЭЈВЃСЇ
ЁЁNa2CO3+SiO2==Na2SiO3+CO2Ёќ
ЁЁCaCO3+SiO2==CaSiO3+CO2Ёќ
ЁЁ [Р§5] ФГЙшЫсаПбљЦЗКЌ58.6%ЕФаПЃЌЖјZnO%гыSiO2%ЕФжЪСПЗжЪ§ЕФзмКЭЮЊ100%ЃЌаДГіетбљЦЗЕФЛЏбЇЪН(зюМђЪН)ЁЃ
ЁЁЗжЮіЃКЬтФПвЊЧѓаДГіетбљЦЗЕФЛЏбЇЪН(зюМђЪН)ЃЌМДЪЧвЊЧѓЭЈЙ§МЦЫуевГіZnOгыSiO2ЕФЮяжЪЕФСПжЎБШжЕЃЌШЛКѓгУSiO2КЭZnOЕФаЮЪНБэЪОДЫЙшЫсаПбљЦЗЕФзщГЩЁЃ
ЁЁПЩЯШгЩZn%ЧѓЫуГіZnO%ЃЌВЂЧѓГіSiO2%ЁЃШЛКѓдйдЫгУЧѓзюМђЪНзюЛљБОЕФЗНЗЈЧѓГіДЫЙшЫсаПЕФзщГЩЁЃ
ЁЁ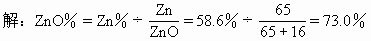
ЁЁSiO2%=1-73.0%=27.0%
ЁЁ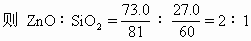
ЁЁИУЙшЫсаПбљЦЗЕФЛЏбЇЪНЮЊЃК2ZnOЁЄSiO2ЁЃ
ЁЁ [Р§6] СНИідЙшЫсЗжзгЕФOHдзгЭХжЎМфПЩвдЯрЛЅзїгУЖјЭбШЅвЛЗжзгЫЎЃК
2H4SiO4===H6Si2O7+H2O
ЁЁдЙшЫсНсЙЙЮЊЃК
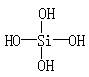
ЁЁдђдкЫљЕУЕФH6Si2O7ЗжзгЕФНсЙЙжаЃЌКЌгаЕФЙшбѕМќЪ§ФПЮЊ [ ]
|
ЁЁAЃЎ5 |
ЁЁBЃЎ6 |
|
ЁЁCЃЎ7 |
ЁЁDЃЎ8 |
ЁЁ ЗжЮіЃКДЫЬтЪЧвЛЕРбЁдёЬтЃЌвВЪЧвЛЕРаХЯЂЧЈвЦЬтЁЃИјГіЕФаТЧщОГЪЧдЙшЫсНсЙЙМАЭбЫЎЗДгІЃЌПМВщФкШнЪЧH6Si2O7ЗжзгжаЕФЙшбѕМќЪ§ФПЁЃСНИідЙшЫсЙВга8ИіЙшбѕМќЃЌЕБЫќУЧЯрЛЅзїгУЪБЃЌЫфШЛгавЛИіЙшбѕМќЖЯСбЃЌЕЋгжаЮГЩвЛИіаТЕФЙшбѕМќЃЌШчЭМЫљЪОЃК
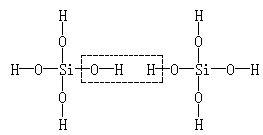
ЁЁЙЪЙшбѕМќЕФзмЪ§ФПУЛгаБфЃЌШдШЛЪЧ8ИіЁЃ
ЁЁД№АИЃКD
ЁЁ[Р§7] ЯТСаРызгЗНГЬЪНЪщаДВЛе§ШЗЕФЪЧ [ ]
ЁЁAЃЎЭљNaOHШмвКжаЭЈШыЙ§СПCO2
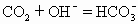
ЁЁBЃЎЕЅжЪЙшгыЩеМюШмвКЗДгІ
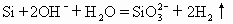
ЁЁCЃЎЪЏгЂЩАгыЩеМюЗДгІжЦЫЎВЃСЇ
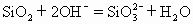
ЁЁDЃЎЭљЫЎВЃСЇжаЭЈШыЖўбѕЛЏЬМ
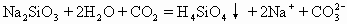
ЁЁ ЗжЮіЃКЭљNaOHШмвКжаЭЈШыЪЪСПCO2ЩњГЩе§бЮNa2CO3ЃЌе§бЮФмгыЫсЗДгІБфЮЊЫсЪНбЮЃЌЫљвдЕБCO2Й§СПЪБМДШмвКжаH2CO3Й§СПЪБЃЌЩњГЩЮяЮЊNaHCO3ЃЌЙЪAЪНе§ШЗЁЃ
ЁЁЕЅжЪЙшФмКЭЩеМюШмвКЗДгІЩњГЩЙшЫсФЦКЭЧтЦјЃЌNaOHЪЧвзШмгкЫЎЕФЧПМюЃЌNa2SiO3ЁЃЪЧвзШмгкЫЎЕФбЮЃЌОљЭъШЋЕчРыЃЌЙЪNa+ПЩвдМђЛЏЕєЃЌBЪНе§ШЗЁЃ
ЁЁЪЏгЂЕФГЩЗжЪЧЖўбѕЛЏЙшгыЩеМювКЗЂЩњИДЗжНтЗДгІЩњГЩЙшЫсФЦКЭЫЎЁЃЙЪCЪНе§ШЗЁЃ
ЁЁЬМЫсБШЙшЫсЫсадЧПЃЌЫљвдЭљЫЎВЃСЇМДЙшЫсФЦЕФЫЎШмвКжаЭЈШыЖўбѕЛЏЬМПЩвджЦЙшЫсЁЃЗДгІЮяжаЕФNa2SiO3КЭЩњГЩЮяжаЕФNa2CO3ОљЮЊвзШмгкЫЎЕФбЮЃЌФмЭъГЩЕчРыаДГЩРызгЪНЃЌВЂЧвNa+ПЩвдМђЛЏЕєЃЌЙЪDЪНВЛе§ШЗЁЃ
ЁЁ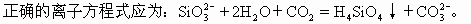
ЁЁ Д№АИЃКD
ЁЁ[Р§8] гавЛЧІЮ§КЯН№жЪСПЮЊ100gЃЌЭъШЋбѕЛЏКѓЕУЕНбѕЛЏЮяЕФЛьКЯЮяжЪСПЮЊ116gЃЌЧѓКЯН№жаЧІЁЂЮ§ЕФжЪСПЗжЪ§ИїЮЊЖрЩйЃП
ЁЁНтЗЈвЛЃК
ЁЁЗжЮіЃКЩш100gЧІЮ§КЯН№жаКЌЮ§xgЃЌдђКЌЧІ(100-x)gЁЃЂйSnбѕЛЏКѓЕФЮШЖЈВњЮяЪЧSnO2(+4МлбѕЛЏЮяЮШЖЈ)ЃЌSnЕФЯрЖддзгжЪСПЮЊ
ЁЁ
ЁЁPbбѕЛЏКѓЕФЮШЖЈВњЮяЪЧPbO(+2МлбѕЛЏЮяЮШЖЈ)ЃЌ PbЕФЯрЖддзгжЪСПЮЊ207ЃЌPbOЕФЪНСПЮЊ223ЃЌ(100-x)g PbбѕЛЏЩњГЩЕФPbOжЪСПБи
ЁЁ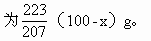
ЁЁвђЮЊSnO2гыPbOжЪСПЙВЮЊ116gЃЌЙЪПЩСавЛдЊвЛДЮЗНГЬЃЌНтЗНГЬЧѓГіSnЁЂPbжЪСПЁЃ
ЁЁ[Нт] Щш100gЮ§ЧІКЯН№жаКЌЮ§xgЃЌКЌЧІЮЊ(100-x)gЁЃ
ЁЁИљОнЛЏбЇЪНЫљБэЪОЕФдЊЫижЪСПЗжЪ§МАЬтвтЃЌСаДњЪ§ЗНГЬЪНЃК
ЁЁ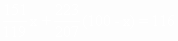
ЁЁНтЕУx=43.2(g)
ЁЁ100-x=100-43.2=56.8(g)
ЁЁ
ЁЁД№ЃККЯН№жаЮ§ЁЂЧІжЪСПЗжЪ§ЗжБ№ЮЊ43.2%ЁЂ56.8%
ЁЁНтЗЈЖўЃК
ЁЁЗжЮіЃКДЫЬтРћгУЮяжЪЕФСПМЦЫувВКмЗНБуЁЃЩш100gКЯН№жаКЌxgЃЌКЌЧІЮЊ(100-x)g
ЁЁ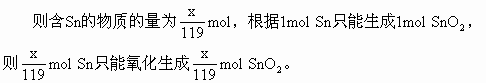
ЁЁ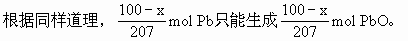
ЁЁНЋSnO2гыPbOгЩЮяжЪЕФСПЛЛЫуГЩжЪСПЃЌжЪСПКЭЮЊ116gЁЃ
ЁЁНтЃКЩш100gЮ§ЧІКЯН№жаКЌЮ§ЮЊxgЃЌКЌЧІЮЊ(100-x)g
ЁЁSnЕФЮяжЪЕФСП=SnO2ЕФЮяжЪЕФСП
ЁЁ
ЁЁPbЕФЮяжЪЕФСП=PbOЕФЮяжЪЕФСП
ЁЁ
ЁЁSnO2гыPbOжЪСПКЭЮЊ116g
ЁЁ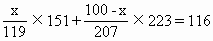
|
ЁЁНтЕУ x=43.2(g) |
ЁЁ(Ю§ЕФжЪСП) |
|
ЁЁ100-x=56.8(g) |
ЁЁ(ЧІЕФжЪСП) |
ЁЁ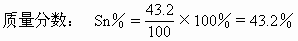
ЁЁPb%=1-43.2%=56.8%
ЁЁД№ЃККЯН№жаЧІЁЂЮ§ЗжБ№еМ56.8%ЁЂ43.2%
ЁЁ [Р§9] ГЦШЁСНЗнгЩЬМЫсФЦЁЂЬМЫсЧтФЦКЭЬМЫсЧтяЇзщГЩЕФЛьКЯЮя7.06gЁЃЦфжаЃКвЛЗнМгШыЙ§СПЕФбЮЫсЃЌПЩЕУCO2ЮЊ1792mL(дкБъзМзДПіЯТ)ЃЌСэвЛЗнМгШШжСжЪСПВЛдйМѕЩйЪБЮЊжЙЁЃРфШДКѓдйИњЙ§СПбЮЫсЗДгІЃЌПЩЕУCO2ЮЊ896mL(дкБъзМзДПіЯТ)ЁЃЧѓдЛьКЯЮяжаЃЌЬМЫсФЦЁЂЬМЫсЧтФЦКЭЬМЫсЧтяЇЕФЮяжЪЕФСПжЎБШЁЃ
ЁЁЗжЮіЃКДЫЬтЪЧИљОнЛЏбЇЗНГЬЪНЃЌМЦЫуЛьКЯЮяГЩЗжЮяжЪЕФСПжЎБШЕФЬтЁЃНтЬтЙиМќдкгке§ШЗХаЖЯЗДгІЮягыЩњГЩЮяЁЂЗДгІЮяЕФСПгыЩњГЩЮяЕФСПжЎМфЕФЙиЯЕЁЃ
ЁЁЕквЛЗн7.06gЛьКЯЮяЃЌИїГЩЗжЖМИњЙ§СПЕФбЮЫсГфЗжЗДгІЃЌОљЩњГЩCO2ЁЃCO2ЬхЛ§жЎКЭЮЊ1792mLЃЛЕкЖўЗн7.06gЛьКЯЮяМгШШКѓЃЌГ§ЬМЫсЧтФЦзЊЛЏЮЊЬМЫсФЦЭтЃЌЬМЫсЧтяЇдђвђШЋВПзЊБфЮЊЦјЬЌЮяжЪЖјВЛДцдкЙЬЬхЮяжЪСЫЁЃЛьКЯЮяжадгаЬМЫсФЦМАЩњГЩЕФЬМЫсФЦЙВЭЌИњЙ§СПбЮЫсЗДгІЃЌЩњГЩ896mLCO2ЁЃ
ЁЁНт ШЋЙ§ГЬЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК
|
ЁЁNa2CO3+2HCl==2NaCl+H2O+CO2Ёќ |
(1) |
|
ЁЁNaHCO3+HCl==NaCl+H2O+CO2Ёќ |
(2) |
|
ЁЁNH4HCO3+HCl==NH4Cl+H2O+CO2Ёќ |
(3) |
ЁЁ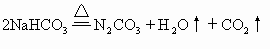 |
(4) |
ЁЁ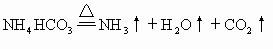 |
(5) |
ЁЁЁЁЩш7.06gИУЛьКЯЮяжаКЌNa2CO3ЁЂNaHCO3ЁЂNH4HCO3ЗжБ№ЮЊxЁЂyЁЂzmol
ЁЁДгЛЏбЇЗНГЬЪН(1)(2)(3)ПЩжЊЃЌЕквЛЗн7.06gЛьКЯЮягыЙ§СПбЮЫсЗДгІЃЌЙВЩњГЩCO2ЮЊ(x+y+z)mol
ЁЁ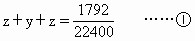
ЁЁДгЛЏбЇЗНГЬЪН(4)ЁЂ(5)ПЩжЊЃЌЕкЖўЗн7.06gЛьКЯЮяМгШШЃЌЦфжа
ЁЁ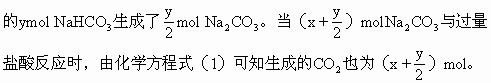

xЁУyЁУz=0.02ЁУ0.04ЁУ0.02=1ЁУ2ЁУ1
ЁЁД№ЃКNa2CO3ЁЂNaHCO3ЁЂNH4HCO3ЕФЮяжЪЕФСПжЎБШЮЊ1ЁУ2ЁУ1ЁЃ
ЁЁаТаЭЮоЛњЗЧН№ЪєВФСЯ
ЁЁ[Р§10] аТаЭЮоЛњЗЧН№ЪєВФСЯИњДЋЭГЙшЫсбЮВФСЯЯрБШЃЌгаЪВУДЬиадЃП
ЁЁ[ЗжЮі] (1)ФмГаЪмИпЮТЃЌЧПЖШИпЁЃШчЕЊЛЏЙшЬеДЩдк1200ЁцЪБШдОпгаИпЧПЖШЁЃ
ЁЁ(2)ОпгаЕчбЇЬиадЁЃгаЕФПЩзїОјдЕЬхЃЌгаЕФПЩзїАыЕМЬхЁЂЕМЬхЁЂГЌЕМЬхЁЃ
ЁЁ(3)ОпгаЙтбЇЬиадЁЃгаЕФФмЗЂГіИїЩЋЙтЃЌгаЕФФмЭИЙ§ПЩМћЙтЃЌгаЕФФмЪЙКьЭтЯпЁЂРзДяЩфЯпДЉЙ§ЁЃ
ЁЁ(4)ОпгаЩњЮяЙІФмЁЃгааЉЖдШЫЬхзщжЏгаНЯКУЕФЪЪгІадЃЌЧвгВЖШИпЁЂЮоЖОЁЂВЛШмгкЫЎЃЌПЩжБНгжВгкШЫЬхФкЁЃ
ЁЁ[Д№АИ] ТдЁЃ
ЁЁ ЁЁ[Р§11] ЧыБШНЯКьБІЪЏКЭРЖБІЪЏГЩЗжЕФвьЭЌЁЃШЫдьКьБІЪЏКЭШЫдьРЖБІЪЏИїгаКЮгУЭОЃП
ЁЁ[НтД№] СНепЕФжївЊГЩЗжЖМЪЧAl2O3(Иегё)ЁЃИегёжаЛьгаЩйСПИѕЪБЃЌГЪЯжКьЩЋЃЌОЭаЮГЩКьБІЪЏЃЛИегёжаЛьгаЩйСПюбЪБЃЌГЪЯжРЖЩЋЃЌОЭаЮГЩРЖБІЪЏЁЃ
ЁЁШЫдьКьБІЪЏгВЖШИпЃЌПЩжЦжгБэЕФжсГаЃЌЫќФмЗХДѓФГвЛВЈГЄЕФЙтЖјВњЩњМЄЙтЃЌПЩзїЙЬЬхМЄЙтЦїЁЃШЫдьРЖБІЪЏвђФмЪЙзЯЭтЯпКЭПЩМћЙтЭЈЙ§ЃЌПЩгУгкжЦдьЙтбЇвЧЦїЁЃ
ЁЁ ЁЁ[Р§12] ЯТСаЫЕЗЈе§ШЗЕФЪЧ [ ]
ЁЁAЃЎЖўбѕЛЏЙшШмгкЫЎЯдЫсад
ЁЁBЃЎЙтЕМЯЫЮЌДЋЕМЙтЕФФмСІЗЧГЃЧПЃЌРћгУЙтРТЭЈбЖЃЌФмЭЌЪБДЋЫЭДѓСПаХЯЂ
ЁЁCЃЎвђЮЊИпЮТЪБЖўбѕЛЏЙшгыЬМЫсФЦЗДгІЗХГіCO2ЃЌЫљвдЙшЫсЕФЫсадБШЬМЫсЧП
ЁЁDЃЎЖўбѕЛЏЙшЪЧЫсадбѕЛЏЮяЃЌЫќВЛШмгкШЮКЮЫсЁЃ
ЁЁЗжЮі ЖўбѕЛЏЙшВЛШмгкЫЎЃЌВЛШмгкЧПЫсЃЌЕЋШмгкЧтЗњЫсЁЃвђЮЊЫќФмгыМюЗДгІЩњГЩбЮКЭЫЎЃЌЫљвдЫќЪЧЫсадбѕЛЏЮяЁЃЙшЫсЫсадБШЬМЫсШѕЃЌЫќЗДгГдкCO2ЭЈШыNa2SiO3ШмвКПЩЩњГЩЙшЫсЁЃЖјSiO2ФмКЭNa2CO3ИпЮТЯТЗДгІЩњГЩCO2ЃЌЫќПЩЫЕУїВЛЛгЗЂЕФSiO2ПЩАбЦјЬхCO2жЦГіЃЌЕЋВЛФмЫЕУїЬМЫсКЭЙшЫсЕФЯрЖдЧПШѕЁЃ
ЁЁД№АИЃКB
ЙшЫсбЮЪЧгЩЙшЁЂбѕЁЂН№ЪєдЊЫизщГЩЕФЛЏКЯЮяЕФзмГЦЃЌЗжВМЙуЃЌНсЙЙИДдгЛЏбЇаджЪЮШЖЈЁЃвЛАуВЛШмгкЫЎЁЃ(Na2SiO3 ЁЂK2SiO3Г§Эт)зюЕфаЭЕФДњБэЪЧЙшЫсФЦNa2SiO3 ЃКПЩШмЃЌЦфЫЎШмвКГЦзїЫЎВЃСЇКЭХнЛЈМюЃЌПЩзїЗЪдэЬюСЯЁЂФОВФЗРЛ№МСКЭ№ЄНКМСЁЃ ГЃгУЙшЫсбЮВњЦЗЃКВЃСЇЁЂЬеДЩЁЂЫЎФрЁЃ
2ЃЎ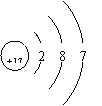 ЙшЕЅжЪгыЬМЯрЫЦЃЌгаОЇЬхКЭЮоЖЈаЮСНжжЁЃОЇЬхЙшНсЙЙРрЫЦгкН№ИеЪЏЃЌгаН№ЪєЙтдѓЕФЛвКкЩЋЙЬЬхЃЌШлЕуИп(1410Ёц)ЃЌгВЖШДѓЃЌНЯДрЃЌГЃЮТЯТЛЏбЇаджЪВЛЛюЦУЁЃЪЧСМКУЕФАыЕМЬхЃЌгІгУЃКАыЕМЬхОЇЬхЙмМАаОЦЌЁЂЙтЕчГиЁЃ
ЙшЕЅжЪгыЬМЯрЫЦЃЌгаОЇЬхКЭЮоЖЈаЮСНжжЁЃОЇЬхЙшНсЙЙРрЫЦгкН№ИеЪЏЃЌгаН№ЪєЙтдѓЕФЛвКкЩЋЙЬЬхЃЌШлЕуИп(1410Ёц)ЃЌгВЖШДѓЃЌНЯДрЃЌГЃЮТЯТЛЏбЇаджЪВЛЛюЦУЁЃЪЧСМКУЕФАыЕМЬхЃЌгІгУЃКАыЕМЬхОЇЬхЙмМАаОЦЌЁЂЙтЕчГиЁЃ
21.(9Зж)ЪЕбщЪвгУЯЁЯѕЫсгыЭЗДгІРДжЦБИNOЦјЬхЃЌШчЙћВЩгУ(Ђё)зАжУ(ЩеЦПФкМгШыЯЁЯѕЫсКЭЭЦЌЃЌБивЊЪБПЩМгШШ)ЁЃЪЕбщаЇЙћВЛЪЎЗжРэЯыЃЌвђЮЊДгЙлВьЕНЕФЯжЯѓВЛФмгаСІжЄУїЗДгІВњЮяЪЧNOЃЛгаШЫЩшМЦСЫ(Ђђ)зАжУ(Я№ЦЄШћЯТЖЫСЌгаЭЫПШІ)ЃЌгУРДзіИУЪЕбщПЩвдДяЕНТњвтЕФаЇЙћЁЃ
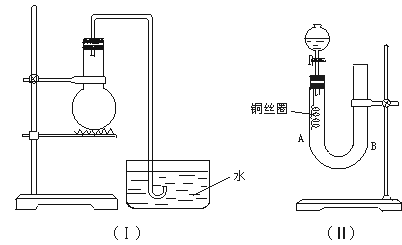
(1)гУЂёзАжУзіЪЕбщЪБЃЌгУХХЫЎЗЈЪеМЏЕНЕФЦјЬхЕФбеЩЋЮЊЁЁЁЁЁЁЁЁ ЁЁЩЋЃЛЪЕбщЙ§ГЬжагЩгкЙлВьЕНЁЁЁЁЁЁЁЁ ЯжЯѓЃЌЖјВЛФмгаСІжЄУїЗДгІВњЮяЪЧNOЁЃЁЁ
(2)гУЂђзАжУзіЪЕбщЪБЃЌНЋгаЙиВйзїВЙГфЭъШЋЃКЁЁ
ЂйНЋЗжвКТЉЖЗЕФЛюШћДђПЊЃЌДгUаЮЙмЕФBВрЙмПкзЂШыЯЁЯѕЫсЃЌвЛжБзЂЕНЁЁЁЁЁЁЁЁ ЮЊжЙЁЃ
ЂкЙиБеЛюШћЃЌгУОЦОЋЕЦдкUаЮЙмЕФAВрМгШШЃЌЕБЁЁЁЁЁЁЁЁ ЪБЃЌСЂМДГЗШЅОЦОЋЕЦЁЃ
(3)ЛиД№ЯТСаЮЪЬтЃКЁЁ
ЂйЗДгІдкЪВУДЧщПіЯТПЩвдздЖЏЭЃжЙЃППЩдкКЮДІЙлВьЕНЮоЩЋЕФNOЦјЬхЃПЁЁ
ЂкШчЙћдйНЋЗжвКТЉЖЗЕФЛюШћТ§Т§ДђПЊЃЌПЩСЂМДЙлВьЕНФФаЉУїЯдЯжЯѓЃП
20.(11Зж)ЪЕбщЪвГЃгУБЅКЭNaNO2гыNH4ClШмвКЗДгІжЦШЁДПОЛЕЊЦјЃЌЗДгІЪНЮЊЃКNH4Cl+NaNO2 NaCl+N2Ёќ+2H2OЃЌІЄHЃМ0ЃЌЪЕбщзАжУШчЯТЭМЫљЪОЃЌЪдЛиД№ЃКЁЁ
NaCl+N2Ёќ+2H2OЃЌІЄHЃМ0ЃЌЪЕбщзАжУШчЯТЭМЫљЪОЃЌЪдЛиД№ЃКЁЁ
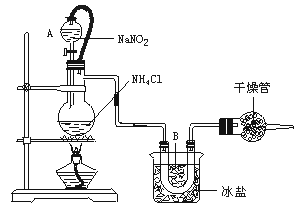
ЁЁ(1)зАжУжаAВПЗжЕФЗжвКТЉЖЗгыеєСѓЩеЦПжЎМфСЌНгЕФЕМЙмЫљЦ№ЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁ (ЬюаДБрКХ)ЁЃ
a.ЗРжЙNaNO2БЅКЭШмвКеєЗЂЁЁ
b.БЃжЄЪЕбщзАжУВЛТЉЦјЁЁ
c.ЪЙNaNO2БЅКЭШмвКШнвзЕЮЯТЁЁ
(2)BВПЗжЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
a.РфФ§ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ b.РфШДЕЊЦјЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ c.ЛКГхЕЊЦјСїЁЁ
(3)МгШШЧАБиаыНјааЕФвЛИіВйзїВНжшЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛМгШШЦЌПЬКѓЃЌМДгІвЦШЅОЦОЋЕЦвдЗРЗДгІЮяГхГіЃЌЦфдвђЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ЪеМЏN2ЧАЃЌБиаыНјааЕФВйзїВНжшЪЧ(гУЮФзжЫЕУї)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃЪеМЏN2зюЪЪвЫЕФЗНЗЈЪЧ(ЬюаДБрКХ)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
a.гУХХЦјЗЈЪеМЏдкМЏЦјЦПжаЁЁ
b.гУХХЫЎЗЈЪеМЏдкМЏЦјЦПжаЁЁ
c.жБНгЪеМЏдкЧђЕЈЛђЫмСЯДќжа
19.(10Зж)ШчгвЫљЪОAЁЂBЁЂCЁЂDЁЂEБфЛЏЙиЯЕЭјЃЌОљЪЁШЅСЫЗДгІЫљашЬѕМўЃЌЁЁ
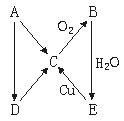
(1)ШчЙћAЮЊЦјЬхЕЅжЪЃЌдђЃКAЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌBЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌCЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌDЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌEЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ШчЙћAЮЊЙЬЬхЕЅжЪЃЌдђЃКЁЁ
AЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌBЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌCЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌDЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌEЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ(ОљЬюЗжзгЪН)
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com