
题目列表(包括答案和解析)
5.原子和离子结构示意图
注意:①要熟练地书写1-20号元素的原子和离子结构示意图。
②要正确区分原子结构示意图和离子结构示意图(通过比较核内质子数和核外电子数)。
4.核外电子排布规律
⑴核外电子是由里向外,分层排布的。
⑵各电子层最多容纳的电子数为2n2个;最外层电子数不得超过8个,次外层电子数不得超过18个,倒数第三层电子数不得超过32个。
⑶以上几点互相联系。
核外电子排布规律是书写结构示意图的主要依据。
3.相对原子质量
⑴原子的相对原子质量:以一个12C原子质量的1/12作为标准,其它原子的质量跟它相比较所得的数值。它是相对质量,单位为1,可忽略不写。
⑵元素的相对原子质量:是按该元素的各种同位素的原子百分比与其相对原子质量的乘积所得的平均值。元素周期表中的相对原子质量就是指元素的相对原子质量。
2.同位素
⑴要点:同--质子数相同,异--中子数不同,微粒--原子。
⑵特点:同位素的化学性质几乎完全相同;自然界中稳定同位素的原子个数百分数不变。
注意:同种元素的同位素可组成不同的单质或化合物,如H2O和D2O是两种不同的物质。
1.几个量的关系(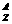 X)
X)
质量数(A)=质子数(Z)+中子数(N)
质子数=核电荷数=原子序数=原子的核外电子数
离子电荷数=质子数-核外电子数
16、O 、S 、P 、 略
15、N 、P 、CO 、CO2 、
14、⑴N2O5 N2O3 ⑵2Li+2H2O=2LiOH+H2↑ ⑶PH3<NH3
7、D 8、CD 9、A 10、BC 11、AB 12、B 13、D
1、B 2、AD 3、B 4、AC 5、AD 6、A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com