
题目列表(包括答案和解析)
8.toC时,将一定质量的某物质的不饱和溶液均分为三份,分别加热蒸发溶液,然后把温度降至toC,已知从三份溶液中蒸发的溶液剂分别为10g、20g、30g,析出晶体(不含结晶水)质量分别为a、b、c(单位g,且a、b、c均大于零),则a、b、c三者的关系为
A.c=2b-a B.c=a+b C.c=a+2b D.c=2a+b
7.将含有0.400 mol Cu(NO3)2和0.400 mol KCl的水溶液1 L,用惰性电极电解一段时间后,在一个电极上能析出0.300 mol铜,此时在另一电极上放出的气体在标准状况下的体积约为
A.1.12 L B.大于5.6 L小于6.72 L
C.6.72 L D.大于1.12 L小于5.6 L
6.下列离子方程式正确的是( )
A.向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+ H2O
B.向硫氢化钠溶液中滴加几滴硫酸铜溶液:Cu2++HS-=CuS↓+H+

C.用石墨电极电解MgCl2溶液:2H2O+2Cl- = 2OH-+H2↑+Cl2↑
D.往苯酚钠溶液中通入少量CO2:
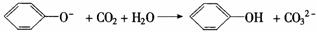
5.铁氧体(Fe3O4)法是处理含铬废水的常用方法.其原理是:用FeSO4把废水中Cr2O72-离子还原为Cr3+离子,井通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或FeO·Fe2O3)的复合氧化物(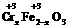 ·
·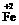 O)。处理含1 mol Cr2O72-的废水至少需要加入a mol FeSO4·7H2O,下列结论正确的是
( )
O)。处理含1 mol Cr2O72-的废水至少需要加入a mol FeSO4·7H2O,下列结论正确的是
( )
A.x=1,a=5 B.x=0.5 a=8 C.x=2,a=10 D.x=0.5,a=10
4.向三份相同浓度、等体积的稀硫酸中分别放入镁、铝、铁三种金属,金属全部消耗完后,所得溶液的质量相等,则放入的三种金属的质量关系是 ( )
A.铝、镁、铁依次减少 B.镁、铝、铁依次减少
C.铁、镁、铝依次减少 D.铝、铁、镁依次减少
3.在某温度下,将2 mol A和3 mol B充入一密闭容器中,发生反应:
aA(气)+ B(气) C(气)+ D(气)
C(气)+ D(气)
5 min后达到平衡。已知各物质的平衡浓度的关系为:[A]a [B] = [C][D]
若在温度不变情况下将容器的体积扩大为原来的10倍,其A的转化率不发生变化,则B的转化率为 ( )
A.60% B.40% C.24% D.4%
2.CuCO3 和Cu2(OH)2CO3的混合物34.6 g ,可恰好完全溶解于300ml、2 mol.L-1的盐酸溶液中,加热分解等量的这种混合物可得CuO ( )
A.16.0 g B.19.2 g C.24.0 g D.30.6 g
1.a mol铜跟含b molHNO3的硝酸溶液恰好完全反应,则被还原的HNO3的物质的量一定是
A.(b-2a)mol B.b/4mol C.2a/3mol D.2amol
16.下列溶液中,微粒浓度关系正确的是( )
A.含有NH4+、Cl-、H+、OH-离子的溶液中,其离子浓度一定是:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.pH=8的氨水与氯化铵的混合溶液中:c(Cl-)>c(NH4+)
C.0.1mol/L 的Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S)
D.pH=3的一元酸和pH=11的一元强碱等体积混合后的溶液中:c(OH-)=c(H+)
15.现有t℃时质量分数为a %的KNO3溶液m g,将其分成质量比为1∶2的甲、乙两份溶液。甲溶液蒸发5 g水,恢复到原温度时析出晶体2 g;乙溶液蒸发12 g水,恢复到原温度时析出晶体5 g。则下列说法正确的是 ( )
A.t℃时,KNO3溶解度为41.7 g B.t℃时,KNO3溶解度为40 g
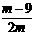 C.t℃时,原KNO3溶液中溶质质量分数为 D.t℃时,原KNO3溶液中溶质质量分数为
C.t℃时,原KNO3溶液中溶质质量分数为 D.t℃时,原KNO3溶液中溶质质量分数为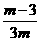
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com