
题目列表(包括答案和解析)
43. a mol FeS与b mol FeO投入到V L、C mol•L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液的成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为
A.(a+b)×63g B.(a+b)×189g
C.(a+b)mol D.(CV-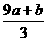 )mol
)mol
42.由FeO 、Fe2O3 、Fe3O4组成的混合物,测得其中铁元素与氧元素的质量比为21∶8,则这种混合物中FeO 、Fe2O3 、Fe3O4的物质的量之比可能为
A、1∶2∶1 B、2∶1∶1 C、1∶1∶1 D、1∶1∶3
41.将15 g铁粉溶于1 L稀硝酸中恰好完全反应,放出NO气体后称量所得溶液,发现比原溶液质量增加9 g,则原溶液中硝酸的浓度为
A、1.0 mol·L-1 B、0.8 mol·L-1 C、0.6 mol·L-1 D、0.4 mol·L-1
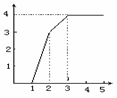
40.某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如下图所示(横坐标表示加入铁粉的物质的量)。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为
A.1∶1∶1 B.1∶3∶1 C.1∶1∶4 D.3∶3∶8
39.含n
g硝酸的稀溶液恰好和m g铁粉完全反应,若有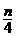 g HNO3 被还原成NO,n:m可能是
g HNO3 被还原成NO,n:m可能是
 A、1:1 B、2:1 C、3:1 D、9:2
A、1:1 B、2:1 C、3:1 D、9:2
38.将一定量铁粉和硫粉的温合物隔绝空气共热,充分反应后冷却,再加入足量稀H2SO4,得
到标准状况下的气体11.2L,则原混合物可能的组成是(n代表物质的量)
A.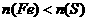 ,总质量等于44g B.
,总质量等于44g B. ,总质量等于44g
,总质量等于44g
C.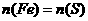 ,总质量大于44g D.
,总质量大于44g D. ,总质量小于44g
,总质量小于44g
37.将适量的铁粉放入三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是
A、2∶3 B、3∶2 C、1∶2 D、1∶1
36. 铁粉和铜粉的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):
|
编号 |
① |
② |
③ |
④ |
|
稀硝酸体积/mL |
100 |
200 |
300 |
400 |
|
剩余金属/g |
18.0 |
9.6 |
0 |
0 |
|
NO体积/mL |
2240 |
4480 |
6720 |
V |
下列计算结果正确的是
A. ①中溶解了5.6gFe B.硝酸的浓度为4mol/L
C. ②中溶解了9.6gCu D.④中V=8960
35.向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL l moL/L的盐酸;恰好使混合物完全溶解并放出标准状况下224mL气体。向所得溶液中加入KSCN溶液无血红色出现,若用足量的CO在高温下还原相同质量的此混合物,能得到单质铁的质量为
A.11.2g B.2.8g C.5.6g D.无法计算
34.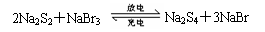 下图是一种正在投入生产的大型蓄电系统的原理图。电池中的左右两侧为电极,中间为离
下图是一种正在投入生产的大型蓄电系统的原理图。电池中的左右两侧为电极,中间为离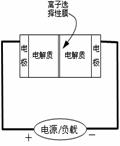 子选择性膜,在电池放电和充电时该膜只允许钠离子通过。电池充、放电的化学反应方程式为:
子选择性膜,在电池放电和充电时该膜只允许钠离子通过。电池充、放电的化学反应方程式为:
下列关于此电池说法正确的是
A.充电的过程中当0.1molNa+通过离子交换膜时,导线通过0.1mol电子
B.电池放电时,负极反应为:3NaBr-2e-=NaBr3+2Na+
C.充电过程中钠离子从右到左通过离子交换膜
D.放电过程中钠离子从右到左通过离子交换膜
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com