
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
1£®°Ń3molAŗĶ2.5 molB»ģŗĻŹ¢ČėČŻ»żĪŖ2LµÄČŻĘ÷ÄŚ£¬·¢Éś·“Ó¦£ŗ
3 A(g) + B(g)  ””x C(g)+2 D(g)
””x C(g)+2 D(g)
5minŗó“ļµ½Ę½ŗā²¢Éś³É1molD£¬²āµĆCµÄĘ½¾łÉś³ÉĖŁĀŹĪŖ0.1 mol”¤L-1”¤min-1£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®xµÄŹżÖµĪŖ2”””””””””””””””””””””””””””””””””””””””””””””””””””””” B£®AµÄĘ½¾łĻūŗÄĖŁĀŹĪŖ0.3 mol.L-1”¤min-1
C£®BµÄ×Ŗ»ÆĀŹĪŖ80©”””””””””””””””””””””””””””””””””””””””””” D£®BµÄĘ½ŗāÅضČĪŖ2 mol”¤L-1
13£® (14·Ö)XeŗĶF2ŌŚ²»Ķ¬ĪĀ¶ČĻĀ·“Ó¦æɵĆXeF6”¢XeF4ŗĶXeF2ČżÖÖ·ś»ÆĪļ£¬ĻĀĶ¼±ķŹöµÄŹĒ½«0.125mol/L
XeŗĶ1.225mol/L F2ĪŖĘšŹ¼·“Ó¦Īļ£¬ŌŚŅ»øöĢå»ż¹Ģ¶ØµÄČŻĘ÷ÄŚ·¢Éś·“Ó¦£¬µĆµ½µÄÉś³ÉĪļŌŚĘ½ŗāĢåĻµÄŚµÄĪļÖŹµÄĮæ·ÖŹżÓė·“Ó¦ĪĀ¶ČµÄ¹ŲĻµ”£
(14·Ö)XeŗĶF2ŌŚ²»Ķ¬ĪĀ¶ČĻĀ·“Ó¦æɵĆXeF6”¢XeF4ŗĶXeF2ČżÖÖ·ś»ÆĪļ£¬ĻĀĶ¼±ķŹöµÄŹĒ½«0.125mol/L
XeŗĶ1.225mol/L F2ĪŖĘšŹ¼·“Ó¦Īļ£¬ŌŚŅ»øöĢå»ż¹Ģ¶ØµÄČŻĘ÷ÄŚ·¢Éś·“Ó¦£¬µĆµ½µÄÉś³ÉĪļŌŚĘ½ŗāĢåĻµÄŚµÄĪļÖŹµÄĮæ·ÖŹżÓė·“Ó¦ĪĀ¶ČµÄ¹ŲĻµ”£
(1)420KŹ±£¬·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
”” _________________________________”£
(2)ÖʱøXeF6ŗĶXeF4×īŹŹŅĖµÄĪĀ¶Č·Ö±šŌ¼ĪŖ
””__________KŗĶ__________K”£
(3)600-800KŹ±£¬»į·¢Éś·“Ó¦£ŗ
XeF6(g) XeF4(g)+ F2(g)£¬Ęä·“Ó¦ČČ”÷H _______0(Ģī”°>”±”°=”±»ņ”°<”±)”£ĄķÓÉŹĒ______________________________________________________________
XeF4(g)+ F2(g)£¬Ęä·“Ó¦ČČ”÷H _______0(Ģī”°>”±”°=”±»ņ”°<”±)”£ĄķÓÉŹĒ______________________________________________________________
”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” ”£
(4)900KŹ±£¬ČŻĘ÷ÖŠ“ęŌŚµÄ×é·ÖÓŠ_________________________________”£
(5)ČōŌŚÄ³ĪĀ¶ČĻĀ£¬·“Ӧֻɜ³ÉXeF2£¬ĘäĪļÖŹµÄĮæ·ÖŹżĪŖ0.08£¬Ēó·“Ó¦»ģŗĻĪļÖŠXeF2µÄÅØ¶Č”£(Š“³ö¼ĘĖć¹ż³Ģ)
12£®(8·Ö)¼ŲŹĒ-ÖÖ»īĘĆµÄ½šŹō£¬¹¤ŅµÉĻĶس£ÓĆ½šŹōÄĘŗĶĀČ»Æ¼ŲŌŚøßĪĀĻĀ·“Ó¦ÖĘČ””£øĆ·“Ó¦ĪŖ£ŗNa(l)+KCl(l) NaCl(l)+K(g)(¦¤H >0)£¬ø÷ĪļÖŹµÄ·ŠµćÓėŃ¹ĒæµÄ¹ŲĻµ¼ūĻĀ±ķ”£
NaCl(l)+K(g)(¦¤H >0)£¬ø÷ĪļÖŹµÄ·ŠµćÓėŃ¹ĒæµÄ¹ŲĻµ¼ūĻĀ±ķ”£
|
Ń¹Ēæ(kPa) |
13.33 |
53.32 |
101.3 |
|
KµÄ·Šµć(”ę) |
590 |
710 |
770 |
|
NaµÄ·Šµć(”ę) |
700 |
830 |
890 |
|
KClµÄ·Šµć(”ę) |
”” |
”” |
1437 |
|
NaClµÄ·Šµć(”ę) |
”” |
”” |
1465 |
(1)ŌŚ³£Ń¹ĻĀ½šŹō¼Ų×Ŗ±äĪŖĘųĢ¬“Ó·“Ó¦»ģŗĻĪļÖŠ·ÖĄėµÄ×īµĶĪĀ¶ČŌ¼ĪŖ”””””””””” £¬¶ų·“Ó¦µÄ×īøßĪĀ¶ČÓ¦µĶÓŚ”””””””” ”””””£
(2)ŌŚÖĘČ”¼ŲµÄ¹ż³ĢÖŠ£¬ĪŖĮĖĢįøßŌĮĻµÄ×Ŗ »ÆĀŹæÉŅŌ²ÉČ”µÄ“ėŹ©ŹĒ””””””””””””””
”””””””””””””””””””””””””””””” ”£
(3)³£Ń¹ĻĀ£¬µ±·“Ó¦ĪĀ¶ČÉżøßµ½900”ꏱ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżæɱķŹ¾ĪŖ£ŗK£½”””””””””” ”””£
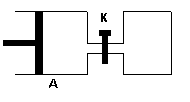
11£®(12·Ö)ČēĶ¼ĖłŹ¾£¬ČŻĘ÷A×ó²ąŹĒæÉĘ½ŠŠŅĘ¶ÆµÄ»īČū”£ĻņAÖŠ³äČė1molXŗĶ1molY£¬ĻņBÖŠ³äČė2molXŗĶ2molY£¬ĘšŹ¼Ź±V(A)=V(B)=aL”£ŌŚĻąĶ¬ĪĀ¶ČŗĶÓŠ“߻ƼĮ“ęŌŚµÄĢõ¼žĻĀ£¬Į½ČŻĘ÷ø÷×Ō·¢Éś£ŗX(g)+Y(g)  Z(g)+2W(g)£»∆H<0“ļµ½Ę½ŗāŹ±V(A)=1.2aL”£ŹŌ»Ų“š£ŗ
Z(g)+2W(g)£»∆H<0“ļµ½Ę½ŗāŹ±V(A)=1.2aL”£ŹŌ»Ų“š£ŗ
 (1)AÖŠXµÄ×Ŗ»ÆĀŹĪŖ””””””””””””””””””
ӣ
(1)AÖŠXµÄ×Ŗ»ÆĀŹĪŖ””””””””””””””””””
ӣ
(2)A”¢BÖŠX×Ŗ»ÆĀŹ“󊔹ŲĻµĪŖA”””””” B
(Ģī”°£¾”±”¢”°£¼”±”¢”°=”± )
(3)“ņæŖK£¬Ņ»¶ĪŹ±¼äŗóÓÖ“ļµ½ŠĀµÄĘ½ŗāŹ±£¬
AµÄĢå»żĪŖ”””””””””” L(Į¬ĶعÜÖŠĘųĢåĢå»ż²»¼Ę)
(4)ŌŚ(3)“ļµ½Ę½ŗāŗó£¬Ķ¬Ź±µČ·łÉżøßA”¢BµÄĪĀ¶Č£¬“ļµ½Ę½ŗāŗó£¬AµÄĢå»ż
”””””””” (Ģī±ä“󔢲»±ä”¢»ņ±äŠ”)£¬ĘäĄķÓÉŹĒ””””””””””””””””””””””””””
”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” ”£
10£®(12·Ö)Ņ»¶ØĢõ¼žĻĀ£¬ŌŚĢå»żĪŖ3 LµÄĆܱÕČŻĘ÷ÖŠ£¬Ņ»Ńõ»ÆĢ¼ÓėĒāĘų·“Ӧɜ³É¼×“¼(“߻ƼĮĪŖCu2O/ZnO)£ŗCO(g)+2H2(g) CH3OH(g)£¬øł¾ŻĢāŅāĶź³ÉĻĀĮŠø÷Ģā£ŗ
CH3OH(g)£¬øł¾ŻĢāŅāĶź³ÉĻĀĮŠø÷Ģā£ŗ
 ””
””
(1)·“Ó¦“ļµ½Ę½ŗāŹ±£¬Ę½ŗā³£Źż±ķ“ļŹ½K£½”””””””””” £¬
ÉżøßĪĀ¶Č£¬KÖµ”””””” (Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)”£
(2)ŌŚ500 ”ę£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹ
v (H2)£½”””””””””””””””””” ”£
(3)ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬¶Ō“¦ÓŚEµćµÄĢåĻµĢå»żŃ¹Ėõµ½ŌĄ“µÄ1/2£¬ĻĀĮŠÓŠ¹ŲøĆĢåĻµµÄĖµ·ØÕżČ·µÄŹĒ”””””””””” ”£”£
a£®ĒāĘųµÄÅØ¶Č¼õÉŁ”””””””” ”””””””””””””””” b£®Õż·“Ó¦ĖŁĀŹ¼Óæģ£¬Äę·“Ó¦ĖŁĀŹŅ²¼Óæģ
c£®¼×“¼µÄĪļÖŹµÄĮæŌö¼Ó”””” ”””””””””””””””” d£®ÖŲŠĀĘ½ŗāŹ±n(H2)/n(CH3OH)Ōö“ó
(4)¾ŻŃŠ¾æ£¬·“Ó¦¹ż³ĢÖŠĘš“ß»Æ×÷ÓƵÄĪŖCu2O£¬·“Ó¦ĢåĻµÖŠŗ¬ÉŁĮæCO2ÓŠĄūÓŚĪ¬³Ö“߻ƼĮCu2OµÄĮæ²»±ä£¬ŌŅņŹĒ£ŗ_________________________________(ÓĆ·½³ĢŹ½±ķŹ¾)”£
9£®(14·Ö)ѧĻ°ĮĖŌŖĖŲÖÜĘŚĀÉŗó£¬Ķ¬Ń§ĆĒ¶ŌµŚĖÄÖÜĘŚ¹ż¶ÉŌŖĖŲŃõ»ÆĪļ²śÉśĮĖÅØŗńµÄŠĖȤ”£ŹĒ·ńÖ»ÓŠ¶žŃõ»ÆĆĢÄÜ“ß»ÆĀČĖį¼ŲŹÜČČ·Ö½ā£æŃõ»ÆĢś”¢Ńõ»ÆĶ”¢Ńõ»ÆøõµČ¶ŌĀČĖį¼ŲµÄŹÜČČ·Ö½āӊƻӊ“ß»Æ×÷ÓĆ£æ¶Ō“ĖĖūĆĒ½ųŠŠĮĖŹµŃéĢ½¾æ”£ĒėÄćøł¾ŻŅŖĒóĶź³ÉĻĀĮŠ²æ·ÖŹµŃé±Øøę”£
I æĪĢāĆū³Ę£ŗ____________________________________________________________
IIŹµŃéŅĒĘ÷¼°ŹŌ¼Į£ŗ
ŹµŃéŅĒĘ÷£ŗ“ųĢś¼ŠµÄĢś¼ÜĢØ”¢“ųĻšĘ¤ČūµÄµ¼¹Ü”¢ĮæĘų×°ÖĆ”¢¹żĀĖ×°ÖĆ”¢µē×ÓĢģĘ½”¢Ņ©³×”¢____________”¢____________”¢____________µČ”£
ŹµŃéŹŌ¼Į£ŗ¶žŃõ»ÆĆĢ”¢Ńõ»ÆĢś”¢Ńõ»ÆĶ”¢Ńõ»ÆøõŗĶĀČĖį¼Ų
III ŹµŃé²½Öč£ŗĀŌ
IV ŹµŃ鏿¾Ż£ŗ
|
ŹµŃé ±ąŗÅ |
KClO3(g) |
Ńõ»ÆĪļ |
²śÉśĘųĢå(mL) |
ŗÄŹ±(s) |
||
|
»ÆѧŹ½ |
ÖŹĮæ(g) |
»ŲŹÕ |
(ŅŃÕŪĖćµ½±źæö) |
|||
|
1 |
0.60 |
£ |
£ |
£ |
10 |
480 |
|
2 |
0.60 |
MnO2 |
0.20 |
90% |
67.2 |
36.5 |
|
3 |
0.60 |
CuO |
0.20 |
90% |
67.2 |
79.5 |
|
4 |
0.60 |
Fe2O3 |
0.20 |
90% |
67.2 |
34.7 |
|
5 |
0.60 |
Cr2O3 |
0.20 |
Ņģ³£ |
67.2 |
188.3 |
V ŹµŃéĢÖĀŪ£ŗ
(1) ŌŚŃõ»ÆĪļµÄ»ŲŹÕ¹ż³ĢÖŠ£¬ŅŖ½ųŠŠ¹żĀĖ²Ł×÷£¬ĖłÓĆµÄ²£Į§ŅĒĘ÷ŹĒ²£Į§°ō”¢______”¢_____”£
(2) ŹµŃ鱹ŗÅ3µÄŹµŃéÖŠKClO3µÄ·Ö½āĀŹĪŖ_________%(±£ĮōŅ»Ī»Š”Źż)”£
(3) ŌŚÓĆCr2O3 ×öŃŠ¾æŹµŃ鏱£¬·¢ĻÖÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢå²śÉś£¬Ķ¬Ź±ĀĢÉ«µÄ»ģŗĻĪļ±ä³ÉĮĖ飻ĘÉ«”£øĆ“Ģ¼¤ŠŌĘųĢåŹĒ________(Ģī·Ö×ÓŹ½)£¬æÉÓĆ________________ŹŌÖ½¼ģŃ锣ÉĻŹöŅģ³£ĻÖĻó²śÉśµÄŌŅņŹĒ______________________________________________”£
VI ŹµŃé½įĀŪ£ŗ____________________________________________________________”£
8£® Ņ»¶ØĪĀ¶ČĻĀ£¬ÓŠæÉÄę·“Ó¦£ŗ2A(g)+2B(g)
Ņ»¶ØĪĀ¶ČĻĀ£¬ÓŠæÉÄę·“Ó¦£ŗ2A(g)+2B(g)  C(g)+3D(g)£»¦¤H£¼0”£ĻÖ½«2molAŗĶ2molB³äČėĢå»żĪŖVµÄ¼×ČŻĘ÷£¬½«2molCŗĶ6molD³äČėŅŅČŻĘ÷²¢Ź¹ŅŅČŻĘ÷ŌŚ·“Ó¦æŖŹ¼Ē°µÄĢå»żĪŖ2V(ČēĶ¼ĖłŹ¾)£¬±£³Ö·“Ó¦¹ż³ĢÖŠĮ½ČŻĘ÷µÄĪĀ¶ČÓėĘšŹ¼Ź±ĻąĶ¬”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
C(g)+3D(g)£»¦¤H£¼0”£ĻÖ½«2molAŗĶ2molB³äČėĢå»żĪŖVµÄ¼×ČŻĘ÷£¬½«2molCŗĶ6molD³äČėŅŅČŻĘ÷²¢Ź¹ŅŅČŻĘ÷ŌŚ·“Ó¦æŖŹ¼Ē°µÄĢå»żĪŖ2V(ČēĶ¼ĖłŹ¾)£¬±£³Ö·“Ó¦¹ż³ĢÖŠĮ½ČŻĘ÷µÄĪĀ¶ČÓėĘšŹ¼Ź±ĻąĶ¬”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®¼×”¢ŅŅĮ½ČŻĘ÷ÖŠµÄ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāŹ±£¬Į½ČŻĘ÷ÄŚŃ¹ĒæĻąµČ
B£®¼×”¢ŅŅĮ½ČŻĘ÷ÖŠµÄ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāŹ±£¬CµÄĢå»ż·ÖŹżĻąµČ
C£®Ļņ¼×ČŻĘ÷ÖŠŌŁ³äČė2molAŗĶ2molB£¬Ę½ŗāŗó¼×ÖŠĪļÖŹCµÄÅØ¶Č²»±ä
D£®ĻņŅŅČŻĘ÷ÖŠŌŁ³äČė2molCŗĶ6molD£¬Ę½ŗāŗóŅŅÖŠĪļÖŹCµÄÅضČĪŖŌĄ“µÄ2±¶
7£®ŌŚŅ»ĆܱÕČŻĘ÷ÖŠ³äČė2molAŗĶlmolB·¢Éś·“Ó¦£ŗ2A(g)+B(g)  xC(g)£¬“ļµ½Ę½ŗāŗó£¬CµÄĢå»ż·ÖŹżĪŖW%£¬ČōĪ¬³ÖČŻĘ÷µÄČŻ»żŗĶĪĀ¶Č²»±ä£¬°“ĘšŹ¼ĪļÖŹµÄĮæA
0.6molӢB
0.3molӢC
1.4mol³äČėČŻĘ÷“ļµ½Ę½ŗāŗó£¬CµÄĢå»ż·ÖŹżČŌĪŖW%”£ŌņĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ””
xC(g)£¬“ļµ½Ę½ŗāŗó£¬CµÄĢå»ż·ÖŹżĪŖW%£¬ČōĪ¬³ÖČŻĘ÷µÄČŻ»żŗĶĪĀ¶Č²»±ä£¬°“ĘšŹ¼ĪļÖŹµÄĮæA
0.6molӢB
0.3molӢC
1.4mol³äČėČŻĘ÷“ļµ½Ę½ŗāŗó£¬CµÄĢå»ż·ÖŹżČŌĪŖW%”£ŌņĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ””
”” A£®Ę½ŗāŹ±A ”¢BµÄĪļÖŹµÄĮæÖ®±ČŅ»¶ØĪŖ2£ŗ1”””””””””””” ”” B£®xµÄÖµæÉÄÜŹĒ2£¬Ņ²æÉÄÜŹĒ3
”” C£®Ę½ŗāŹ±A µÄĪļÖŹµÄĮæÓėŌĘ½ŗāŅ»¶ØĻąµČ”””””” ””D£®CµÄĢå»ż·ÖŹż²»æÉÄÜĪŖW%
6£®Ä³ĪĀ¶ČĻĀ£¬ŌŚČŻ»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠæÉ·¢ÉśæÉÄę·“Ó¦A(g)+2B(g) 2Q(g)£¬Ę½ŗāŹ±£¬ø÷ĪļÖŹµÄĮæÅØ¶Č±ČĪŖc(A)”Ćc(B)”Ćc(Q)£½1”Ć1”Ć2£¬±£³ÖĪĀ¶Č²»±ä£¬ŅŌ1”Ć1”Ć2µÄĢå»ż±ČŌŁ³äČėA”¢B”¢Q£¬ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ
2Q(g)£¬Ę½ŗāŹ±£¬ø÷ĪļÖŹµÄĮæÅØ¶Č±ČĪŖc(A)”Ćc(B)”Ćc(Q)£½1”Ć1”Ć2£¬±£³ÖĪĀ¶Č²»±ä£¬ŅŌ1”Ć1”Ć2µÄĢå»ż±ČŌŁ³äČėA”¢B”¢Q£¬ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ
”” A£®øÕ³äČėŹ±·“Ó¦ĖŁĀŹvÕż¼õÉŁ£¬vÄęŌö“ó
”” B£®“ļµ½ŠĀµÄĘ½ŗāŹ±£¬·“Ó¦»ģŗĻĪļÖŠA”¢BµÄĪļÖŹµÄĮæ·ÖŹżŌö¼Ó
”” C£®“ļµ½ŠĀµÄĘ½ŗāŹ±£¬c(A)”Ćc(B)”Ćc(Q)ČŌĪŖ1”Ć1”Ć2
”” D£®“ļµ½ŠĀµÄĘ½ŗā¹ż³ĢÖŠ£¬ĢåĻµŃ¹ĒæĻČŌö“ó£¬ŗóÖš½„¼õŠ”
5£®øł¾ŻĻĀĮŠÓŠ¹ŲĶ¼Ļó£¬Ėµ·Ø²»ÕżČ·µÄŹĒ
 ””
””
A£®ÓÉĶ¼Ļó¢ńÖŖ£¬øĆ·“Ó¦ŌŚT1”¢T3“¦“ļµ½Ę½ŗā£¬ĒŅøĆ·“Ó¦µÄ”÷H£¼0
B£®ÓÉĶ¼Ļó¢ņÖŖ£¬øĆ·“Ó¦ŌŚt5½×¶ĪNH3Ģå»ż·ÖŹż×ī“ó
C£®Ķ¼Ļó¢óŹĒŌŚ10LČŻĘ÷ÖŠ850”ꏱ·“Ó¦£¬ÓÉĶ¼ÖŖ£¬µ½4minŹ±£¬·“Ó¦·Å³ö51.6kJµÄČČĮæ
D£®ÓÉĶ¼Ļó¢ōÖŖ£¬ĻąĶ¬Ģõ¼žĻĀĘšŹ¼Ź±Ķ¶Čė0.3mol/LX”¢0.1mol/LYŗĶ0.4mol/LZ·“Ó¦£¬“ļµ½Ę½ŗāŗó£¬ZµÄÅضČĪŖ0.4mol/L
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com