
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
7ЃЎдквЛЖЈЮТЖШЯТЃЌЯђБЅКЭЩеМюШмвКжаЗХШыЩйСПЙ§бѕЛЏФЦЃЌЗДгІКѓЛиИДЕНдРДЕФЮТЖШЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
ЁЁЁЁЁЁ AЃЎШмвКЕФpHдіДѓЃЌгаO2ЗХГіЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎШмвКЕФpHВЛБфЃЌгаO2ЗХГі
CЃЎШмвКc(Na+)діДѓЃЌгаO2ЗХГіЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎШмвКn(Na+)МѕаЁЃЌгаO2ЗХГі
6ЃЎШЁЖдЫЎеєЦјЕФЯрЖдУмЖШЮЊ0.4ЕФCOКЭH2зщГЩЕФЛьКЯЦјЬхШєИЩПЫЃЌЭЈШыЕНЪЂзуСПЕФNa2O2ЙЬЬхЗлФЉЕФШнЦїжаЃЌВЂЭЌЪБМгШыЩйСПЕФO2ЃЌЕчЛ№ЛЈв§ШМЃЌГфЗжЗДгІКѓЃЌГЦжиЗЂЯжЙЬЬхЗлФЉЕФжЪСПдіМгСЫ2.1gЃЌдђдЛьКЯЦјЬхЕФжЪСПБШЮЊ
AЃЎ1ЃК4ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ2ЃК3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎ6ЃК5ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ7ЃК2
5ЃЎаэЖрЗЧН№ЪєбѕЛЏЮядквЛЖЈЬѕМўЯТФмгыNa2O2ЗДгІЃЌЧвЗДгІМЋгаЙцТЩЁЃШчЃКNa2O2+SO2 == Na2SO4ЁЂ2Na2O2+2SO3 ==2Na2SO4+ O2ЃЌОнДЫЃЌФуШЯЮЊЯТСаЗНГЬЪНжаВЛе§ШЗЕФЪЧ
AЃЎ2Na2O2+2Mn2O7==4NaMnO4+O2ЁќЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ2Na2O2+P2O3==Na4P2O7
ЁЁ ЁЁCЃЎ2Na2O2+2 N2O3==4NaNO2+O2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁ DЃЎ2 Na2O2+2 N2O5 ==4NaNO3+O2Ёќ
4ЃЎНЋ4.34 g NaЁЂNa2OЁЂNa2O2ЕФЛьКЯЮягызуСПЕФЫЎЗДгІЃЌдкБъзМзДПіЯТЕУЕН672mlЛьКЯЦјЬхЃЌНЋЛьКЯЦјЬхЭЈЕчКѓЧЁКУЭъШЋЗДгІЃЌдђNaЁЂNa2OЁЂNa2O2ЕФЮяжЪЕФСПжЎБШЮЊ
AЃЎ4ЁУ3ЁУ2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ1ЁУ2ЁУ1ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎ1ЁУ1ЁУ2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ1ЁУ1ЁУ1
3ЃЎНЋФЦЁЂУОЁЂТСИї0.3molЗжБ№ЗХШы100 mL1 molЁЄL-1бЮЫсжаЃЌЭЌЮТЭЌбЙЯТВњЩњЕФЦјЬхЕФЬхЛ§БШЪЧ
AЃЎ1 : 2 : 3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ6 : 3 : 2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎ3 : 1 : 1ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ1 : 1 : 1
2ЃЎЯТСаИїзщЮяжЪЯрЛЅЛьКЯЗДгІЃЌМШгаЦјЬхЩњГЩЃЌзюжегжгаГСЕэЩњГЩЕФЪЧ
ЂйН№ЪєФЦЭЖШыЕНFeCl3ШмвКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЂкЙ§СПNaOHШмвККЭУїЗЏШмвК
ЂлЩйСПЕчЪЏЭЖШыЙ§СПNaHCO3ШмвКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЂмNa2O2ЭЖШыFeCl2ШмвК
AЃЎЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂкЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂйЂлЂм
1ЃЎЯТСагаЙиФЦЕФа№ЪіжаЃЌДэЮѓЕФЪЧ
AЃЎФЦЕФЛЙдадКмЧПЃЌПЩвдгУРДвБСЖН№ЪєюбЁЂяЏЁЂюъЕШ
BЃЎФЦЕФЛЏбЇаджЪЗЧГЃЛюЦУЃЌФЦдЊЫижЛФмвдЛЏКЯЬЌДцдкгкздШЛНч
CЃЎдкФЦЁЂМиЁЂяЈШ§жжЕЅжЪжаЃЌяЈЕФШлЕузюИп
DЃЎФЦЕФжЪЕиШэЃЌПЩгУаЁЕЖЧаИю
15ЃЎ(12Зж)дкБъзМзДПіЯТЃЌШЁМзЁЂввЁЂБћИї30.0mLЯрЭЌХЈЖШЕФбЮЫсЃЌШЛКѓЗжБ№Т§Т§МгШызщГЩЯрЭЌЕФУОТСКЯН№ЗлФЉЃЌЕУЯТБэжагаЙиЪ§Он(ЩшЗДгІЧАКѓШмвКЬхЛ§ВЛЗЂЩњБфЛЏ)ЃК
|
ЪЕбщађКХ |
Мз |
вв |
Бћ |
|
КЯН№жЪСП/mg |
255 |
385 |
459 |
|
ЦјЬхЬхЛ§/ mL |
280 |
336 |
336 |
ЧыЛиД№ЃК
(1)МззщЪЕбщжаЃЌбЮЫс(бЁЬюЁАЙ§СПЁБЁАЪЪСПЁБЛђЁАВЛзуСПЁБЃЌЯТЭЌ)ЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛБћзщЪЕбщжабЮЫсЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)бЮЫсЕФЮяжЪЕФСПХЈЖШЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)КЯН№жаMgЁЂAlЕФЮяжЪЕФСПжЎБШЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
14ЃЎ(12Зж)Н№ЪєУОКЭУОКЯН№дкКНПеЁЂЦћГЕжЦдьКЭЕчзгЙЄвЕЕШСьгђОпгаЙуЗКЕФгУЭОЃЌН№ЪєУОЕФвБСЖгаЖржжЗНЗЈЃЌЦфжажЎвЛЮЊЦЄНЗЈЁЃИУЗНЗЈЪЧвдАздЦЪЏ(CaCO3•MgCO3ЮЊдСЯЃЌОИпЮТьбЩеЩњГЩбѕЛЏЮя(CaO•MgO)ЃЌбѕЛЏЮядкЛЙдТЏжаО1200ЁцецПеЬѕМўЯТгУЙшЬњЛЙдЩњГЩУОеєЦћ(ЬњдкЗДгІЧАКѓЛЏКЯМлВЛБф)ЃЌУОеєЦћОРфФ§ЦїРфОлЮЊДжУОЃЌДжУОдйООЋСЖЁЂж§ЖЇЕУЕНГЩЦЗН№ЪєУОЁЃЗДгІЙЄвеСїГЬШчЯТЭМЃК
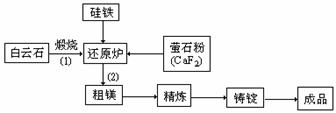
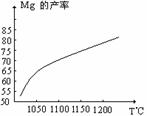
(1)дквБСЖЙ§ГЬжаЗДгІЮТЖШЖдЩњГЩН№ЪєУОЕФгА
ЯьШчЭМЃЌДгЭМжаЗжЮіЃЌЛЙдЗДгІЕФЗДгІШШ
ЁїH ЁЁЁЁЁЁ0(ЬюЁА<ЁБЁА>ЁБЁА=ЁБ)ЃЛРэгЩЪЧЃК
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(2)ЛЙдТЏжаашвЊдк1200ЁцецПеЬѕМўЯТЗДгІЃЌЗДгІДяЕНЦНКтЪБЕФЮТЖШгыбЙЧПЕФЙиЯЕШчЯТ
|
ЪЃгрбЙЧПmmHg |
760 |
10 |
1 |
0.1 |
|
ЦНКтЪБЕФЮТЖШЁц |
2370 |
1700 |
1430 |
1235 |
ецПеЬѕМўЖджЦБИН№ЪєУОРДНВЃЌПЩвдДяЕНЕФФПЕФЪЧЃК
ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3)КЌУОПѓЮяГЃМћЕФгаСтУОПѓ(MgCO3)ЁЂАздЦЪЏКЭЙтТБЪЏ(KCl••MgCl2• 6H2O)ЃЌЦфжа
KCl••MgCl2• 6H2OЪєгкЁЁЁЁЁЁЁЁЁЁ ЁЃ
AЃЎИДбЮЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЛьКЯЮяЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎХфКЯЮяЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЛьбЮ
(4)аДГіЯТСаЗДгІЕФЗНГЬЪН
ЂйьбЩеАздЦЪЏЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂкCaO•MgOгыSiЕФЗДгІЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
13ЃЎ(14Зж)ФГЛЏбЇаЫШЄаЁзщгУКЌгаТСЁЂЬњЁЂЭЕФКЯН№жЦШЁДПОЛЕФТШЛЏТСШмвКЁЂТЬЗЏОЇЬх(FeSO4ЁЄ7H2O)КЭЕЈЗЏОЇЬх(CuSO4ЁЄ5H2O)ЃЌвдЬНЫїЙЄвЕЗЯСЯЕФдйРћгУЁЃЦфЪЕбщЗНАИ
ШчЯТЃК
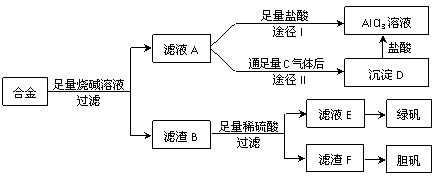

ЪдЛиД№ЯТСаЮЪЬтЃК
(1)Й§ТЫгУЕФВЃСЇвЧЦїгаЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)аДГіТЫвКAзЊЛЏЮЊГСЕэDЕФРызгЗНГЬЪНЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(3)гЩТЫвКAжЦAlCl3ШмвКЕФЭООЖгаЂёКЭЂђСНЬѕЃЌФуШЯЮЊКЯРэЕФЪЧЭООЖЁЁЁЁЁЁ (ЬюЁАЂёЁБЛђЁАЂђЁБ)ЃЌРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ДгТЫвКEжаЕУЕНТЬЗЏОЇЬхЕФЪЕбщВйзїЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(5)H2O2ЪЧвЛжжТЬЩЋбѕЛЏМСЃЌгІгУЪЎЗжЙуЗКЃЌдкТЫдќFжаМгШыЯЁСђЫсКЭH2O2РДжЦБИЕЈЗЏОЇЬхЪЧвЛжжТЬЩЋЙЄвеЃЌИУЗДгІЕФзмЛЏбЇЗНГЬЪНЮЊЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(6)гаЭЌбЇЬсГіПЩНЋЗНАИжазюГѕШмНтКЯН№ЕФЩеМюИФгУбЮЫсЃЌжиаТЩшМЦЗНАИЃЌвВФмжЦЕУШ§жжЮяжЪЃЌФуШЯЮЊКѓепЕФЗНАИЪЧЗёИќКЯРэЃПЁЁЁЁЁЁЁЁ ЃЛРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com