
题目列表(包括答案和解析)
7.铜有两种天然同位素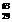 Cu 和
Cu 和 Cu,已知铜的近似相对原子质量为63.5,估算
Cu,已知铜的近似相对原子质量为63.5,估算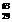 Cu的
Cu的
原子百分含量为:
A.20% B.25% C.50% D.75%
6.在水溶液中,,YO3n-和S2-发生如下反应:YO3n– +3S2– +6H+ = Y– +3S↓+ 3H2O,则YO3n-中Y元素的化合价和原子最外层电子数分别为
A.+4、6 B.+7、7 C.+5、5 D.+5、7
5.A、B、C三种短周期元素,原子序数按A、B、C依次增大,A元素原子最外层电子数是次外层电子数的2倍,B元素原子的次外层电子数是最外电子数的2倍,C元素原子的最外层电子数是内层电子总数的一半。则下列说法中正确的是
A.A元素的气态氢化物都是含极性键的非极性分子
B.由B元素的单质分子形成的晶体熔沸点较高。
C.C元素可以组成不同的单质,它们互为同素异形体。
D.A、B、C的氧化物都能溶于水形成酸
4.下列分子中,每个原子最外层均满足8电子稳定结构的是
A.NO2 B.SF6 C.BeCl2 D.NCl3
3. 下列各项中表达正确的是
下列各项中表达正确的是
A.S2-的结构示意图为: B.CO2的分子模型示意图:
B.CO2的分子模型示意图:
C.Na2S的电子式: D.N2的结构式: :N≡N:
D.N2的结构式: :N≡N:
2.核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学论断等高科技领域。已知只有质子数或中子数为奇数的原子核才有NMR现象。试判断下列哪组原子均可产生NMR现象
A.18O 、31P 、119Sn B.27Al 、19F 、12C
C.元素周期表中VA族所有元素的原子 D.元素周期表中第一周期所有元素的原子
1.2002年由德、法、美及波兰等多国科学家组成的科研小组合成了非常罕见的 Fe原子,有关
Fe原子,有关 Fe的说法正确的是
Fe的说法正确的是
A.它是一种新元素
B. Fe与
Fe与 Fe互为同素异形体
Fe互为同素异形体
C.它是一种新原子
D.这种铁原子发生衰变放出两个质子后变成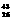 Fe
Fe
20.(6分)下表列有四种物质的沸点:
|
物质 |
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
|
沸点/℃ |
1465 |
1412 |
181(升华) |
57.6 |
(1)从表中的数据,结合学过的化学知识,你能得到的规律是
。
(2)以上四种物质中,属于共价化合物的是 。
(3)若你得到的规律具有普遍性,则以下两种物质的沸点高低是:LiCl BCl3。(填“>”、“==”、“<”)。
19.(10分)下表列出了前20号元素中的某些元素性质的有关数据:
|
|
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
|
原子半径(10-10m) |
1.52 |
2.27 |
0.74 |
1.43 |
0.77 |
1.10 |
0.99 |
1.86 |
0.75 |
0.71 |
|
最高价态 |
+1 |
+1 |
- |
+3 |
+4 |
+5 |
+7 |
+1 |
+5 |
- |
|
最低价态 |
- |
- |
-2 |
- |
-4 |
-3 |
-1 |
- |
-3 |
-1 |
试回答下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是 (写编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是 (写分子式)。某元素R的原子半径为1.02×10-10m,该元素在周期表中的位置是 ;电解⑧和R的熔融化合物时,当阴极消耗 2 mol 该化合物的正离子时,阳极可得3 mol单质,。由此可推断得知该盐的化学式是 (填化学式)。其阳极上所发生的电极方程式是: __________________________________________。
18.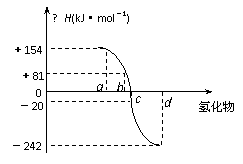 (6分)已知:在热力学标准态(298K、1.01×105Pa)下,由稳定的单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H)。右图为氧族元素氢化物a、b、c、d的生成热数据示意图。试回答下列问题:
(6分)已知:在热力学标准态(298K、1.01×105Pa)下,由稳定的单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H)。右图为氧族元素氢化物a、b、c、d的生成热数据示意图。试回答下列问题:
(1)写出氧族元素中含有18e-的两种氢化物的电子式 。
(2)请你归纳:非金属元素氢化物的稳定性与氢化物的反应热△H的关系
。
(3)写出硒化氢在热力学标准态下,发生分解反应的热化学反应方程式:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com