
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
4ЃЎвдЯТЖдЛЏбЇЪЕбщЕФУшЪіКЯРэЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎХфжЦвЛЖЈЮяжЪЕФСПХЈЖШЕФСђЫсШмвКЪБ,гІНЋСПШЁКУЕФХЈСђЫсЯШЗХШыЩеБжа,ШЛКѓМгЫЎЯЁЪЭЁЁ
BЃЎжаКЭЕЮЖЈЪЕбщЧАЃЌЫљЪЙгУЕФЕЮЖЈЙмКЭзЖаЮЦПБиаыЯДОЛЃЌВЂгУД§ВтвКШѓЯДЁЃ
CЃЎгУгкМьбщЦјЬхЕФЪджНвЛАуашЯШШѓЪЊЁЃ
DЃЎСђЫсЭОЇЬхНсОЇЫЎКЌСПЕФВтЖЈЪЕбщжаЃЌЪЂОЇЬхЕФлслізЦЩеКѓЃЌашЗХдкЪЏУоЭјЩЯРфШДКѓГЦСП
3ЃЎЯТСаЗНГЬЪНаДЗЈе§ШЗЕФЪЧ(ЁЁЁЁ )
AЃЎИпЮТьбЩеЪЏгЂКЭДПМюЛьКЯЮяЃКSiO2+ Na2CO3
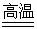 ЁЁNa2SiO3+ CO2Ёќ
ЁЁNa2SiO3+ CO2Ёќ
BЃЎЙ§СПSO2ЭЈШыЕНBa(NO3)2ШмвКжаЃК
3 SO2+2 NO3-+3 Ba2++2H2O = 3 BaSO4Ё§+2NO+4H+
CЃЎвЛЖЈСПЕФCl2ЭЈШыЕНFeBr2ШмвКжаЃКFeBr2+ Cl2 = FeCl2 + Br2
DЃЎН№ЪєNaЭЖШыЕНCuSO4ШмвКжаЃК2Na + Cu2+ = 2Na+ + Cu
2ЃЎNAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ )
AЃЎБъПіЯТЃЌ22.4LNO2гыЫЎЗДгІЃЌзЊвЦЕФЕчзгЪ§ЮЊNA
BЃЎГЃЮТЯТЃЌ78gNa2O2ЙЬЬхжавѕРызгЪ§ЮЊNA
CЃЎ3gН№ИеЪЏОЇЬхжаЃЌКЌгаЕФЙВМлМќЪ§ЮЊNA
DЃЎ25ЁцЪБЃЌpH=14ЕФBa(OH)2ШмвК1LЃЌBa2+Ъ§ЮЊNA
1ЃЎЫЎЪЧЩњУќжЎдДЃЌЯТСагаЙиЫЕЗЈжае§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁЁЁ AЃЎЫЋбѕЫЎБЛГЦЮЊТЬЩЋбѕЛЏМСЃЌЪЧвђЮЊЦфЛЙдВњЮяЮЊO2ЃЌЖдЛЗОГУЛгаЮлШО
BЃЎЭѕЫЎЪЧХЈбЮЫсКЭХЈЯѕЫсАДЬхЛ§БШ1ЃК3ХфГЩЕФЛьКЯЮяЃЌПЩвдШмНтAuЁЂPt
CЃЎАБЫЎФмЕМЕчЃЌЫЕУїАБЦјЪЧЕчНтжЪ
DЃЎаТжЦБИЕФТШЫЎжаДцдкШ§жжЗжзгЃЌЫФжжРызг
12ЁЂ(1)CH3CHЃНCH2(2Зж)ЁЁ 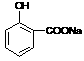 (3Зж)
(3Зж)
(2)ЂйЂкЂн(2Зж)ЁЁ (3)6(2Зж)
(4)2 CH3CH(OH)CH3+O2
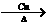 2CH3COCH3+H2O (3Зж)
2CH3COCH3+H2O (3Зж)
CH3COCH3+2C6H5OH
 +H2O(3Зж)
+H2O(3Зж)
НтЮіЃКБШНЯXКЭBПЩжЊЃЌXЮЊБНЃЌBЮЊБНЗгЃЌCЮЊБНЗгФЦЃЌЭЈЙ§DЁЂCЗжзгЪНЕФВювьБШНЯПЩжЊDБШCЖрвЛИієШЛљЃЌОЫсЛЏЕУЕНЕФEЪЧЫЎбюЫсЁЃАбBADЫЎНтПЩВ№ГЩНЬг§ВЉПЭ2ЗжзгЕФ ЁЁ (E)КЭвЛ ЗжзгЕФ
ЁЁ (E)КЭвЛ ЗжзгЕФ (H )ЁЃBADЯћКФЧтбѕЛЏФЦЕФЖрЩйгЩДЫПЩжЊЁЃ
(H )ЁЃBADЯћКФЧтбѕЛЏФЦЕФЖрЩйгЩДЫПЩжЊЁЃ
HгЩBКЭGКЯГЩЃЌЙЪGЪЧШ§ИіЬМЕФгаЛњЮяЃЌYЪЧШ§ИіЬМЕФЬўЃЌЧвЦфПЩгыЫЎЗДгІЃЌПЩФмКЌгаВЛБЅКЭНсЙЙЃЌЙЪЭЦВтЦфЮЊБћЯЉ(CH3CHЃНCH2)ЁЃ
DЕФНсЙЙгаФбЖШЃЌвђЮЊЖўбѕЛЏЬМПЩвдЪЙЗгФЦБфГЩЗгєЧЛљЃЌЙЪЮЊ ЁЃНЬг§ВЉПЭ
ЁЃНЬг§ВЉПЭ
ПДЬѕМўПЩжЊFБЛДпЛЏбѕЛЏГЩGЃЌдйгЩHжаБНЛЗСЌдкЕкЖўИіЬМдзгЩЯЃЌжЊЙйФмЭХдкЕкЖўИіЬМдзгЩЯЁЃЙЪGЮЊБћЭЊЁЃGЁЂBКЯГЩHЕФЗДгІЮвУЧУЛгабЇЙ§ЃЌЕЋБШНЯдСЯНсЙЙКЭВњЮяНсЙЙЃЌДѓЕЈВТВтЪЧЖЯПЊЬМбѕЫЋМќКѓЬМдзгСЌНсСНИіБНЗгЗжзгЁЃ
9ЃЎ(1)NЁЁ ЕкШ§жмЦкIAзх(УППе2Зж)ЁЁ НЬг§ВЉПЭ (2)Na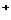 ЃлЁУOЁУOЁУЃн
ЃлЁУOЁУOЁУЃн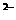 Na
Na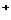 (2Зж)
(2Зж)
(3)3NaN3=Na3N+4N2Ёќ(3Зж)
(4)C2H2(g)+ O2(g)=2CO2(g) +H2O(
O2(g)=2CO2(g) +H2O(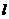 )ЃЛЁїH=Ѓ313.5 kJ/mol(3Зж)
)ЃЛЁїH=Ѓ313.5 kJ/mol(3Зж)
(5)Na2CO3ЛђNa2CO3КЭNaOH(3Зж)
НтЮіЃКBЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФ2БЖЃЌгІЮЊЬМЃЌгЩAЁЂBПЩзщГЩB2A2ЕФЛЏКЯЮяжаКЌгаЗЧМЋадМќПЩЭЦжЊB2A2ЪЧC2H2ЃЛAЁЂEЭЌжїзхЃЌЧвAЁЂBЁЂCЁЂDЁЂEдзгађЪ§вРДЮдіДѓЃЌПЩЭЦжЊEЪЧФЦЃЌAЁЂDЁЂEзщГЩЛЏКЯЮяA2D2ЃЌE2D2ПЩЭЦжЊA2D2ЪЧH2O2ЃЌE2D2ЪЧNa2O2ЃЌЙЪDЪЧбѕЃЌдђCЮЊЕЊЃЌЙЪEC3ЪЧNaN3ЁЃ2 mol NaHCO3ЗжНтЕУЕН1 mol CO2КЭ1 molЫЎеєЦјЃЌгЩгкCO2КЭH2OЖМПЩгыNa2O2ЗДгІЩњГЩO2ЃЌЙЪ150ЁцЪБЫљЕУЕФНЬг§ВЉПЭ2жжЦјЬхжавЛЖЈКЌгаO2ЃЌгжвђЮЊCO2КЭH2OгыNa2O2ЗДгІЪБЃЌПЩПДзїЪЧCO2ЯШЗДгІЃЌЙЪСэвЛжжЦјЬхБиЮЊЫЎеєЦјЁЃДЫЪБЃЌгІгаСНжжПЩФмЃЌвЛЪЧNa2O2ЧЁКУгыCO2ЗДгІЃЌЖўЪЧЫЎеєЦјжЛгаВПЗжгыNa2O2ЗДгІЃЌЙЪЗДгІКѓЙЬЬхЪЧNa2CO3ЛђNa2CO3КЭNaOHЃЌвЛЖЈЮоNa2O2ЁЃ
|
10ЃК(1)O=C=OЁЁ (2)MOH+SO2=MHSO3(3)Fe2O3+3CO 2Fe+3CO2ЁЁ 3Fe2++4H++NO3-=3Fe3++NOЁќ+2H2OЁЁ
2Fe+3CO2ЁЁ 3Fe2++4H++NO3-=3Fe3++NOЁќ+2H2OЁЁ
(4)Al3++4OH-=AlO2-+2H2OЁЁ Al3++3AlO2-+6H2O=4Al(OH)3Ё§(УППе2Зж) НЬг§ВЉПЭ
НтЮіЃКБОЬтПђЭМЬиЕуЪЧЃЌAгыEЗДгІЃЌЯрЖдСПВЛЭЌВњЮяВЛЭЌЃЛЧвВњЮяжЎМфПЩвдЯрЛЅзЊЛЏЃЌЗћКЯЬѕМўЕФAЁЂBЁЂDБиаыОпгаЁАШ§НЧЁБзЊЛЏЙиЯЕЁЃ (1)вРЬтвтЃЌBЮЊМЋадМќаЮГЩЕФЗЧМЋадЗжзгЃЌжабЇГЃМћЕФЮяжЪгаЖўбѕЛЏЬМЁЂЖўСђЛЏЬМЁЂЫФТШЛЏЬМЁЂМзЭщЕШЃЌЖјAЁЂEЮЊЕЅжЪЃЌГЃМћЕФЮяжЪжажЛгаЬМКЭбѕЦјЃЌбѕЦјЙ§СПЩњГЩЖўбѕЛЏЬМЃЌбѕЦјВЛзуЩњГЩвЛбѕЛЏЬМЁЃЖўбѕЛЏЬМЪЧгЩМЋадМќаЮГЩЕФЗЧМЋадЗжзгЁЃЫљвдЃЌAЮЊЬМЃЌBЮЊЖўбѕЛЏЬМЃЌDЮЊвЛбѕЛЏЬМЃЌEЮЊбѕЦјЁЃНЬг§ВЉПЭ
(2)вРЬтвтЃЌEЮЊSO2ЃЌгУЧПМюMOHзїЮЊЛЏбЇЪНаДЛЏбЇЗНГЬЪНЃЌMПЩФмЪЧФЦЃЌМиЃЌяЈЃЌяЄЁЃ
ЁЁ(3)вРЬтвтЃЌBжаКЌгаFe2+,ЕЮМгбЮЫсЃЌFe2+зЊЛЏГЩFe3+,ЫЕУїШмвКжаКЌгаNO3-ЃЌМДAЮЊЯѕЫсЃЌEЮЊЬњЃЌBЮЊЯѕЫсбЧЬњЃЌDЮЊЯѕЫсЬњЁЃЯѕЫсЬњжаКЌЩйСПЯѕЫсбЧЬњЃЌПЩвдЕЮМгЯЁЯѕЫсГ§ШЅЃЌЛЏбЇЗНГЬЪНЮЊ3Fe(NO3)2+4HNO3=3Fe(NO3)3+NOЁќ+2H2OЃЌГ§дгжЪВЛФмв§ШыаТдгжЪЁЃНЬг§ВЉПЭ
(4)вРЬтвтЃЌAЮЊТШЛЏТСЃЌBЮЊЦЋТСЫсбЮЃЌDЮЊЧтбѕЛЏТСЁЃНЬг§ВЉПЭ
10 (1)BCA(6Зж)НЬг§ВЉПЭ
ЁЁЁЁ (2)Ђй2Na+2CO2 CO+Na2CO3Ђк4Na+3CO2
CO+Na2CO3Ђк4Na+3CO2 2Na2CO3+C(6Зж)НЬг§ВЉПЭ
2Na2CO3+C(6Зж)НЬг§ВЉПЭ
ЁЁЁЁ (3)НЋВаСєЮяШмгкЪЪСПЫЎЃЌШєгаКкЩЋВЛШмЮядђжЄУїВаСєЮяжагаCЃЌдкШмвКжаМгзуСПBaCl2ШмвКЃЌШЛКѓЙ§ТЫЃЌдкТЫвКжаЕЮМгМИЕЮЗгЬЊЃЌШєШмвКБфКьЃЌдђжЄУїВаСєЮяжаКЌгаNa2OЁЃ(4Зж)
НтЮіЃК (1) ЬМЫсЧтФЦЗжНтжЦЖўбѕЛЏЬМЕФзАжУЪЧЪЙгУЁБЙЬЬх+ЙЬЬхЁБМгШШзАжУ,МДбЁBЃЛ
ПщзДЪЏЛвЪЏгыЯЁбЮЫсЗДгІЃЌВЛФмбЁA ЃЌНЬг§ВЉПЭAзАжУВЛЪЪгУгкПщзДЙЬЬхгывКЬхЗДгІЃЌМДбЁCЃЛЗлФЉзДЬМЫсФЦЙЬЬхгыЯЁСђЫсЗДгІПЩбЁAЁЃ(2)ЂйзАжУ6НЬг§ВЉПЭжагаКкЩЋГСЕэЃЌвРЬтжааХЯЂжЊВњЩњСЫCOЃЌВаСєЮягыHClзїгУВњЩњCO2ЃЌдђВаСєЮяжаКЌNa2CO3ЁЃЂкВаСєЮягыHClзїгУВњЩњCO2ЃЌжЄУїВаСєЮяжаКЌNa2CO3ЃЌЖјгжЮоCOВњЩњЃЌИљОнбѕЛЏЛЙдЗДгІЙцТЩжЊЃЌФЦБЛбѕЛЏЃЌдђБигадЊЫиБЛЛЙдЃЌСЊЯЕВаСєЙЬЬхжагаСНжжЮяжЪЙЪжЊгаCЩњГЩЁЃНЬг§ВЉПЭ (3)ИљОнЬМВЛШмгкЫЎЃЌПЩжЄУїжЎЃЌИљОнNa2O+H2O 2NaOHШмвКЯдМюадПЩжЄУїNa2OДцдкЃЌЕЋNa2CO3ШмвКвВЯдМюадЃЌЖдЪЕбщгаИЩШХЃЌЙЪЯШНЋ
2NaOHШмвКЯдМюадПЩжЄУїNa2OДцдкЃЌЕЋNa2CO3ШмвКвВЯдМюадЃЌЖдЪЕбщгаИЩШХЃЌЙЪЯШНЋ гУBa2+ГСЕэЁЃНЬг§ВЉПЭ
гУBa2+ГСЕэЁЃНЬг§ВЉПЭ
8ЃЎDЁЁ NaYШмвКЕФpH = 9ЃЌЫЕУїHXЪЧШѕЫсЃЌc(OHЃ)ЃН10Ѓ5 molЁЄLЃ1 ЃЌЧвЖМЪЧгЩЫЎЕчРыВњЩњЕФЃЌAбЁЯюДэЮѓЃЛXЃЛсЫЎНтЃЌЫљвдРызгХЈЖШЕФДѓаЁЮЊЃКc(Na+) >c(YЃ)> c(OHЃ)>c(H+)ЃЌBбЁЯюДэЮѓЃЛвђЮЊЪЧЕШЬхЛ§ЛьКЯЃЌc(Na+)МѕАыЃЌМДЮЊ0.15molЁЄLЃ1ЃЌдђc(Na+)ЃНc(X¯)+c(HX) ЃН0.15molЁЄLЃ1ЃЌCбЁЯюДэЮѓЃЛИљОнжЪзгЪиКугаЃКc(OHЃ)Ѓc(HY)ЃНc(H+)ЃЌc(H+)ЃН1ЁС10Ѓ9molЁЄLЃ1ЃЌDбЁЯюе§ШЗЁЃНЬг§ВЉПЭ
10.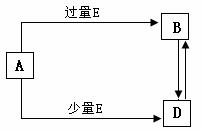 (15Зж)вбжЊAЁЂBЁЂDЁЂEОљЮЊжабЇЛЏбЇГЃМћЕЅжЪМАЛЏКЯЮяЃЌЫќУЧжЎМфЕФзЊЛЏЙиЯЕШчЭМЫљЪО(ВПЗжВњЮяТдШЅ)ЁЃ
(15Зж)вбжЊAЁЂBЁЂDЁЂEОљЮЊжабЇЛЏбЇГЃМћЕЅжЪМАЛЏКЯЮяЃЌЫќУЧжЎМфЕФзЊЛЏЙиЯЕШчЭМЫљЪО(ВПЗжВњЮяТдШЅ)ЁЃ
(1)ШєAКЭEОљЮЊЕЅжЪЧвBЮяжЪЮЊМЋадМќаЮГЩЕФЗЧМЋадЗжзгЁЃBЕФНсЙЙЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃНЬг§ВЉПЭ
(2)ШєAЮЊПЩШмадЧПМю(MOH)ЃЌEЮЊЭЌжїзхдЊЫиаЮГЩЕФГЃМћЗЧН№ЪєЛЏКЯЮяЃЌЧвИУЛЏКЯЮяжаСНжждЊЫиЕФжЪСПБШЮЊ1ЃК1ЃЌЪдаДГіAЕНBЕФЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁ ЁЃНЬг§ВЉПЭ
(3)ШєШЁBЕФШмвКзАгкЪдЙмЃЌЯђШмвКжаЕЮМгKSCNШмвКЃЌЮоЯжЯѓНЬг§ВЉПЭЃЌдйЕЮМгЯЁбЮЫсЃЌВњЩњКьЩЋШмвКЃЌдђгУЛЏбЇЗНГЬЪНБэЪОЙЄвЕжЦБИEЛЏбЇдРэЃКЁЁЁЁЁЁЁЁЁЁ НЬг§ВЉПЭЃЛDЕФШмвКжаКЌгаЩйСПBЃЌгУРызгЗНГЬЪНБэЪОГ§дгЗНЗЈЃКЁЁЁЁЁЁ ЁЃ
(4)ШєAгЩЭЌвЛЖЬжмЦкЕФСНжждЊЫизщГЩЃЌDЮЊАзЩЋГСЕэЃЌЧвAЁЂBШмвКЛьКЯЩњГЩDЃЌЪдаДГіAЕНBЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁ ЃЛAЁЂBШмвКЛьКЯЩњГЩDЕФРызгЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃ
11 (16Зж) ФГаЫШЄаЁзщЕФбЇЩњИљОнMgгыCO2ЗДгІдРэЃЌЭЦВтФЦвВгІФмдкCO2жаШМЩеЁЃЮЊСЫШЗЖЈЦфЩњГЩВњЮяВЂНјааЪЕбщТлжЄЃЌЧыФуВЮгывдЯТбаОПЙ§ГЬЁЃ
(1)МзЭЌбЇЪзЯШЩшМЦСЫЪЕбщЪвжЦШЁЖўбѕЛЏЬМЕФШ§жжЗЂЩњзАжУЃЌНЬг§ВЉПЭШєбЁгУЬМЫсЧтФЦЗжНтжЦЖўбѕЛЏЬМгІбЁгУзАжУЪЧ_______(ЬюзАжУађКХЁАAЁБЁАBЁБЛђЁАCЁБЃЌЯТЭЌ)ЃЛНЬг§ВЉПЭШєгУЪЏЛвЪЏгыЯЁбЮЫсЮЊдСЯЃЌВЂФмПижЦЗДгІЫцЪБЗЂЩњЫцЪБЭЃжЙЃЌзюКУгІбЁгУЕФзАжУЪЧ_______ЃЛНЬг§ВЉПЭШєгУЬМЫсФЦЙЬЬхгыЯЁСђЫсЗДгІгІбЁгУЕФзАжУЪЧ_______ЁЃНЬг§ВЉПЭ
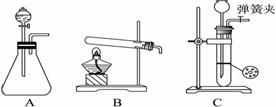
(2)ввЭЌбЇАДЪЕбщвЊЧѓЃЌгУЯТСазАжУНјааЪЕбщ(вбжЊPdCl2ШмвКФмБЛCOЛЙдЕУЕНКкЩЋЕФPd)ЃЌЧыЭъГЩЯТСаЮЪЬтЃК

ЁЁЁЁ ЂйШєзАжУ6жагаКкЩЋГСЕэЃЌзАжУ4жаЕФВаСєЙЬЬх(жЛгавЛжжЮяжЪ)НЬг§ВЉПЭМгбЮЫсгаФмЪЙЪЏЛвЫЎБфЛызЧЕФЦјЬхЗХГіЃЌдђФЦгыЖўбѕЛЏЬМЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК_____________________ЁЃНЬг§ВЉПЭ
ЁЁЁЁ ЂкШєзАжУ6жаШмвКЮоУїЯдЯжЯѓЃЌзАжУ4жаВаСєЙЬЬх(гаСНжжЮяжЪ)МгбЮЫсгаФмЪЙЪЏЛвЫЎБфЛызЧЕФЦјЬхЗХГіЃЌдђФЦгыЖўбѕЛЏЬМЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК_____________________ЁЃНЬг§ВЉПЭ
(3)жИЕМРЯЪІШЯЮЊЃЌВЛНівЊМьбщВаСєЙЬЬхжаЪЧЗёгаЬМЫсФЦЛЙвЊМьбщЦфжаЪЧЗёгабѕЛЏФЦКЭЬМЃЌЕБШЗШЯФЦГфЗжЗДгІКѓЃЌЧыФуЩшМЦвЛИіМђЕЅЪЕбщЃЌбщжЄзАжУ4жаЕУЕНЕФВаСєЙЬЬхжаЪЧЗёКЌгаNa2OКЭCЁЃ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
12 (15Зж)РћгУЗМЯуЬўXКЭСДЬўYПЩвдКЯГЩзЯЭтЯпЮќЪеМСBADЃЌBADЕФНсЙЙМђЪНЮЊЃК

BADЕФКЯГЩТЗЯпШчЯТ(вбжЊGВЛФмЗЂЩњвјОЕЗДгІ)ЃКНЬг§ВЉПЭ
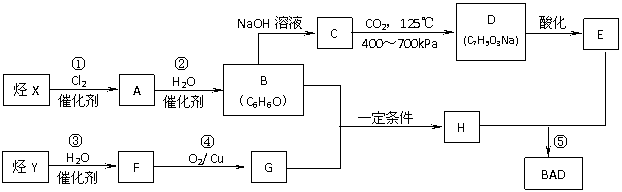
НЬг§ВЉПЭ
ЪдЛиД№ЯТСаЮЪЬтЃК
(1)аДГіНсЙЙМђЪНЃКY_________________ЃЛD______________________ЁЃ
(2)ЪєгкШЁДњЗДгІЕФга_______________________(ЬюЪ§зжађКХ)ЁЃНЬг§ВЉПЭ
(3)1 mol BADзюЖрПЩгыКЌ__________mol NaOHЕФШмвКЭъШЋЗДгІЁЃНЬг§ВЉПЭ
(4)аДГіЯТСаЗДгІЕФЛЏбЇЗНГЬЪНЃК
ЗДгІЂмЃКЁЁЁЁЁЁЁЁ ________________________________ЁЁЁЁЁЁЁЁЁЁ ЃЛ
B+GЁњ HЃКЁЁЁЁЁЁ ________________________________ ЁЁЁЁЁЁЁЁЁЁ ЁЃ
НЬг§ВЉПЭ
Д№АИгыЬсЪО
1-5 DBDDDНЬг§ВЉПЭ
6ЁЁ DЁЁ AЯюжаЭтЕчТЗЕФЕчзгСїЯђЮЊЃКНЬг§ВЉПЭXЁњЭтЕчТЗЁњYЃЌНЬг§ВЉПЭЕчСїЗНЯђгыЦфЯрЗДЃЛXМЋЪЇЕчзгЃЌЪЧИКМЋЃЌY МЋЩЯЗЂЩњЕФЪЧЛЙдЗДгІЃЌНЬг§ВЉПЭX МЋЩЯЗЂЩњЕФЪЧбѕЛЏЗДгІЃЛШєСНЕчМЋЗжБ№ЮЊ Fe КЭЬМАєЃЌдђ YЮЊЬМАєЃЌ X ЮЊFeЃЌЙЪABCДэЮѓЃЌМДбЁDЁЃНЬг§ВЉПЭ
7ЁЁ D
9ЃЎ(14Зж)AЁЂBЁЂCЁЂDЁЂEЮхжжЖЬжмЦкдЊЫиЃЌдзгађЪ§вРДЮдіДѓЃЌЧвдзгКЫЭтзюЭтВуЕчзгЪ§ОљВЛГЌЙ§7ЁЃЦфжаAЁЂEЭЌжїзхЃЌНЬг§ВЉПЭBЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФ2БЖЃЛAЁЂBЁЂDЁЂEПЩзщГЩЛЏКЯЮяЁЃA2D2ЁЂB2A2ЁЂE2D2ЃЌНЬг§ВЉПЭЫќУЧЖМКЌгаЗЧМЋадЙВМлМќЁЃЧыЛиД№ЃКНЬг§ВЉПЭ
ЁЁ (1)CдЊЫиЗћКХЪЧЁЁЁЁЁЁ ЃЌEдЊЫидкжмЦкБэжаЮЛжУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃНЬг§ВЉПЭ
(2)аДГіE2D2ЕФЕчзгЪНЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(3)3 mol EC3ЪмзВЛїЩњГЩ4 mol C2ЦјЬхКЭвЛжжРызгЛЏКЯЮяЃЌПЩгУгкЦћГЕзїБЃЛЄЦјФвЃЌаДГіИУЗДгІЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃНЬг§ВЉПЭ
(4)вбжЊB2A2ЕФШМЩеШШЮЊ313.5 kJ/molЃЌаДГіИУЮяжЪШМЩеЕФШШЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЃНЬг§ВЉПЭ
(5)НЋ2 mol EABD3КЭвЛЖЈСПE2D2ЙЬЬхЛьКЯЃЌдкУмБеШнЦїжаМгШШНЬг§ВЉПЭЃЌЪЙЦфГфЗжЗДгІЃЌВтЕУ150ЁцЪБШнЦїжаНіКЌ2жжЦјЬхЃЌдђЗДгІКѓЙЬЬхЮяжЪЕФГЩЗжЪЧЁЁЁЁЁЁЁЁЁЁ ЁЃ
8ЃЎЪвЮТЯТЃЌШЁ0.3 molЁЄLЃ1HYШмвКгы0.3 molЁЄLЃ1NaOHШмвКЕШЬхЛ§ЛьКЯ(КіТдЛьКЯКѓШмвКЬхЛ§ЕФБфЛЏ)ЃЌВтЕУЛьКЯШмвКЕФpH = 9ЃЌдђЯТСаЫЕЗЈ(ЛђЙиЯЕЪН)е§ШЗЕФЪЧ
AЃЎЛьКЯШмвКжагЩЫЎЕчРыГіЕФc(OHЃ)ЃН10Ѓ9 molЁЄLЃ1ЁЁЁЁ ЁЁНЬг§ВЉПЭ
BЃЎШмвКжаРызгХЈЖШгЩДѓЕНаЁЕФЫГађЮЊ c(YЃ)> c(Na+) > c(OHЃ)>c(H+)
CЃЎc(Na+)ЃНc(Y¯)+c(HY) ЃН0.3 molЁЄLЃ1ЁЁ НЬг§ВЉПЭ
ЁЁDЃЎc(OHЃ)Ѓc(HY)ЃНc(H+)ЃН1ЁС10Ѓ9molЁЄLЃ1
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com