
题目列表(包括答案和解析)
14.(16分)
苯佐卡因是一种局部麻醉剂,可用于黏膜溃疡、创面及痔疮的镇痛,一般制成软膏或栓剂使用。其合成路线如图所示,其中有机物B具有酸性。
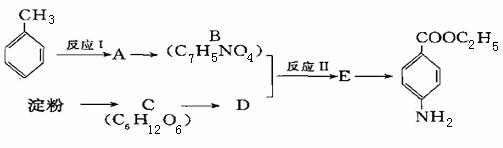
已知苯环上的取代有如下定位规律:当苯环上的碳原子连有甲基时,可在其邻位或对位上引入官能团;当苯环上的碳原子连有羧基时,可在其间位上引入官能团。
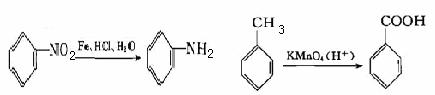
请写出:w.w.^w.k.&s.5*
(1)反应类型:反应Ⅰ ,反应Ⅱ 。
(2)化合物A、C的结构简式:A ,C 。
(3)下列转化的化学方程式
C→D: ;
B+D→E: 。
(4)苯佐卡因有多种同分异构体,其中-NH2直接连在苯环上,分子结构中含有--COOR
官能团,且苯环上一氯取代物只有两种的同分异构体共有六种,除苯佐卡因外,其中三种的结构简式是:

则剩余两种同分异构体的结构简式为 、 。
13.(20分)A、B、C、D、E、F是短周期元素,原子序数依次增大,A、D同主族,D、F同周期,C的最外层电子数与次外层电子数之和为8。B与C,D与F可以分别形成两种不同类型的晶体X和Y,其原子个数比分别为1:2和1:1。C、D、E可组成一种离子化合物Z,其阴阳离子的个数比为1:2,X与Z的水溶液反应可必得到白色沉淀W,将W加热分解后得到白色固体S,S的晶体类型与X和Y都不同。回答下列问题
(1)写出元素符号A ,D ,E ,F的原子结构示意图为 。w.w.^w.k.&s.5*
(2)X、Y、S的固态化合物存在三种不同的晶体类型,则三者中熔点最高的是 (填化学式,下同),在水中的溶解度最大的是 ,晶体中同时存在两种粒子(原子、分子、离子)间的相互作用力的是 ,Y与S晶体中中心原子的配位数(与该原子 距离最近的原子的数目)之比为 。
(3)将W经过一系列处理后可制得一种常用的高活性吸附材料M,M中的主要成分为S,常用于食品干燥、药物提纯、高级化妆品、高级涂料以及树脂生产或保存等,也是实验室中常用的干燥剂和吸湿剂,则M不可能具有的性质有
A.化学性质非常稳定 B.固态时为原子晶体 C.结构疏松多孔
D.能溶于强碱溶液 E.作干燥剂时可再生使用
(4)写出化学方程式:X+Z-W: ;请从中学阶段所学的反应中找出一个与此反应在本质上非常相似的反应,若反应物中都有X,请写出该反应的化学方程式 ,说明二者相似的原因 。
12.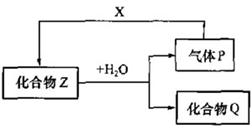 (15分)X、Z、P、Q四种物质相互转化关系如右图所示(图中部分反应物和生成物已略去),物质X与P之间的反应不在溶液中进行,通常状况下P为气体。
(15分)X、Z、P、Q四种物质相互转化关系如右图所示(图中部分反应物和生成物已略去),物质X与P之间的反应不在溶液中进行,通常状况下P为气体。
请回答下列问题:
(1)若X、P均为短周期元素的单质,P能使带火星的木条复燃,则X的原子结构示意图是 ,化合物Q的电子式为 。实验室制取气体P的化学方程式为:
(任写常用的一种)。
(2)若X为短周期元素的单质,P为化合物,X与P在常温下发生化合反应得到Z,则化合物Z是 ,写出化合物Q分解的化学方程式: 。
11.(16分)现有A、B、C、D四种短周期非金属元素,它们的主要化合价不止一种,但它们有一种相同的化合价,它们一些物理常数如下;
|
元素 |
A w.w.^w.k.&s.5* |
B |
C w.w.^w.k.&s.5* |
D |
|
原子半径/nm |
0.102 |
0.077 |
0.117 |
0.075 |
|
单质沸点/℃ |
444.6 |
4827 |
2355 |
-195.8 |
(1)B和D最高价氧化物水化物的酸性强弱是(用化学式表示)_________>___________
(2) 化学式是___________,是由____________(选填“极性”或“非极性”)键构成的_________(选填“极性”或“非极性”)分子。其分子空间构型是_________(选填“直线形”、“V型”、“三角锥形”或“正四面体”)。
化学式是___________,是由____________(选填“极性”或“非极性”)键构成的_________(选填“极性”或“非极性”)分子。其分子空间构型是_________(选填“直线形”、“V型”、“三角锥形”或“正四面体”)。
(3)D的氢化物与D的最高价氧化物水化物发生反应离子化学方程式______________。
(4)单质B与元素C的氧化物在一定条件下相互反应的化学方程式_______________。
(5)与D同主族的短周期元素E单质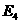 与氯气反应的物质的量之比为1:8,则它的总化学反应式是_________________________________________________。
与氯气反应的物质的量之比为1:8,则它的总化学反应式是_________________________________________________。
10、(15分) 下图是某同学检验铜与浓硫酸反应产物并推测铜与浓硫酸反应原理的实验图。
实验步骤如下:
①连接好装置, ;
②加入相应的试剂,加热试管A直到装置B中品红溶液完全褪色;
③熄灭酒精灯;
④将铜丝上提离开液面;
⑤用洗耳球从a管口向试管A中大量鼓气,以除尽A中的SO2气体;
⑥取出铜丝,浸入稀硫酸中,铜丝表面的黑色固体溶解,溶液变为蓝色;
⑦取出试管A底部的白色固体放人盛水的烧杯中,溶液变为蓝色。
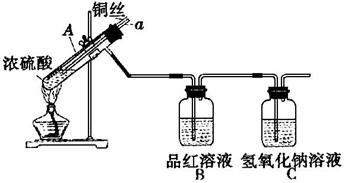
完成下列问题:
(1)完成操作步骤①: ; ,
(2)熄灭酒精灯后导管。的作用除了用于⑤中鼓空气外,还有一个重要作用是
;
(3)C的作用是 ;C中发生反应的离子方程式为 ;
(4)由上述操作过程与现象,可推测铜与浓硫酸反应原理为 ;
(用两个化学方程式填写)。
9、(13分)设X、Y、Z、W代表4种元素。已知:①X+和Y-两种离子具有相同的电子层结构;②Z元素原子核内质子数比Y元素原子核内质子数少9个;③Y和Z两元素可以形成四核41个电子的负一价阴离子;④W元素原子最外电子层上的电子数是其电子层数的2倍。据此填空:
(1)Y元素是 ,Z元素是 。
(2)由W、Z两元素所形成的含22个电子的化合物的电子式是 ;由X、Y、Z三元素所形成含68个电子的盐的化学式是 。
(3)W元素的单质中有一种分子W60,它可能最易发生的反应是 。
A. 消去反应 B. 取代反应 C. 加成反应 D. 聚合反应
(4)向X、Y、Z三种元素构成的化合物溶液中加入适量Z、W两种元素形成的化合物,可得一可使品红溶液褪色的物质,该反应的离子方程式为 。
8、(14分) 在一定条件下(不需添加另外的反应物),中学化学常见物质经不同的化学反应,可实现如下图的各种变化。其中,反应③④⑤属氧化还原反应,而反应①、②属非氧化还原反应。X、F和Y为单质,且F是空气的主要成份之一,其余为化合物。据此请填空:
 w.w.^w.k.&s.5*
w.w.^w.k.&s.5*
(1)物质A是 ,F是 ,Y是 。
(2)写出化合反应②的离子方程式: 。
写出反应⑤的离子方程式 。
(3)写出反应④的化学方程式,并注明反应条件: 。写出反应③Y和少量D的化学方程式: 。
7.(15分) A、B、C、D、E五种短周期元素,其中A、B、C属于同一周期元素,A元素的气态氢化物是一种广泛应用的优质气体燃料,B元素的氢化物是用途最广的溶剂。B元素可分别与A、C、D、E组成RB2型化合物。已知在DB2中,D与B的质量比为7:8;在EB2中,E与B的质量比为1:1。根据以上条件回答下列问题:
(1)写出C元素的名称 ;写出DB2的晶体类型 ;写出AB2的结构式 。
(2)熔点比较:B的氢化物 E的氢化物(选填“<”、“=”、“>’”),解释原因:
。
(3)C和D结合可生成一种超硬物质。本身具有润滑性,耐磨损,抗腐蚀,抗氧化,抗冷热。写出该物质的化学式 。
(4)B元素可分别与A、E形成多种阴离子。某溶液是由其中若干种阴离子组成的无机钠盐溶液,为了检验该溶液中的阴离子,分别取两份溶液进行如下实验:
①第一份溶液中加入足量盐酸溶液,只产生无色气体;
②第二份溶液中加入足量的BaCl2溶液,有白色沉淀产生,再加入足量的稀HNO3 ,白色沉淀质量减少。
由此得出的结论是 。
6.(16分)(湖北省八校第二次联考)A、B、C、D、E均为有机化合物,转化关系如下:
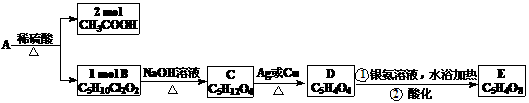
已知:同一个碳原子上不能同时连两个羟基。请回答:
(1)化合物A的分子式__________________
(2)B的结构简式_______________________
(3)写出A→B,C→D的有机反应类型:
A→B___________________反应 C→D________________反应
(4)B不能发生的反应是__________________
①氧化反应 ②取代反应 ③消去反应 ④水解反应 ⑤加聚反应
(5)写出D与足量的银氨溶液在一定条件下反应的方程式
____________________________________________________________ (6)分子式为C5H12O4的四元醇共有_______种。
5. (15分)
人体呼出气体中含有N2、O2、CO2、水蒸气等多种成分。某课外学习小组利用下图装置测定N2、O2、CO2的百分含量(忽略水蒸气等微量成分)。其中B是带刻度的量气装置。

试验步骤:
①先检验装置的气密性。在向装置中装入药品(如图所示),其中C瓶溶液上方为100mL已除尽CO2的空气(N2和O2的体积比为4/1)。
②打开止水夹b、c、d,关闭止水夹e,向B瓶中吹气后关闭d,并冷却到室温,收集到V1mL气体。
③关闭b,打开止水夹a、c、e、f,用打气筒向A瓶中缓缓充气,直到B中气体刚好全部排出,此时量筒中液面读数为V2mL。
④关闭e、f,降低燃烧匙的高度,用电火花引燃红磷。
⑤等C瓶冷却到室温,打开f1最终量筒液面读数为V3mL。
回答下列问题:
(1)A、B中装饱和NaHCO3而不能装饱和Na2CO3溶液的原因是
。
(2)C装置中红磷要过量的目的是 。
(3)反应结束后,C瓶溶液中含有溶质的化学式为
(4)利用上述数据计算人体呼出气体中氧气所占体积百分数为
CO2所占体积百分数为
(5)步骤⑤中C瓶还未冷却到室温就打开止水夹读数,这样会使所测氧气体积分数
(填“偏大”或“偏小”)。 w.w.^w.k.&s.5*
(6)严格按①-⑤进行试验后测得数据仍有一定误差,可能的原因是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com