
题目列表(包括答案和解析)
2.下列反应起了氮的固定作用的是
A.N2与H2在一定条件下反应生成NH3
B.NH3经催化氧化生成NO
C.NO与O2反应生成NO2
D.由NH3制碳铵和尿素
1.(2001年全国高考题)有一种磷的结构式是 有关它的下列
叙述中不正确的是
A.它完全燃烧时的产物是P2O5
B.它不溶于水
C.它在常温下呈固态
D.它与白磷互为同分异构体
44.8 L。现将此条件下V1 L SO2和O2的混合气体通过装有催化剂的反应器,充分反应后(假设反应完全)气体的体积为V2 L。所得气体用含a mol的NaOH溶液吸收,恰好完全反应。当产物分别为下列三种情况时,计算并推导a的表达式(用V1,V2表示)。
(1)Na2SO4
(2)Na2SO4和Na2SO3
16.(8分)(吉林省调研题)已知273℃,1.01×105 Pa时,1 mol气体所占的体积为
15.(6分)室温时,V L真空容器内通入n mol SO2和m mol H2S。
(1)若n=2,则当m等于多少时,反应后容器内气体的密度最小?
(2)若2n>m,则反应后氧化产物与还原产物的质量差为多少克?
(3)若5n=m,且反应后氧化产物与还原产物的质量和为48 g,则n+m的值是多少?
14.(6分)Na2SO3在空气中极易被氧化,现有a g样品,将其溶解后,
加入足量BaCl2溶液,可得干燥的沉淀b g。
(1)若Na2SO3未被氧化,b= a。
(2)若Na2SO3全部被氧化,b= a。
(3)若Na2SO3部分被氧化,b与a的关系式为 。
13.(12分)实验室制取SO2的反应原理为:Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
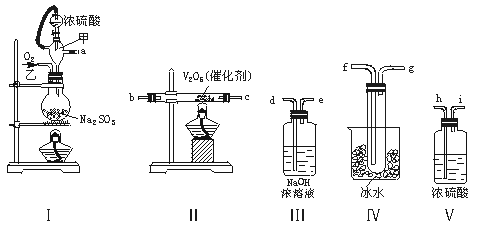
(1)这些装置的连接顺序(按气体左右的方向)是 → → → →
→ → → (填各接口的编号)。
(2)实验时甲仪器的作用与原理是 。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是 。
(4)Ⅳ处观察到的现象是 。
(5)在Ⅰ处用大火加热烧瓶时,SO2的转化率会 (填“增大”“不变”或“减小”)。
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重m g,则本实验中SO2的转化率为 。
12.(8分)A和B在常温下都是气体,A和B在空气中都不能被点燃,A的式量比B大。现分步实验如下:在A溶液中通入适量B气体,溶液酸性显著增强;继续加硝酸钡溶液反应,得到一种不溶于稀硝酸的白色沉淀;过滤,滤液无色;再向滤液中加入硝酸银溶液,析出另一种不溶于稀硝酸的白色沉淀。回答下列问题:
(1)写出A、B两种气体的名称:A ,B 。
(2)写出上述各步实验中的化学方程式,属离子反应的写离子方程式: 。
11.(10分)将SO2通入下列溶液中:
①氢硫酸,②溴水,③品红溶液,④澄清石灰水,⑤酸性高锰酸钾,⑥氯化钙溶液,
⑦用硝酸酸化的硝酸钡溶液,⑧硝酸钡
(1)使溶液颜色褪去的有 。
(2)先生成沉淀而后能溶解的有 。
(3)有沉淀产生不能溶解的有 。
(4)SO2作还原剂的有 。
(5)SO2作氧化剂的有 。
(6)无明显现象的有 。
10.一定物质的量的SO2与NaOH溶液反应,所得产物中含Na2SO3和NaHSO3物质的量之比为3∶5,则参加反应的SO2与NaOH物质的量之比为
A.1∶2 B.3∶5
C.8∶11 D.18∶8
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com