
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
1.(ЩЯКЃИпПМЬт)Й§бѕЛЏЧтЕФЗаЕуБШЫЎИпЃЌЕЋЪмШШШнвзЗжНтЁЃФГЪдМСГЇЯШжЦЕУ7%~8%ЕФЙ§бѕЛЏЧтШмвКЃЌдйХЈЫѕГЩ30%ШмвКЪБЃЌПЩВЩгУЕФЪЪвЫЗНЗЈЪЧ
A.ГЃбЙеєСѓЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.МѕбЙеєСѓЁЁ
C.МгЩњЪЏЛвГЃбЙеєСѓЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.МгбЙеєСѓ
31ЃЎ[гаЛњЛЏбЇЛљДЁ]
гУЗМЯуЬўAЮЊдСЯКЯГЩGЕФТЗЯпШчЯТЃК
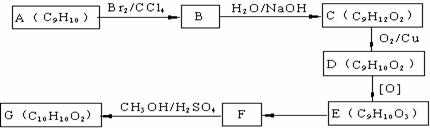
ЦфжаDЗжзгБНЛЗЩЯжЛгавЛИіжЇСДЃЌИУЗжзгдкЙтееЬѕМўЯТгыCl2 ЗЂЩњШЁДњЗДгІЩњГЩЕФвЛТШДњЮяжЛгавЛжжЃЌDгыаТжЦБИЕФCu(OH)2 аќзЧвКЗДгІЩњГЩКьЩЋГСЕэЁЃ
(1) ЛЏКЯЮя DЕФНсЙЙМђЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЛЏКЯЮяEжаЕФЙйФмЭХгаЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюУћГЦ)ЃЛ
(2)BЁњCЕФЗДгІРраЭЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЃЌDЁњEЕФЗДгІРраЭЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЃЌ
CЁњDЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
FЁњGЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
(3) аДГіЗћКЯЯТСаЬѕМўЕФFЕФЭЌЗжвьЙЙЬхЕФНсЙЙМђЪН ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
ЁЁЂЁЃЎЗжзгФкКЌБНЛЗЃЌЧвБНЛЗЩЯжЛгавЛИіжЇСДЃЛ
ЁЁЁЁ ЂЂЃЎвЛЖЈЬѕМўЯТЃЌ1 molИУЮяжЪгызуСПвјАБШмвКГфЗжЗДгІЃЌЩњГЩ4 molвјЕЅжЪЁЃ
30ЃЎ[ЮяжЪНсЙЙгыаджЪ]AЁЂBЁЂCЁЂDЁЂEЁЂFЮЊдзгађЪ§вРДЮдіДѓЕФЖЬжмЦкжїзхдЊЫиЁЃ AЁЂFдзгЕФзюЭтВуЕчзгЪ§ОљЕШгкЦфжмЦкађЪ§ЃЌFдзгЕФЕчзгВуЪ§ЪЧAЕФ3БЖЃЛBдзгКЫЭтЕчзгЗжДІ3ИіВЛЭЌФмМЖЃЌЧвУПИіФмМЖЩЯХХВМЕФЕчзгЪ§ЯрЭЌЃЛAгыCаЮГЩЕФзюМђЕЅЗжзгЮЊШ§НЧзЖаЮЃЛDдзгpЙьЕРЩЯГЩЖдЕчзгЪ§ЕШгкЮДГЩЖдЕчзгЪ§ЃЛEдзгКЫЭтУПИідзгЙьЕРЩЯЕФЕчзгЖМвбГЩЖдЃЌEЕчИКадаЁгкFЁЃ
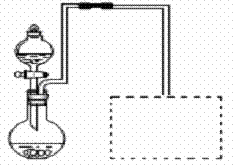
ЂХаДГіBЕФЛљЬЌдзгЕФКЫЭтЕчзгХХВМЪНЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂЦAЁЂCаЮГЩЕФзюМђЕЅЗжзгМЋвзШмгкЫЎЃЌЦфжївЊдвђЪЧЁЁЁЁЁЁЁЁЁЁЁЁ
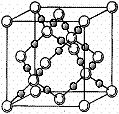 ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛгыИУзюМђЕЅЗжзгЛЅЮЊЕШЕчзгЬхЕФбєРызгЮЊЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛгыИУзюМђЕЅЗжзгЛЅЮЊЕШЕчзгЬхЕФбєРызгЮЊЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂЧБШНЯEЁЂFЕФЕквЛЕчРыФмЃКEЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁF(бЁЬюЁАЃОЁБЛђЁАЃМЁБ)ЁЃ
ЂШBD2дкИпЮТИпбЙЯТЫљаЮГЩЕФОЇАћШчгвЭМЫљЪОЁЃИУОЇЬхЕФРраЭЪєгк
ЁЁЁЁ ЁЁЁЁЁЁЁЁ(бЁЬюЁАЗжзгЁБЁЂЁАдзгЁБЁЂЁАРызгЁБЛђЁАН№ЪєЁБ)ОЇЬхЃЌИУОЇЬхжаBдзгЕФдгЛЏаЮЪНЮЊЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂЩЙтЦзжЄЪЕЕЅжЪFгыЧПМюадШмвКЗДгІга[F(OH)4]-ЩњГЩЃЌдђ[F(OH)4]-жаДцдкЁЁ ЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ aЃЎЙВМлМќЁЁЁЁ bЃЎЗЧМЋадМќЁЁЁЁ cЃЎХфЮЛМќЁЁЁЁ dЃЎІвМќЁЁЁЁ eЃЎІаМќ
25ЃЎ(15Зж)ЬњМАЦфЛЏКЯЮядкШеГЃЩњЛюжагІгУЙуЗКЃЌЧыЛиД№ЯТСаЮЪЬтЃК
(1)Fe(NO3)3ЁЄ9H2OвзШмгкЫЎЃЌЮЂШмгкЯѕЫсЃЌжївЊгУзїДпЛЏМСКЭУНШОМСЁЃЙЄвЕЩЯгУЯИЬњаМгыЯЁЯѕЫсЗДгІжЦБИЃЌжївЊСїГЬШчЯТЃК
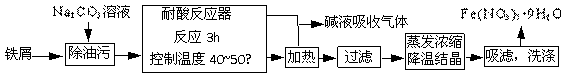
ЂйNa2CO3 ШмвКГЪМюадЃЌПЩвдГ§гЭЮлЃЌдвђЪЧ(гУРызгЗНГЬЪНБэЪО)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁЂкФЭЫсЗДгІЦїжаПЩвдЙлВьЕНЕФЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
жЦБИЙ§ГЬжаашПижЦМгШыЬњаМЕФСПЃЌЕБЙлВьЕНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЕФЯжЯѓЪБгІЭЃжЙМгШыЬњаМЃЛ
ЂлжЦЕУЕФFe(NO3)3ЁЄ9H2OгУ20% HNO3ЯДЕгЃЌЦфдвђЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
ЂмШєдкЪЕбщЪвжаНјааеєЗЂХЈЫѕЁЂНЕЮТНсОЇЕФВйзїЃЌдђЫљашЕФвЧЦїгаЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ(аДГіжївЊвЧЦїжаЕФШ§жжМДПЩ)
(2)ФГаЫШЄаЁзщдкЪЕбщЪвгУгвЭМзАжУжЦШЁFe(NO3)3(ЙЬЖЈЫљгУвЧЦїКЭМгШШзАжУЮДЛГі)
ЁЁЂйИУЪЕбщжаЖддВЕзЩеЦПМгШШЕФзюМбЗНЪНгУЁЁЁЁЁЁЁЁЁЁЁЁЁЁ МгШШЃЛ
ЁЁЂкзАжУжадВЕзЩеЦПЩЯЗНГЄЕМЙмЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁЂлЧыдкЭМжаащЯпПђФкЛГіЗРжЙЕЙЮќЕФЮВЦјЮќЪезАжУ
ЁЁ(ЬсЪОЃКМювКПЩПьЫйЁЂГфЗжЮќЪеВњЩњЕФЕЊбѕЛЏЮяЦјЬх)ЁЃ
[БиПМВПЗж]
24ЃЎ(15Зж)ФГбаОПадбЇЯАаЁзщЖдЙ§СПЬПЗлгыбѕЛЏЬњЗДгІЕФЦјЬхВњЮяГЩЗжНјаабаОПЁЃ
ЁЁ ЂХЬсГіМйЩшЁЁ ЂйИУЗДгІЕФЦјЬхВњЮяЪЧCO2ЁЃ
ЂкИУЗДгІЕФЦјЬхВњЮяЪЧCOЁЃ
ЂлИУЗДгІЕФЦјЬхВњЮяЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ 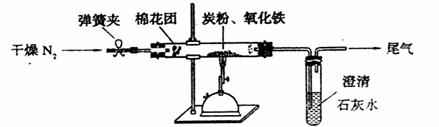 ЁЁ
ЁЁ ЂЦЩшМЦЗНАИЁЁ ШчЭМЫљЪОЃЌНЋвЛЖЈСПЕФбѕЛЏЬњдкИєОјПеЦјЕФЬѕМўЯТгыЙ§СПЬПЗлЭъШЋЗДгІЃЌВтЖЈВЮМгЗДгІЕФЬМдЊЫигыбѕдЊЫиЕФжЪСПБШ
ЁЁ
ЁЁ ЂЦЩшМЦЗНАИЁЁ ШчЭМЫљЪОЃЌНЋвЛЖЈСПЕФбѕЛЏЬњдкИєОјПеЦјЕФЬѕМўЯТгыЙ§СПЬПЗлЭъШЋЗДгІЃЌВтЖЈВЮМгЗДгІЕФЬМдЊЫигыбѕдЊЫиЕФжЪСПБШ
ЂЧВщдФзЪСЯ
ЕЊЦјВЛгыЬМЁЂбѕЛЏЬњЗЂЩњЗДгІЁЃЪЕбщЪвПЩвдгУТШЛЏяЇБЅКЭШмвККЭбЧЯѕЫсФЦ(NaNO2)БЅКЭ
ШмвКЛьКЯМгШШЗДгІжЦЕУЕЊЦјЁЃЧыаДГіИУЗДгІЕФРызгЗНГЬЪНЃК
ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ ЂШЪЕбщВНжш
ЁЁЁЁ ЂйАДЩЯЭМСЌНгзАжУЃЌВЂМьВщзАжУЕФЦјУмадЃЌГЦШЁ3.20gбѕЛЏЬњЁЂ2.00gЬМЗлЛьКЯОљдШЃЌЗХШы48.48gЕФгВжЪВЃСЇЙмжаЃЛ
ЁЁЁЁ ЂкМгШШЧАЃЌЯШЭЈвЛЖЮЪБМфДПОЛИЩдяЕФЕЊЦјЃЛ
ЁЁЁЁ ЂлЭЃжЙЭЈШыN2КѓЃЌМаНєЕЏЛЩМаЃЌМгШШвЛЖЮЪБМфЃЌГЮЧхЪЏЛвЫЎ(зуСП)БфЛызЧЃЛ
ЁЁЁЁ ЂмД§ЗДгІНсЪјЃЌдйЛКЛКЭЈШывЛЖЮЪБМфЕФЕЊЦјЁЃРфШДжСЪвЮТЃЌГЦЕУгВжЪВЃСЇЙмКЭЙЬЬхзмжЪСПЮЊ52.24gЃЛ
ЁЁЁЁ ЂнЙ§ТЫГіЪЏЛвЫЎжаЕФГСЕэЃЌЯДЕгЁЂКцИЩКѓГЦЕУжЪСПЮЊ2.00gЁЃ
ВНжшЂкЁЂЂмжаЖМЗжБ№ЭЈШыN2ЃЌЦфзїгУЗжБ№ЮЊЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂЩЪ§ОнДІРэ
ЪдИљОнЪЕбщЪ§ОнЗжЮіЃЌаДГіИУЪЕбщжабѕЛЏЬњгыЬМЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЃК
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ ЂЪЪЕбщгХЛЏЁЁ бЇЯАаЁзщгаЭЌбЇШЯЮЊгІЖдЪЕбщзАжУНјвЛВНЭъЩЦЁЃ
ЁЁЁЁ ЂйМзЭЌбЇШЯЮЊЃКгІНЋГЮЧхЪЏЛвЫЎЛЛГЩBa(OH)2ШмвКЃЌЦфРэгЩЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁЁЁ ЂкДгЛЗОГБЃЛЄЕФНЧЖШЃЌЧыФудйЬсГівЛИігХЛЏЗНАИЃКЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
23ЃЎ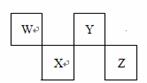 (15Зж)WЁЂXЁЂYЁЂZЫФжжЖЬжмЦкдЊЫидкдЊЫижмЦкБэжа
(15Зж)WЁЂXЁЂYЁЂZЫФжжЖЬжмЦкдЊЫидкдЊЫижмЦкБэжа ЕФЮЛжУШчгвЭМЫљЪОЃЌЦфжа
ЕФЮЛжУШчгвЭМЫљЪОЃЌЦфжа YгыФЦдЊЫиКЭЧтдЊЫиОљПЩаЮГЩдзгИіЪ§lЃК1КЭ1ЃК2ЕФЛЏКЯЮяЁЃЧыЛиД№ЯТСаЮЪЬтЁЃ
YгыФЦдЊЫиКЭЧтдЊЫиОљПЩаЮГЩдзгИіЪ§lЃК1КЭ1ЃК2ЕФЛЏКЯЮяЁЃЧыЛиД№ЯТСаЮЪЬтЁЃ
(1)WдЊЫиаЮГЩЕФЭЌЫивьаЮЬхЕФОЇЬхРраЭПЩФмЪЧ(ЬюађКХ)ЁЁЁЁ ЁЁЁЁ
ЂйдзгОЇЬхЁЁЁЁ ЂкРызгОЇЬхЁЁ ЂлЗжзгОЇЬхЁЁЁЁ ЂмН№ЪєОЇЬх
 (2)H2Y2ЕФЕчзгЪНЮЊЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЌNa2Y2жа
(2)H2Y2ЕФЕчзгЪНЮЊЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЌNa2Y2жа ЕФЛЏбЇМќжжРр
ЕФЛЏбЇМќжжРр
ЮЊЃКЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
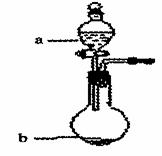
(3)дкгвЭМжа ЃЌbЕФpHдМЮЊ7ЃЌЧвКЌгаFe2+КЭЕэЗлKIЕФЫЎШмвКЃЌ
ЃЌbЕФpHдМЮЊ7ЃЌЧвКЌгаFe2+КЭЕэЗлKIЕФЫЎШмвКЃЌ
aЮЊH2Y2ЕФЫЎШмвКЃЌа§ПЊЗжвКТЉЖЗа§ХЅЃЌЙлВьЕНЩеЦПжа ШмвК
ШмвК
ГЪРЖЩЋВЂгаКьКжЩЋГСЕэЩњГЩЁЃЕБЯћКФ2 molI-ЪБЃЌЙВзЊвЦ3mol
ЕчзгЃЌИУЗДгІЕФРызгЗНГЬЪНЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(4)вбжЊЃК298KЪБЃЌН№ЪєФЦгыY2ЦјЬхЗДгІЃЌШєЩњГЩ1 molNa2YЙЬЬхЪБЃЌЗХГіШШСП414 kJЃЛШєЩњГЩ1mol Na2Y2ЙЬЬхЪБЃЌЗХГіШШСП511 kJЁЃдђгЩNa2YЙЬЬхгыY2ЦјЬхЗДгІЩњГЩNa2Y2ЙЬЬхЕФШШЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(5)XЕФдзгНсЙЙЪОвтЭМЮЊЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЃZдкжмЦкБэжа ЕФЮЛжУЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЕФЮЛжУЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(6)гаШЫЩшЯыРћгУдЕчГидРэвдЦјЬхZ2КЭЧтЦјжЦБИвЛжжживЊЕФЛЏЙЄдСЯЃЌЭЌЪБЛёШЁЕчФмЁЃМйЩшетжжЯыЗЈПЩааЃЌгУЪЏФЋзїЕчМЋВФСЯЃЌгУЯЁбЮЫсзїЕчНтжЪШмвКЃЌдђЭЈШыZ2ЕФЕчМЋЮЊдЕчГиЕФЁЁЁЁЁЁЁЁЁЁ МЋЃЌЦфЕчМЋЗДгІЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
12ЃЎ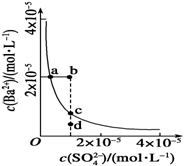 ФГЮТЖШЪБЃЌBaSO4дкЫЎжаЕФГСЕэШмНтЦНКтЧњЯпШчгвЭМЫљЪОЁЃ
ФГЮТЖШЪБЃЌBaSO4дкЫЎжаЕФГСЕэШмНтЦНКтЧњЯпШчгвЭМЫљЪОЁЃ
ЯТСаЫЕЗЈДэЮѓЕФЪЧ
ЁЁA. МгШыЪЪСПBaCl2(ЙЬЬх) ПЩвдЪЙШмвКгЩdЕуБфЕНcЕу
B. ЭЈЙ§МгЫЎЯЁЪЭПЩвдЪЙШмвКгЩbЕуБфЕНaЕу
C. dЕуЮоBaSO4ГСЕэЩњГЩЁЁ
D. aЕуЖдгІЕФKspЕШгкcЕуЖдгІЕФKsp
ЕкЂђОэ (ЙВ58Зж)
[БиПМВПЗж]
11ЃЎLi-SOCl2ЕчГиПЩгУгкаФдрЦ№ВЋЦїЁЃИУЕчГиЕФЕчМЋВФСЯЗжБ№ЮЊяЎКЭЬМЃЌЕчНтвКЪЧLiAlCl4-SOCl2ЁЃЕчГиЕФзмЗДгІПЩБэЪОЮЊЃК4Li+2SOCl2 =4LiCl+S +SO2 ЯТСаЫЕЗЈДэЮѓЕФЪЧ
AЃЎИУЕчГиЙЄзїЪБЃЌе§МЋЗДгІЮЊЃК2SOCl2+4eЃ= 4ClЃ+S+SO2
BЃЎяЎЕчМЋзїИУЕчГиИКМЋЃЌИКМЋЗДгІЮЊЃКLiЃeЃ=Li+
CЃЎИУЕчГиЙЄзїЪБЃЌЕчзгЭЈЙ§ЭтЕчТЗДге§МЋСїЯђИКМЋ
DЃЎИУЕчГизщзАЪБЃЌБиаыдкЮоЫЎЮобѕЬѕМўЯТНјаа
10ЃЎ25ЁцЃЌНЋVa mL pH=2ЕФCH3COOHШмвКгыVb mL pH=12ЕФNaOHШмвКЛьКЯЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁ (ЁЁЁЁ )
ЁЁЁЁ AЃЎШєVa=VbЃЌдђЛьКЯКѓШмвКpH=7
ЁЁЁЁ BЃЎШєVaЃМVbЃЌдђЛьКЯКѓШмвКpHвЛЖЈДѓгк7
ЁЁЁЁ CЃЎШєVa=VbЃЌдђCH3COOHгыNaOHЧЁКУЭъШЋжаКЭ
ЁЁЁЁ DЃЎШєVa=VbЃЌЛьКЯКѓШмвКжаЮЂСЃХЈЖШЕФЙиЯЕПЩФмЮЊЃКc(CH3COO)ЃОc(Na+)ЃОc(H+)ЃОc(OHЃ)
9ЃЎУмБеШнЦїжаXЁЂYЁЂZШ§жжЦјЬхЕФГѕЪМХЈЖШКЭВЛЭЌЮТЖШЯТЕФЦНКтХЈЖШШчЯТБэЃК
|
ЮяжЪ |
X |
Y |
Z |
|
25ЁцЪБГѕЪМХЈЖШ/mol/L |
0.1 |
0.2 |
0 |
|
25ЁцЪБЦНКтХЈЖШ/mol/L |
0.05 |
0.05 |
0.1 |
|
50ЁцЪБЦНКтХЈЖШ/mol/L |
0.06 |
0.08 |
0.08 |
ЯТСаЫЕЗЈДэЮѓЕФЪЧ
AЃЎИУЗДгІЪЧЗХШШЗДгІ
BЃЎИУЗДгІПЩБэЪОЮЊЁЁ X(g)+3Y(g) 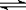 ЁЁ2Z(g)
ЁЁ2Z(g)
CЃЎЦНКтКѓШєдіДѓбЙЧПЃЌдЦНКтНЋЯђЩњГЩZЕФЗНЯђвЦЖЏЃЌXХЈЖШНЋБШдРДМѕЩй
DЃЎЗДгІДяЕНЦНКтЪБЃЌYЕФЗжНтЫйТЪЪЧZЕФЗжНтЫйТЪЕФ1.5БЖ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com