
题目列表(包括答案和解析)
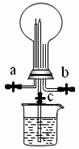
15.(12分)某化学兴趣小组的同学利用下图所示实验装置进行NH3、Cl2的制备、性质等实验(图中夹持装置均省略)。请按要求填空。






|
|

|
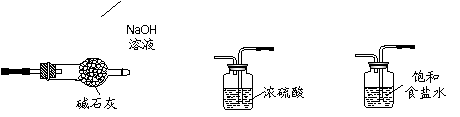
|
供选择的装置:
|
(1)利用A装置可制备NH3外,还可制备的气体有 (写出两种即可)。
(2)请利用D、G装置设计一个简单的实验验证Cl2、Fe3+、I2的氧化性强弱(实验中不断小心振荡D装置中的试管)。
① 试剂M为 溶液;
② 装置G中发生反应的离子方程式 ;
③ 实验中若先观察到CCl4层先由无色变为 色,上层溶液后变为 色,证明氧化性为Cl2>Fe3+>I2。
(3)氯气和氨气在常温下相混合就会反应生成氯化铵和氮气,该反应的化学方程式为 ;
A、B为干燥氨气的制取装置,将G、F、E依次相连组成纯净、干燥氯气的制取装置。C为氯气与氨气反应的探究及尾气处理装置,实验时关闭c活塞。将氯气和氨气通入到装置C烧瓶中。回答下列问题:
① 装置A中的烧瓶内固体宜选用 (选填以下选项的代号)。
A.碱石灰 B.氯化钙 C.五氧化二磷 D.生石灰 E.二氧化硅
② 虚线框内应添加必要的除杂装置,请从上图供选择的装置中选择,并将编号填入下列空格。B 、F 。
③ 实验中装置C烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子 。
④ 若实验完毕后C装置的烧瓶内有N2和少量的Cl2,应如何处理才能不污染环境? 。
14.某温度下,在一密闭容器中发生如下可逆反应:2E(g)  F(g)+xG(g);△H<0。若起始时E浓度为a mol·L-1,F、G浓度均为0,达平衡时E浓度为O.5a mol·L-1;若E的起始浓度改为 2a mol·L-1,F、G浓度仍为O,当达到新的平衡时,下列说法正确的是
F(g)+xG(g);△H<0。若起始时E浓度为a mol·L-1,F、G浓度均为0,达平衡时E浓度为O.5a mol·L-1;若E的起始浓度改为 2a mol·L-1,F、G浓度仍为O,当达到新的平衡时,下列说法正确的是
A.升高温度时,正反应速率加快、逆反应速率减慢
B.若x=l,容器体积保持不变,新平衡下E的体积分数为50%
C.若x=2,容器体积保持不变,新平衡下F的平衡浓度小于0.5a mol·L-1
D.若x=2,容器压强保持不变,新平衡下E的物质的量为a mol
第Ⅱ卷 非选择题(共78分)
13.下列溶液中微粒的物质的量浓度关系正确的是
A.氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)]
B.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2 c(H2CO3)
C.等物质的量浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+ c(H2CO3)
D.室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加NaOH溶液至中性:
c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
12.某同学按右图所示的装置进行试验。A、B 为两种常见金属,它们的硫酸盐可溶于水。当 K 闭
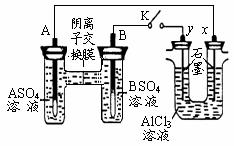 合时,在交换膜处 SO42一从右向左移动。下列分析错误的是
合时,在交换膜处 SO42一从右向左移动。下列分析错误的是
A.金属活动性A强于B
B.B 的电极反应: B-2e一= B2+
C.x电极上有 H2 产生,发生还原反应
D.反应初期, x 电极周围出现白色沉淀,不久沉淀溶解
11. 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如在右图转化关系(部分生成物
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如在右图转化关系(部分生成物
和反应条件略去)下列推断错误的是
A.若X是Na2CO3,C为含极性键的非极性分子,
则A一定是氯气,且D和E不反应
B.若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,则E是一种清洁的能源
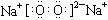 C.若D为CO,C能和E反应,则A一定为Na2O2,其电子式是
C.若D为CO,C能和E反应,则A一定为Na2O2,其电子式是
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
10.下列离子或化学方程式与所述事实相符且正确的是
A.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O
 B.用K37ClO3 与浓盐酸反应制氯气: K37ClO3
+ 6HCl (浓) K37Cl + 3Cl2↑+ 3H2O
B.用K37ClO3 与浓盐酸反应制氯气: K37ClO3
+ 6HCl (浓) K37Cl + 3Cl2↑+ 3H2O
C.向硅酸钠溶液中通入过量的CO2: SiO32- + 2CO2 + 3H2O =H4SiO4↓+ 2HCO3-
D.向AlCl3溶液中滴加过量的氨水:Al3++4OH-=AlO2-+ 2H2O
9.下列化学实验事实及其解释或结论都正确的是
A.向相同浓度的NaCl、NaI溶液中滴加硝酸银溶液,先出现黄色沉淀,说明KSP (AgI)>KSP (AgCl)
B.向紫色石蕊试液中加入过量的Na2O2粉末,溶液先变蓝后褪色,说明Na2O2已变质
C.向某溶液中加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在
D.把相同物质的量的CuSO4、FeCl3和Zn置于水中充分反应,所得溶液中含有 Zn2+、Cu2+、Fe2+
8.食品香精菠萝酯的生产路线(反应条件略去)如下:

下列叙述错误的是
A.步骤(1)产物中残留的苯酚可用FeCl3溶液检验
B.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
D.步骤(2)产物中残留的烯丙醇可用溴水检验
不定项选择题(本题包括6小题,每小题3分,共18分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得1分,选两个且都正确的得满分,但只要选错一个,该小题就为0分)
7. 在下列条件下,一定能大量共存的离子组是
A.在AlCl3溶液中:K+、Na+、SiO32-、SO42-
B.在=10-8 的溶液中:Na+、K+、S2-、SO2-3
C.能使甲基橙变红的溶液:Na+、NH+4、Fe2+、NO-3
D.加入铝粉有大量氢气产生的溶液中:Mg2+、K+、NO3-、C1-
6.某同学用下列装置制备并检验Cl2的性质。
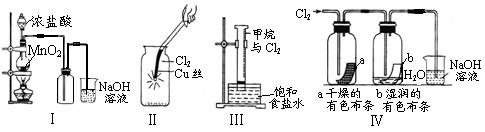
下列说法正确的是
A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗完
B.Ⅱ图中:生成蓝色的烟
C.Ⅲ图中:量筒中发生了加成反应
D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com