
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
26Ђй ТШЛЏяЇ ЃЌAЁЁЁЁЁЁЁЁЁЁ
Ђк NH4ClКЭHClЁЁЁЁЁЁЁЁЁЁ
Ђл ЃМ ЃЌЃН
27. HCO3-+H2O H2CO3+OH-ЃЛДѓгкЃЛ ЂХ вв ЃЛ BЃЛ
H2CO3+OH-ЃЛДѓгкЃЛ ЂХ вв ЃЛ BЃЛ
ЂЦЕШгк ЃЛМзЃЛЂЧвв ЃЛГЃбЙЯТМгШШNaHCO3ЕФЫЎШмвКЃЌШмвКЕФЮТЖШДяВЛЕН150Ёц
23. вѕЁЁ ИКЁЁ 2H+ + 2eЁњH2 ЁќЁЁ =ЁЁ >ЁЁ 2Cl-+ 2H2OЁЁЁЁЁЁ 2OH-
+Cl2 Ёќ+ H2ЁќЁЁ 24ЃЎOH-ЁЂK+ЁЂCl-ЃЛЬњЗлЃЛAgЃЛAg+ЁЂCl-ЁЂFe3+ЁЂOH-ЃЛKNO3
вѕЁЁ ИКЁЁ 2H+ + 2eЁњH2 ЁќЁЁ =ЁЁ >ЁЁ 2Cl-+ 2H2OЁЁЁЁЁЁ 2OH-
+Cl2 Ёќ+ H2ЁќЁЁ 24ЃЎOH-ЁЂK+ЁЂCl-ЃЛЬњЗлЃЛAgЃЛAg+ЁЂCl-ЁЂFe3+ЁЂOH-ЃЛKNO3
ЁЁ25(1)NO3-ЁЂSO42- Mg2+ЁЂAl3+ЃЛFe2+ЁЂHCO3-ЁЂI-ЁЂBa2+ЃЛ
(2)K+ЕФМьбщПЩвдгУбцЩЋЗДгІЃЛCl-ЕФМьбщЃКЭљШмвКжаМгзуСПЕФЯѕЫсБЕШмвКЃЌЙ§ТЫКѓЃЌдкТЫвКжаМгЯѕЫсвјШмвКЃЌдйМгЯЁЯѕЫсЃЌАзЩЋГСЕэВЛШмНтЁЃ
18ЃЎBDЁЁ 19ЃЎDЁЁЁЁ 20ЃЎBDЁЁЁЁ 21ЃЎCЁЁЁЁ 22ЃЎAD
6ЃЎC 7ЃЎB ЁЁ8ЃЎC ЁЁ9ЃЎB ЁЁ10ЃЎBЁЁ 11 ЁЁC ЁЁ12ЃЎB 13ЃЎBЁЁ 14ЁЁ CЁЁ 15ЃЎAЁЁ 16ЃЎDЁЁ 17ЃЎA
1 C 2ЃЎB 3ЃЎDЁЁ 4ЃЎCЁЁ 5ЃЎC
31ЁЂ(12Зж)ШЁвЛЖЈСПЕФЬМЫсФЦЁЂЬМЫсЧтФЦКЭСђЫсФЦЕФЛьКЯЮягы250КСЩ§1ФІЖћ/Щ§ЕФбЮЫсЗДгІЃЌЩњГЩ2..016Щ§ЖўбѕЛЏЬМ(БъзМзДПіЯТ)ЃЌШЛКѓМгШы500КСЩ§0.100ФІЖћ/Щ§ЕФЧтбѕЛЏБЕШмвКЃЌЕУЕНГСЕэЕФжЪСПЮЊ2.33ПЫЃЌШмвКжаЙ§СПЕФМюгУ10.0КСЩ§1.00ФІЖћ/Щ§ЕФбЮЫсЧЁКУЭъШЋжаКЭЁЃМЦЫуЛьКЯЮяжаИїЮяжЪЕФжЪСПЁЃ
ЕчНтжЪШмвКД№АИ
30ЁЂ(6Зж)дк500mlфхЛЏбЧЬњШмвКжаЃЌЭЈШыБъПіЯТЕФТШЦј11.2Щ§ЃЌЗДгІжага2/3ЕФBr-ЮДБЛбѕЛЏЃЌ
(1)дђдРДфхЛЏбЧЬњШмвКЕФЮяжЪЕФСПХЈЖШЪЧЖрЩйЃП
(2)ШєНЋдШмвКжаЕФРызгШЋВПбѕЛЏЃЌЛЙашЭЈШыБъПіЯТЕФТШЦјЖрЩйЩ§ЃП
29ЁЂ(12Зж)ФГжжЮИвЉЕФжЙЫсМСЮЊЬМЫсИЦЃЌВтЖЈУПЦЌвЉжаЬМЫсИЦКЌСПЕФЗНЗЈгавдЯТМИИіВНжшВйзї(ЩшвЉЦЌжаЕФЦфЫћГЩЗжВЛгыбЮЫсЁЂЧтбѕЛЏФЦ ЗДгІ)ЃК
ЂйХфжЦ0.10mol/LЯЁбЮЫсКЭ0.10mol/LЕФЧтбѕЛЏФЦШмвК
ЂкШЁвЛСЃвЉЦЌ(вЉЦЌжЪСПЯрЭЌОљЮЊ0.1g)ЃЌбаФЅКѓМгШы20.0mlеєСѓЫЎЃЌЁЁЁЁЁЁЁЁ
ЂлвдЗгЬЊзїжИЪОМСЃЌгУ0.10mol/LЧтбѕЛЏФЦШмвКЕЮЖЈЃЌгУШЅЬхЛ§ЮЊVЩ§ЪБДя
ЕНжеЕуЁЃ
ЂмМгШы25ml0.10mol/LЯЁбЮЫсЧыЛиД№ЯТСаЮЪЬтЃК
(1)ВтЖЈЙ§ГЬжаЕФе§ШЗВйзїЫГађЪЧ_________________(ЬюађКХ)
(2)ВтЖЈЙ§ГЬжаЗЂЩњЕФРызгЗДгІЗНГЬЪНЪЧЃК_______________ЁЁЁЁЁЁ _____________ЃЌ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁ



 ЁЁ(3)ЯТСаЫљЪОЕФвЧЦїжаЃЌдкХфжЦЯЁбЮЫсКЭЧтбѕЛЏФЦШмвКЪБвЛЖЈВЛашвЊЕФЪЧ________________________
ЁЁ(3)ЯТСаЫљЪОЕФвЧЦїжаЃЌдкХфжЦЯЁбЮЫсКЭЧтбѕЛЏФЦШмвКЪБвЛЖЈВЛашвЊЕФЪЧ________________________
 ЁЁ
ЁЁ
ЁЁЁЁ AЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЁЁЁЁЁЁЁЁЁЁ CЁЁЁЁЁЁЁЁ DЁЁЁЁЁЁ EЁЁЁЁЁЁЁЁ F
(4) ФГЭЌбЇЫФДЮВтЖЈЕФVЪ§ОнШчЯТЃК
|
ВтЖЈДЮађ |
ЕквЛДЮ |
ЕкЖўДЮ |
ЕкШ§ДЮ |
ЕкЫФДЮ |
|
V/ml |
12.9 |
15.4 |
13.1 |
13.0 |
ИљОнИУЭЌбЇЕФЪЕбщЪ§ОнЃЌМЦЫувЉЦЌжаЕФЬМЫсИЦЕФжЪСПЗжЪ§ЮЊ_______________
(5) ШєЮЊМѕаЁЮѓВюЃЌИУЪЕбщашвЊЕЮЖЈ4ДЮЃЌЪЕбщЪвЯжга50mlЃЌ100ml,250ml,500mlЙцИёЕФШнСПЦПЃЌХфжЦБОЪЕбщгУЯЁбЮЫсгІбЁгУЕФШнСПЦПЙцИёзюКУЮЊ_________ml
28ЁЂ(8Зж)гаЯТСаМИжжШмвКЃК
(1)вЛЖЈЮТЖШЯТЃЌБљДзЫсМгЫЎЯЁЪЭЙ§ГЬжаШмвКЕФЕМЕчФмСІШчЭМ2-9ЫљЪОЧыЛиД№ЃК
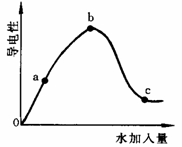
ЂйЁА0ЁБЕуЮЊЪВУДВЛЕМЕчЁЁЁЁ ЃЛ
ЂкaЁЂbЁЂcШ§ЕуpHжЕгЩДѓЕНаЁЕФЫГађЮЊЁЁЁЁЁЁ ЃЛ
ЂлaЁЂbЁЂcШ§ЕужаДзЫсЕФЕчРыЖШІСзюДѓЕФвЛЕуЪЧЁЁ ЁЁЁЁЕуЃЛ
ЂмШєЪЙcЕуШмвКжаЕФ[CH3COO-]ЬсИпЃЌдкШчЯТДыЪЉжаПЩбЁдёЁЁЁЁЁЁ ЁЃ(ЬюБъКХ)
A.МгШШЁЁ B.МгКмЯЁЕФNaOHШмвКЁЁ C.МгЙЬЬхKOHЁЁ
ЁЁD.МгЫЎЁЁ E.МгЙЬЬхNaAcЁЁ F.МгZnСЃ
(2)вбжЊФГШмвКжажЛКЌгаOH-ЁЂH+ЁЂNa+ЁЂCH3COO- ЫФжжРызгЁЃ (A)ШєШмвКжажЛШмНтСЫвЛжжШмжЪЃЌдђИУШмжЪЪЧ_______________________ЁЃ
(B)ШєШмвКжаc (CH3COO-)ЃОc (Na+)ЃОc (H+)ЃОc (OH- )ЃЌдђКЌгаЕФШмжЪЪЧ ЁЁЁЁЁЁЁЁ ______________________________________ЁЃ
(C)ШєШмвКЪЧгЩЬхЛ§ЯрЕШЕФNaOHШмвККЭCH3COOHШмвКЛьКЯЖјГЩЃЌЧвЧЁКУГЪжаадЃЌ
дђЛьКЯЧАc (CH3COOH)_________c (NaOH)(ЬюЁАЃМЁБЁЂЁАЃОЁБЛђЁА=ЁБ)ЁЃ
27ЁЂ(14Зж)10ЁцЪБМгШШNaHCO3БЅКЭШмвКЃЌВтЕУИУШмвКЕФpHЗЂЩњШчЯТБфЛЏЃК
|
ЮТЖШ(Ёц) |
10 |
20 |
30 |
МгШШжѓЗаКѓРфШДЕН50Ёц |
|
pH |
8.3 |
8.4 |
8.5 |
8.8 |
МзЭЌбЇШЯЮЊЃЌИУШмвКЕФpHЩ§ИпЕФдвђЪЧHCO3-ЕФЫЎНтГЬЖШдіДѓЃЌЙЪМюаддіЧПЃЌИУЗДгІЕФРызгЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃввЭЌбЇШЯЮЊЃЌШмвКpHЩ§ИпЕФдвђЪЧNaHCO3ЪмШШЗжНтЃЌЩњГЩСЫNa2CO3ЃЌВЂЭЦЖЯNa2CO3ЕФЫЎНтГЬЖШЁЁЁЁЁЁ (ЬюЁАДѓгкЁБЛђЁАаЁгкЁБ)NaHCO3ЁЃБћЭЌбЇШЯЮЊМзЁЂввЕФХаЖЯЖМВЛГфЗжЁЃБћШЯЮЊЃК
ЂХжЛвЊдкМгШШжѓЗаЕФШмвКжаМгШызуСПЕФЪдМСXЃЌШєВњЩњГСЕэЃЌдђЁЁЁЁ (ЬюЁАМзЁБЛђЁАввЁБ)ХаЖЯе§ШЗЁЃЪдМСXЪЧЁЁЁЁЁЁ ЁЃ
A.Ba(OH)2ШмвКЁЁЁЁ B.BaCl2ШмвКЁЁЁЁ C.NaOHШмвКЁЁЁЁ D.ГЮЧхЕФЪЏЛвЫЎ
ЂЦНЋМгШШКѓЕФШмвКРфШДЕН10ЁцЃЌШєШмвКЕФpHЁЁЁЁ (ЬюЁАИпгкЁБЁЂЁАЕЭгкЁБЛђЁАЕШгкЁБ)8.3ЃЌдђЁЁЁЁ (ЬюЁАМзЁБЛђЁАввЁБ)ХаЖЯе§ШЗЁЃ
ЂЧВщдФзЪСЯЃЌЗЂЯжNaHCO3ЕФЗжНтЮТЖШЮЊ150ЁцЃЌБћЖЯбд ЁЁЁЁ(ЬюЁАМзЁБЛђЁАввЁБ)ХаЖЯЪЧДэЮѓЕФЃЌРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com