
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
5£®ėĀ(N2H4)-æÕĘųČ¼ĮĻµē³ŲŹĒŅ»ÖÖ»·±£ŠĶ¼īŠŌČ¼ĮĻµē³Ų£¬µē½āÖŹČÜŅŗŹĒ20%-30%µÄKOH
ČÜŅŗ”£µē³Ų×Ü·“Ó¦ĪŖ£ŗN2H4+O2£½N2+2H2O”£ĻĀĮŠ¹ŲÓŚøĆČ¼ĮĻµē³Ų¹¤×÷Ź±µÄĖµ·ØÕżČ·µÄŹĒ( )
”””””””” A£®øŗ¼«µÄµē¼«·“Ó¦Ź½ŹĒ£ŗN2H4+4OH£”ś4H2O+N2”ü+4e£
”””””””” B£®Õż¼«µÄµē¼«·“Ó¦Ź½ŹĒ£ŗO2+4H++4e£”ś2H2O
 ”””””””” C£®ČÜŅŗÖŠŅõĄė×ÓĻņÕż¼«ŅʶÆ
”””””””” C£®ČÜŅŗÖŠŅõĄė×ÓĻņÕż¼«ŅʶÆ
”””””””” D£®µē½āŗóµē½āÖŹČÜŅŗµÄ¼īŠŌŌöĒæ
4£®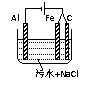 Čżµē¼«·ØĪŪĖ®“¦ĄķŌĄķČēĻĀĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ(”””” )
Čżµē¼«·ØĪŪĖ®“¦ĄķŌĄķČēĻĀĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ(”””” )
A£®Cµē¼«µē¼«·“Ó¦Ź½ĪŖ£ŗ2Cl--2e-=Cl2”ü
B£®Ņõ¼«µÄAl²»»įÓŠ±ä»Æ
C£®Ė«Ńō¼«¹²Ķ¬×÷ÓĆŹĒĪŖĮĖ²śÉś“ŁŹ¹ĪŪĪļ¾Ū³ĮµÄFe(OH)3
D£®ĪŖĮĖŌö¼Óµ¼µēŠŌ£¬ĪŪĖ®ÖŠŅ²æÉŅŌ¼ÓČėNa2SO4
3£®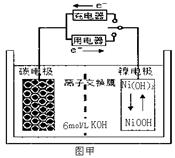 Ņ»ÖÖĢ¼ÄÉĆ×¹ÜÄܹ»Īüø½ĒāĘų£¬ÓĆÕāÖÖ²ÄĮĻÖʱøµÄ¶ž“Īµē³ŲŌĄķČēĶ¼¼×ĖłŹ¾£¬øƵē³ŲµÄµē½āÖŹĪŖ6 mol/L KOHČÜŅŗ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·(”” )””””””””””””””””””””
Ņ»ÖÖĢ¼ÄÉĆ×¹ÜÄܹ»Īüø½ĒāĘų£¬ÓĆÕāÖÖ²ÄĮĻÖʱøµÄ¶ž“Īµē³ŲŌĄķČēĶ¼¼×ĖłŹ¾£¬øƵē³ŲµÄµē½āÖŹĪŖ6 mol/L KOHČÜŅŗ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·(”” )””””””””””””””””””””
A”¢·ÅµēŹ±K+ŅĘĻņøŗ¼«
”””””” B”¢·ÅµēŹ±µē³Ųøŗ¼«µÄµē¼«·“Ó¦ĪŖ£ŗH2-2e- = 2H+
”””””” C”¢·ÅµēŹ±µē³ŲÕż¼«µÄµē¼«·“Ó¦ĪŖ£ŗ
”””””” NiO(OH)+H2O+e- = Ni(OH)2+OH-
D”¢øƵē³Ų³äµēŹ±½«Ģ¼µē¼«ÓėµēŌ“µÄÕż¼«ĻąĮ¬
2”¢ČēĶ¼ŹĒµē½ā±„ŗĶŹ³ŃĪĖ®µÄ×°ÖĆ£¬ĻĀĮŠÓŠ¹ŲÅŠ¶ĻÕżČ·µÄŹĒ(”””” )
A£®µē½āŹ±Ńō¼«µĆµ½ĀČĘų£¬Ņõ¼«µĆµ½½šŹōÄĘ
B£®ČōŌŚŃō¼«ø½½üµÄČÜŅŗÖŠ£¬µĪČėKIČÜŅŗ£¬ČÜŅŗĻŌ×Ų»ĘÉ«
C£®ČōŌŚŅõ¼«ø½½üµÄČÜŅŗÖŠµĪČė·ÓĢŖŹŌŅŗ£¬ČÜŅŗĻŌĪŽÉ«
D£®£®µē½āŅ»¶ĪŹ±¼äŗ󣬽«Č«²æµē½āŅŗ×ŖŅʵ½ÉÕ±ÖŠ£¬³ä·Ö½Į°čŗóČÜŅŗ³ŹÖŠŠŌ
1£®LiFePO4ŠĀŠĶļ®Ąė×Ó¶ÆĮ¦µē³ŲŅŌĘ䶥ĢŲµÄÓÅŹĘ³ÉĪŖ°ĀŌĖ»įĀĢÉ«ÄÜŌ“µÄŠĀ³č.ŅŃÖŖøƵē³Ų·ÅµēŹ±µÄµē¼«·“Ó¦Ź½ĪŖ£ŗÕż¼« FePO4+Li++e£==LiFePO4 ,øŗ¼« Li£e£== Li+ .ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ””””””””””””””””””””””””””””””””””””””””””””””””””””””
A£®³äµēŹ±µē³Ų×Ü·“Ó¦ĪŖFePO4+Li= LiFePO4
B£®·ÅµēŹ±£¬ŌŚÕż¼«ÉĻŹĒLi+µĆµē×Ó±»»¹Ō£¬Ćæ×ŖŅĘ1molµē×ÓŌņÉś³É1mol LiFePO4
C£®·ÅµēŹ±µē³ŲÄŚ²æLi+Ļņøŗ¼«ŅĘ¶Æ£¬µē×ÓÖ»ÄÜĶعżĶāµēĀ·ÓÉøŗ¼«µ½Õż¼«””””””””
 D£®³äµēŹ±¶ÆĮ¦µē³ŲÉĻ±ź×¢”°+”±µÄµē¼«Ó¦ÓėĶā½ÓµēŌ“µÄÕż¼«ĻąĮ¬
D£®³äµēŹ±¶ÆĮ¦µē³ŲÉĻ±ź×¢”°+”±µÄµē¼«Ó¦ÓėĶā½ÓµēŌ“µÄÕż¼«ĻąĮ¬
8£®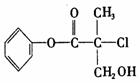 ijӊ»śĪļ(ČēÓŅĶ¼)ŹĒÅ©Ņ©Éś²śÖŠµÄŅ»ÖÖÖŠ¼äĢ壬Ęä½į¹¹¼ņŹ½ČēĻĀ”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(”””” )
ijӊ»śĪļ(ČēÓŅĶ¼)ŹĒÅ©Ņ©Éś²śÖŠµÄŅ»ÖÖÖŠ¼äĢ壬Ęä½į¹¹¼ņŹ½ČēĻĀ”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(”””” )
A£®øĆÓŠ»śĪļŹōÓŚ·¼ĻćĢž
B£®øĆÓŠ»śĪļæÉŅŌŗĶBr2µÄCCl4ČÜŅŗ·¢Éś¼Ó³É·“Ó¦
C£®øĆÓŠ»śĪļŗĶÅØĮņĖį»ģŗĻ¼ÓČČ£¬æÉÄÜ·¢ÉśĻūČ„·“Ó¦
D£®1moløĆÓŠ»śĪļŗĶ×ćĮæµÄNaOHČÜŅŗ·“Ó¦£¬×ī¶ąæÉÓė3mol NaOH·“Ó¦
7£®ĻĀĶ¼ŹĒµē½āCuCl2ČÜŅŗµÄ×°ÖĆ£¬c”¢dĪŖŹÆÄ«µē¼«£¬ĻĀĮŠÓŠ¹ŲµÄÅŠ¶ĻÕżČ·µÄŹĒ(”””” )
 A£®µē½ā¹ż³ĢÖŠ£¬dµē¼«ÖŹĮæŌö¼Ó
A£®µē½ā¹ż³ĢÖŠ£¬dµē¼«ÖŹĮæŌö¼Ó
B£®aĪŖŃō¼«”¢bĪŖŅõ¼«
C£®aĪŖøŗ¼«”¢bĪŖÕż¼«
D£®µē½ā¹ż³ĢÖŠ£¬ĀČĄė×ÓÅØ¶Č»ł±¾²»±ä
6£®ClO2ŹĒŅ»ÖÖɱ¾śĻū¶¾Š§ĀŹøßµÄĖ®“¦Ąķ¼Į£¬ŹµŃéŹŅæÉĶعżŅŌĻĀ·“Ó¦ÖĘµĆ£ŗ
2KClO3+H2C2O4+H2SO4£½2ClO2”ü+K2SO4+2CO2”ü+2H2O”£ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ(”””” )
A£®ClO2ŹĒ»¹Ō²śĪļ”””””””””””””””” B£®1mol KClO3²Ī¼Ó·“Ó¦£¬Ź§Č„µē×ÓĪŖ1mol
C£®H2C2O4ŌŚ·“Ó¦ÖŠ±»Ńõ»Æ”””””””””” D£®H2C2O4µÄ»¹ŌŠŌ“óÓŚClO2µÄ»¹ŌŠŌ
5£®Ä³ĪĀ¶ČĻĀ£¬ŌŚĆܱÕČŻ»ż²»±äµÄČŻĘ÷ÖŠ·¢ÉśČēĻĀ·“Ó¦£ŗ2M(g)+N(g) 2E(g)£¬æŖŹ¼³äČė2 mol E(g)£¬“ļĘ½ŗāŹ±£¬»ģŗĻĘųĢåµÄŃ¹Ēæ±ČĘšŹ¼Ź±Ōö“óĮĖ20%£»ČōæŖŹ¼Ź±Ö»³äČė2 mol MŗĶ1 mol NµÄ»ģŗĻĘųĢ壬“ļĘ½ŗāŹ±MµÄ×Ŗ»ÆĀŹĪŖ(”””” )
2E(g)£¬æŖŹ¼³äČė2 mol E(g)£¬“ļĘ½ŗāŹ±£¬»ģŗĻĘųĢåµÄŃ¹Ēæ±ČĘšŹ¼Ź±Ōö“óĮĖ20%£»ČōæŖŹ¼Ź±Ö»³äČė2 mol MŗĶ1 mol NµÄ»ģŗĻĘųĢ壬“ļĘ½ŗāŹ±MµÄ×Ŗ»ÆĀŹĪŖ(”””” )
A£®20%”””””””””” B£®40%”””””””””” C£®80%”””””””””””” D£®60%
4£®ĻĀĮŠĪļÖŹ½öÓĆĖ®²»Äܼų±šµÄŹĒ(”””” )
A£®ŅŅ“¼”¢±½”¢ĖÄĀČ»ÆĢ¼ČżÖÖŅŗĢå”””””””” B£®ĮņĖįĶ”¢Ģ¼ĖįøĘ”¢µēŹÆČżÖÖ¹ĢĢå
C£®¼×“¼”¢ŅŅČ©”¢äå±½ČżÖÖŅŗĢå”””””””””” D£®ĒāŃõ»ÆÄĘ”¢Ź³ŃĪ”¢ĻõĖįļ§ČżÖÖ·ŪÄ©
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com