
题目列表(包括答案和解析)
1.下列说法中,不正确的是
A.双原子分子中的共价键,一定是非极性键
B.非极性键也可能存在于离子化合物中
C.分子间作用力,又叫范德华力,它比化学键要弱得多
D.共价化合物在液态时不能导电
15.对于反应2SO2+O2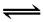 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
|
编号 |
改变的条件 |
生成SO3的速率 |
|
① |
升高温度 |
|
|
② |
降低温度 |
|
|
③ |
增大氧气的浓度 |
|
|
④ |
使用催化剂 |
|
|
⑤ |
压缩体积 |
|
|
⑥ |
恒容下充入Ne |
|
2010年高考总复习化学培优补差训练(13)
14.氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图所示, 已知这个反应速率随着溶液中c(H+)增大而加快。
已知这个反应速率随着溶液中c(H+)增大而加快。
(1)反应开始进行时,反应速率加快的原因是(要求写出化学方程式)
;
(2)反应后期,反应速率下降的原因是
。
13.某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学方程式为
(2)反应开始至2min、5minZ的平均反应速率为 、 ;
(3)5min后Z的生成速率比5min末Z的生成速率 (大、小、相等)。

12.在一定条件下,使NO和O2在一密闭容器中进行反应,下列说法不正确的
A.反应开始时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,最后为零
C.随着反应的进行,逆反应速率逐渐增大,最后不变
D.随着反应的进行,正反应速率逐渐减小,最后不变
11.已知某反应的各物质浓度数据如下:aA(气)十bB(气) cC(气)
cC(气)
起始浓度(mol/L) 3.2 0.8 0.0
2s末浓度(mol/L) 2.0 0.4 0.8
由此可推算出上述方程式中各物质前面的化学计量数之比是
A.1∶2∶4 B.4∶1∶2 C.3∶1∶2 D.3∶2∶1
10.下列情况下,反应速率相同的是
A.等体积0.1 mol/L HCl和0.05 mol/L H2SO4分别与0.2 mol/L NaOH溶液反应
B.等质量锌粒和锌粉分别与等量1 mol/L HCl反应
C.等体积等浓度HCl和HNO3分别与等质量的Na2CO3粉末反应
D.等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等量等表面积等品质石灰石反应
9.下列实验中,反应速率加快是由催化剂引起的是
A、在炭粉中加入KCl03,点燃时燃烧更为剧烈
B、H2O2中加入少量MnO2,即可迅速放出气体
C、将炭块粉碎成粉末状,可使燃烧更加充分
D、电解水时,加少量硫酸可使电解速率加快
8.反应4 (气)+5
(气)+5 (气)
(气) 4NO(气)+6
4NO(气)+6 (气)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率
(气)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率 (X)(反应物的消耗速率或产物的生成速率)可表示为
(X)(反应物的消耗速率或产物的生成速率)可表示为
A、 (NH3)=0.0100mol.L-1.s-1 B、
(NH3)=0.0100mol.L-1.s-1 B、 (O2)=0.0010mol.L-1.S-1
C、
(O2)=0.0010mol.L-1.S-1
C、 (NO)=0.0010mol.L-1.s-1
D、
(NO)=0.0010mol.L-1.s-1
D、 (H2O)=0.045mol.L-1.s-1
(H2O)=0.045mol.L-1.s-1
7.用铁片和硫酸反应制取氢气时,下列措施中,不能使氢气生成速率加快的是
A、加热 B、不用稀硫酸,改用98%的浓硫酸
C、滴加少量硫酸铜溶液 D、不用铁片,改用铁粉
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com