
题目列表(包括答案和解析)
5.在a LAl2(SO4)3和(NH4)2SO4的混合溶液中加入b mol的BaCl2,恰好使溶液中的SO42-完全沉淀;如加入足量强碱并加热可得到c molNH3,则原溶液中的Al3+的浓度(mol/L)为 [C]
A. B.
B.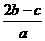 C.
C. D.
D.
4. 将足量的铝粉分别投入等物质的量浓度的NaOH溶液和盐酸中,待反应结束后,两者产生的气体在相同状况下占有相同的体积。下列叙述不正确的是 [BD]
A.消耗铝的质量相等
B.NaOH溶液和盐酸的体积相等
C.两反应中转移的电子数相等
D.反应后两溶液混合会产生白色沉淀且溶液中的溶质只有NaCl
3. 化学在生产和日常生活中有着重要的应用。下列说法不正确的是 [D]
A. 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B. 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C. MgO的熔点很高,可用于制作耐高温材料
D. 电解MgCl2饱和溶液,可制得金属镁
1.将总物质的量为n mol的钠和铝(其中钠的物质的量分数为x),投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V L。下列关系式中正确的是[D]
A.x=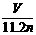 B.0<x≤0.5
B.0<x≤0.5
C.V=33.6n(1-x) D.11.2n<V≤22.4n
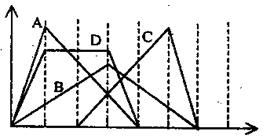 2.下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量。下列反应对应的曲线错误的是[D]
2.下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量。下列反应对应的曲线错误的是[D]
A.向NaAlO2溶液中滴入HCl至过量
B.向澄清石灰水中通入CO2至过量
C.向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量
D.向含有等物质的量的Ca(OH)2、KOH的混合溶液
中通入CO2至沉淀消失
26、联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:
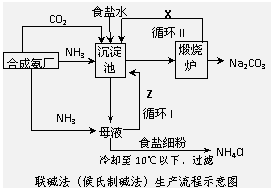

(1)沉淀池中发生反应的化学方程式为_______________________;
(2)X是________,Y是_______(填化学式);
(3)Z中除了溶解的氨气、食盐外,其它溶质还有________________________________;排出液W中的溶质除了氢氧化钙外,还有________________________;
(4)从理论上分析,在氨碱法生产过程中_________(填“需要”、“不需要”)补充氨气,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为 ;
(5)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是_____;
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na+的浓度, 促进碳酸氢钠结晶析出
(6)联碱法中,每当通入NH3 44.8L(已折合成标准状况下)时可以得到纯碱100.0g,则NH3的利用率为______。相比于氨碱法,指出联碱法的一项优点_________________。
答案 1)NaCl + NH3 + CO2 +H2O → NaHCO3↓+ NH4Cl(1分);
(2)CO2(1分),NH3(1分); (3)Na2CO3、NH4Cl(1分), CaCl2、NaCl(1分)
(4)不需要(1分) CaCO3 +2NaCl → Na2CO3 + CaCl2(1分)
(5)b;(1分)
(6)94.3% (1分) 不产生无用的CaCl2(或提高了食盐的转化率等等) (1分)
25. 取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的CO2后,再分别稀释到100 mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的CO2体积(标准状况)与所加盐酸的体积关系如图所示,下列说法正确的是[AC]
取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的CO2后,再分别稀释到100 mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的CO2体积(标准状况)与所加盐酸的体积关系如图所示,下列说法正确的是[AC]
A.原NaOH溶液的物质的量浓度0.15mol/L
B.A曲线表明原溶液通入CO2后,所得溶质为NaOH和Na2CO3,此时用酚酞作指示剂,溶液颜色变化时消耗盐酸的体积为75mL
C.B曲线表明原溶液通入CO2后,所得溶质为Na2CO3和NaHCO3且物质的量之比为1:1
D.B曲线表明原溶液通入CO2后,所得溶质与盐酸反应产生的最大体积为33.6 mL(标准状况)
24.向盛有无水乙醇的烧杯中投入一小块金属钠,可以观察到的现象是[B]
A.钠块在乙醇液面上四处快速游动钠块
B.开始时钠块沉在乙醇液面下
C.熔成小球
D.钠块表面有大量气泡迅速产生,比水反应剧烈
23. 我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O NH4HCO3 ; NH4HCO3+NaCl NaHCO3↓+NH4Cl ;2NaHCO3 Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填字母标号)。
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
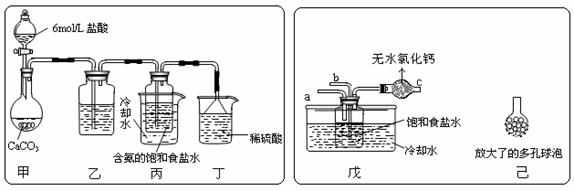
试回答下列有关问题:
 (Ⅰ)乙装置中的试剂是 ;
(Ⅰ)乙装置中的试剂是 ;
(Ⅱ)丁装置中稀硫酸的作用是 ;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称)。
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从 管通入 气体,再从 管中通入 气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是 ;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法:
答案(1)c (1分) (2)①(Ⅰ)饱和碳酸氢钠溶液; (Ⅱ)吸收未反应的NH3(答“防止倒吸”或“吸收CO2”不给分));(Ⅲ)过滤 (每空1分,共3分)
②(Ⅰ)a、NH3, b、CO2; (每空1分,共4分)
(Ⅱ)增大气体与溶液接触面积,提高CO2吸收率; (2分)
(3)用碳酸氢铵与适量饱和食盐水反应。(或往烧碱溶液中通入过量CO2 ;往饱和Na2CO3 溶液中通入过量CO2 等。其他合理方法均可) (2分)
22.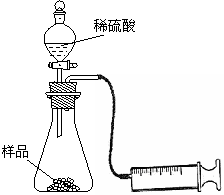 某学校化学科研小组从文献资料上获得如下信息:NaHCO3在潮湿的空气中会缓慢分解成Na2CO3、H2O和CO2。为了验证这一信息,该科研小组将一瓶在潮湿空气中久置的NaHCO3样品混合均匀后,进行如下实验:
某学校化学科研小组从文献资料上获得如下信息:NaHCO3在潮湿的空气中会缓慢分解成Na2CO3、H2O和CO2。为了验证这一信息,该科研小组将一瓶在潮湿空气中久置的NaHCO3样品混合均匀后,进行如下实验:
(1)在一个质量为ag的蒸发皿中加入一些样品,称得总质量为bg。用酒精灯对其充分加热,冷却后称得其总质量为cg。残留在蒸发皿中的固体是(填化学式)_________。
(2)另称取相同质量的样品放入锥形瓶中,实验装置如右图所示。为了保证实验成功,所选用针筒的最大刻度值应大于或等于_________(mL)。(设实验在标准状况下进行)
(3)打开活塞逐滴加入稀硫酸,至没有气泡产生为止。针筒中收集到气体折算成标准状况下的体积为VmL(滴入稀硫酸的体积及针筒活塞的内壁的摩擦力忽略不计)。该科研小组设称取的每份样品中的Na2CO3、NaHCO3的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出了如下算式:x+y=VmL/22400mL·mol-1,他们依据的原理是_________。根据相似原理,请完成下列算式:2x+y=__________。由上述两算式,该科研小组通过计算,得出了样品中的Na2CO3、NaHCO3的质量分数。
答案、(10分)(1)Na2CO3(2分)(2) (2分)
(2分)
(3)原子守恒(2分)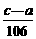 ×2(2分)
×2(2分)
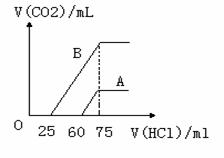
21.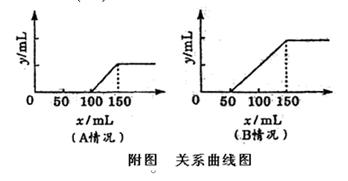 分别取等物质的量浓度的氢氧化钠溶液各100 mL,再通入一定量的CO2,随后分别各取20 mL 溶液,向其中逐滴滴入0.2 mol/L的盐酸,在标准状况下产生CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如附图(分A、B两种情况);
分别取等物质的量浓度的氢氧化钠溶液各100 mL,再通入一定量的CO2,随后分别各取20 mL 溶液,向其中逐滴滴入0.2 mol/L的盐酸,在标准状况下产生CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如附图(分A、B两种情况);
(1)在A情况下,溶质是(填化学式) ,其物质的量之比为
(2)在B情况下,溶质是(填化学式) ,其物质的量之比为
(3)原氢氧化钠溶液的物质的量浓度为
答案.(10分)(1)NaOH、Na2CO3 1:1
(2)Na2CO3、NaHCO3 1:1
(3)1.5 mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com