
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
2°¢◊¯±Í‘≠µ„‘⁄◊ð÷·∫Õ∫·÷·…œÀ˘±Ì 浃 ˝÷µ£ª
1°¢“™∂Ƶ√◊ð÷·°¢∫·÷·À˘±Ì 浃ªØ—ß“‚“£ª
25°¢(8∑÷)𧓵…œ°∞∫Ó œ°±÷∆ºÓ∑®÷∆µ√µƒ¥øºÓ≤˙∆∑÷–≥£∫¨”–…Ÿ¡øµƒNaCl°£Œ™≤‚∂®¥øºÓ≤˙∆∑÷–Na2CO3µƒ∫¨¡ø£¨»°23g—˘∆∑÷√”⁄…’±≠÷–£¨º”ÀÆΩ´∆‰»ÐΩ‚£¨»ª∫Û÷µŒµŒ»Îœ°—ŒÀ·£¨µ±µŒ»Î200gœ°—ŒÀ· ±£¨¡Ω’þ«°∫√ÕÍ»´∑¥”¶£¨…˙≥…µƒ∆¯Ã»´≤ø“ð≥ˆ£¨π≤ ’ºØµΩ8.8gCO2°£
(1)À˘”√œ°—ŒÀ·÷–»Ð÷ µƒ÷ ¡ø∑÷ ˝Œ™____________£ª23g—˘∆∑÷–Na2CO3µƒ÷ ¡øŒ™__________g
(2)∑¥”¶∫Û…’±≠÷–µƒ»Ð“∫Œ™≤ª±•∫ջГ∫£¨ ‘Õ®π˝º∆À„«Û≥ˆ∏√»Ð“∫÷–»Ð÷ µƒ÷ ¡ø°£
24°¢(6∑÷)…ˆ≤°ªº’þ–Ë“™ ≥”√µÕƒ∆—Œµƒ ≥∆∑£¨ƒø«∞ –≥°π©”¶µƒµÕƒ∆—Œ∂ýŒ™∆ªπ˚À·ƒ∆—Œ (C4H5O5Na)°£«Îªÿ¥£∫
(1)∆ªπ˚À·ƒ∆—Œ÷–∏˜‘™Àÿµƒ÷ ¡ø±»Œ™C£∫H£∫O£∫Na=____________________£¨∆ªπ˚À·ƒ∆—Œ÷–ƒ∆‘™Àÿµƒ÷ ¡ø∑÷ ˝Œ™_____________________________°£
°° (2)15.6g∆ªπ˚À·ƒ∆—Œ÷–µƒƒ∆‘™Àÿ÷ ¡ø”Î_________________g ≥—Œ÷–µƒƒ∆‘™Àÿ÷ ¡øœýµ»°£
23°¢(9∑÷)ƒ≥—–æø–‘—ßœ∞–°◊È∂‘°∞SO2ƒÐ∑Ò”ÎH2O∑¥”¶…˙≥…À·°±Ω¯––ÃΩæø°£°°
«Îƒ„≤Œ”ÎÀ˚√«µƒÃΩæøªÓ∂Ø£¨≤¢ªÿ¥”–πÿŒ °£
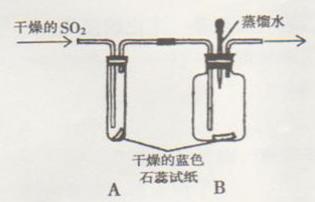
(1)≤È‘ƒ◊ ¡œ£∫¢ŸSO2≥£Œ¬œ¬ «“ª÷÷ŒÞ…´∆¯Ã£¨“◊»Ð”⁄ÀÆ£ª¢⁄À·ƒÐ π¿∂…´ Ø»Ô ‘÷Ω±‰≥…∫Ï…´£ª¢€SO2”–∂æ°£
(2)÷≥ˆºŸ…Ë£∫SO2ƒÐ”ÎH2O∑¥”¶…˙≥…À·°£
(3) µ—ÈÃΩæø£∫…˺∆»Á”“ÕºÀ˘ æ◊∞÷√Ω¯–– µ—È°£
¢Ÿ µ—Èπ˝≥Ã÷–£¨A◊∞÷√ƒ⁄¿∂…´ Ø»Ô ‘÷Ωµƒ—’…´ º÷’√ª”–±‰ªØ°£A◊∞÷√µƒ◊˜”√ «_________________________________°£
¢⁄‘⁄Õ®»ÎSO2÷Æ«∞Ω´B◊∞÷√÷–Ω∫Õ∑µŒπЃ⁄µƒ’Ù¡ÛÀƵŒµΩ¿∂…´ Ø»Ô ‘÷Ω…œ£¨Œ¥º˚ ‘÷Ω—’
…´∑¢…˙±‰ªØ£¨¥À≤Ω≤Ÿ◊˜µƒƒøµƒ «______________________________°£µ±”–SO2Õ®π˝ ±
∑¢œ÷ ™»Ûµƒ¿∂…´ Ø»Ô ‘÷Ω±‰∫Ï£¨¥Àœ÷œÛÀµ√˜___________________________£¨¥Àπ˝≥Ã÷–
∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™____________________________________________________°£
(4)Ω·¬€£∫‘≠ºŸ…Ë≥…¡¢°£
(5)∑¥Àº”Î∆¿º€£∫∏√ µ—È∑Ω∞∏÷–£¨”–“ª∏ˆ√˜œ‘µƒ ˬ©£¨«Îƒ„∞ÔÀ˚√«÷∏≥ˆ≤ª◊„÷Æ¥¶_________°£
(6)Õÿ’πÃΩæø£∫∏√—–æø–‘—ßœ∞–°◊È»°∏’ΩµµΩ¡ÚÀ·≥ß(…˙≤˙π˝≥Ã÷–≤˙…˙SO2)∏ΩΩ¸µƒ”ÍÀÆΩ¯––≤‚∂®£¨√ø∏Ùº∏∑÷÷”≤‚“ª¥ŒpH£¨∆‰ ˝æð»Áœ¬±ÌÀ˘ æ£∫
|
≤‚∂® ±øà |
5£∫05 |
5£∫10 |
5£∫15 |
5£∫20 |
5£∫25 |
5£∫30 |
5£∫35 |
|
pH |
4.95 |
4.94 |
4.94 |
4.88 |
4.86 |
4.85 |
4.85 |
∑÷Œˆ…œ ˆ ˝æ𵃱‰ªØ£¨ƒ„ø…µ√≥ˆµƒΩ·¬€ «_____________________________£ª’Î∂‘¥ÀΩ·¬€£¨ƒ„≤¬≤‚∆‰÷–µƒ‘≠“ÚŒ™___________________________________________________°£Ω·∫œ¥Û¿Ì ØµÒœÒ ÐµΩÀ·”Í∏Ø ¥µƒ ¬ µ£¨ƒ„»œŒ™ÃºÀ·°¢¡ÚÀ·°¢—«¡ÚÀ·(H2SO3)À·–‘”…«øµΩ»ıµƒÀ≥–Ú «__°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
22°¢(12∑÷)œ¬Õº « µ—È “÷–≥£”√µƒº∏÷÷◊∞÷√°£
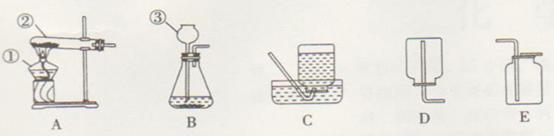
«Îªÿ¥œ¬¡–Œ £∫
(1)–¥≥ˆ”–±ý∫≈“«∆˜µƒ√˚≥∆£∫¢Ÿ___________£¨¢⁄________________£¨¢€_____________°£
(2) µ—È “”√KMnO4÷∆»°O2£¨‘Ú”¶—°”√µƒ∆¯ÃÂ∑¢…˙◊∞÷√ «___________(ÃÓ◊∞÷√–Ú∫≈)£ªº”»Î“©∆∑«∞£¨”¶ ◊œ»____________________________°£
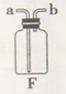 (3) µ—È “÷∆»°CO2∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™________________________________£ª÷∆»°CO2—°”√B◊∞÷√◊˜Œ™∆¯ÃÂ∑¢…˙◊∞÷√µƒ¿Ì”… «¢Ÿ________________________£¨¢⁄________________£ª ’ºØCO2 ±—°”√µƒ◊∞÷√ «________(ÃÓ◊∞÷√–Ú∫≈)°£
(3) µ—È “÷∆»°CO2∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™________________________________£ª÷∆»°CO2—°”√B◊∞÷√◊˜Œ™∆¯ÃÂ∑¢…˙◊∞÷√µƒ¿Ì”… «¢Ÿ________________________£¨¢⁄________________£ª ’ºØCO2 ±—°”√µƒ◊∞÷√ «________(ÃÓ◊∞÷√–Ú∫≈)°£
(4)ƒ≥Õ¨—ß”˚ ’ºØ“ª÷÷ƒ—»Ð–‘∆¯Ã£ƻœŒ™”“ÕºF◊∞÷√ø…“‘¥˙ÃÊC◊∞÷√£¨
«ÎºÚ ˆ∏√Õ¨—ß»Á∫Œ π”√F◊∞÷√ ’ºØ’‚÷÷ƒ—»Ð–‘∆¯ÃÂ
__________________________________________°£
20°¢(5∑÷)«‚—ıªØƒ∆ «“ª÷÷÷ÿ“™µƒªØπ§‘≠¡œ°£
(1)«‚—ıªØƒ∆»Ð“∫≥§∆⁄±©¬∂‘⁄ø’∆¯÷–ª·÷Ω•±‰÷ £¨ºÏ—È«‚—ıªØƒ∆»Ð“∫ «∑Ò±‰÷ µƒ ‘º¡ «______________£¨»Ù“—±‰÷ ‘ÚºÏ—È ±ø…π€≤ÏµΩµƒœ÷œÛ «____________________°£
(2)»Áπ˚“™ π«‚—ıªØƒ∆»Ð“∫µƒpHºı–°£¨ø…≤…»°µƒ∑Ω∑®”–£∫
¢Ÿ≤ª∑¢…˙ªØ—ß∑¥”¶µƒ∑Ω∑®_________________°£
¢⁄”–ªØ—ß∑¥”¶∑¢…˙µƒ∑Ω∑®(“™«Û∏˜÷÷∑Ω∑®÷–À˘—°µƒŒÔ÷ ¿ý±≤ªÕ¨)_________________£ª_______________________°£
2l°¢(9∑÷)A°¢B°¢C°¢D°¢E°¢F°¢H°¢I°¢MŒ™≥ı÷–ªØ—ß≥£º˚µƒŒÔ÷ £¨«“”–œ¬ÕºÀ˘ 浃◊™ªØπÿœµ°£“—÷™A°¢B∫¨”–œýÕ¨µƒ‘™Àÿ£¨B°¢D°¢H°¢MŒ™—ıªØŒÔ£¨C°¢EŒ™µ•÷ £¨∑¥”¶¢⁄ « µ—È “ºÏ—È∆¯ÃÂHµƒ∑¥”¶°£«Îªÿ¥£∫
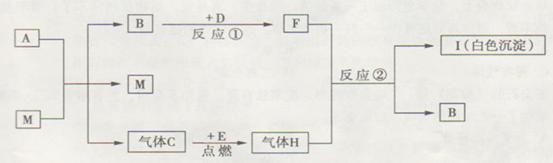
(1)A°¢MµƒªØ—ß Ω∑÷± «_________°¢__________£ªMµƒ◊˜”√ «_______________°£
(2)–¥≥ˆ∑¥”¶¢Ÿ°¢¢⁄µƒªØ—ß∑Ω≥Ã Ω£∫
∑¥”¶¢Ÿ____________________________£ª∑¥”¶¢⁄_______________________________°£
(3) µ—È “ºÏ—ȺØ∆¯∆øƒ⁄∆¯ÃÂCµƒ∑Ω∑® «____________________________________°£
19°¢(4∑÷)Œ“π˙±±∑Ω”––Ì∂ý—Œ∫˛£¨∫˛ÀÆ÷–»Ð”–¥Û¡øµƒNa2CO3∫ÕNaCl£¨ƒ«¿Ôµƒ»À√«∂¨ÃϿúÓ(Na2CO3)£¨œƒÃÏ…π—Œ(NaCl)°£Na2CO3∫ÕNaClµƒ»ÐΩ‚∂»«˙œþ»Áœ¬ÕºÀ˘ 棨æðÕºªÿ¥œ¬¡–Œ £∫
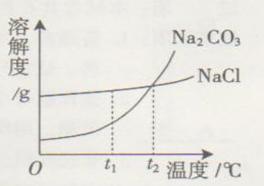
(1)t1°Ê ±£¨»ÐΩ‚∂»Ωœ¥ÛµƒŒÔ÷ «__________________°£
(2)µ»÷ ¡øNa2CO3°¢NaCl±•∫ջГ∫∑÷±¥”t2°ÊΩµŒ¬µΩt1°Ê£¨Œˆ≥ˆæßÃÂΩœ∂ýµƒ «________°£
(3)∂¨ÃϿúӵƒ‘≠“Ú «”…”⁄Na2CO3µƒ»ÐΩ‚∂»ÀÊŒ¬∂»ΩµµÕ∂¯_____________ (ÃÓ°∞‘ˆ¥Û°±°¢°∞ºı–°°±ªÚ°∞≤ª±‰°±)°£
(4)œƒÃÏ…π—Œ «¿˚”√_________________(ÃÓ–Ú∫≈)µƒ∑Ω∑®£¨ πNaClæßÃÂŒˆ≥ˆ°£
¢Ÿ…˝∏þŒ¬∂»£¨ πNaCl»ÐΩ‚∂»‘ˆ¥Û°°°°°°°°°°°° °°¢⁄∑Á¥µ»’…π£Æ π»Ðº¡’Ù∑¢
18°¢(5∑÷)‘⁄»’≥£…˙ªÓ÷–”¶◊¢“‚∫œ¿Ì…„»°”™—¯ŒÔ÷ ∫Õ»Àñÿ–˵ƒ‘™Àÿ°£
(1) þ≤À÷–À˘∫¨µƒ”™—¯Àÿ÷˜“™ «_____________________°£
(2)µ∞∞◊÷ «ππ≥……˙√¸µƒª˘¥°ŒÔ÷ °£ «»’≥£…≈ ≥µƒ÷ÿ“™◊È≥…≤ø∑÷°£œ¬¡– ≥ŒÔ÷–∏ª∫¨µ∞∞◊÷ µƒ «______________________(ÃÓ–Ú∫≈)°£
¢Ÿ∆œÃ—∏…°°°°°°°°°° ¢⁄∆ªπ˚°°°°°°°° ¢€¥Û∂π°°°°°° ¢Ð≈£ƒÃ°°°°°°°°°° ¢ð√◊∑π
(3)ë¿ý «»ÀÃÂÀ˘–Ë_____________________µƒ÷˜“™¿¥‘¥°£
(4)ƒø«∞ –≥°…œ”–“ª÷÷Ω–µ‚À·∏∆µƒ±£Ω°∆∑£¨∆‰∫¨”–»Àñÿ–˵ƒŒ¢¡ø‘™Àÿ «____________°£
17°¢(6∑÷)±±æ©2008ƒÍ∞¬‘Àª·÷˜Ã”˝≥°°∞ƒÒ≥≤°±£¨±ª°∂éŒÓ ø±®°∑∆¿Œ™»´«Ú°∞◊Ó«ø∫∑°±π§≥ð£Ω®‘Ï°∞ƒÒ≥≤°± π”√¡À¥Û¡øµƒ∏÷Ã˙°£
(1)∏÷Ã˙ Ù”⁄____________(ÃÓ°∞¥ø檌԰±ªÚ°∞ªÏ∫œŒÔ°±)°£
(2)Œ™¡À∑¿÷π∏÷Ã˙–‚ ¥£¨»À√«≥£≤…”√‘⁄∆‰±Ì√Ê_____________ªÚ∂∆…œ∆‰À˚Ω Ùµ»∏≤∏«±£ª§ƒ§µƒ∑Ω∑®°£’‚–©∑Ω∑®∂ºƒÐπª∑¿÷π–‚ ¥µƒπ≤Õ¨‘≠¿Ì «_______________________°£
(3)∞—≥ýÃ˙øÛ(÷˜“™≥…∑÷ «Fe2O3)“±¡∂≥…Ã˙µƒ÷˜“™∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™_______________°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com