
题目列表(包括答案和解析)
7. (天津市2008年中考化学题)
将10g某物质溶解于90g水中形成溶液,所得的溶液中溶质质量分数是 ( )
A一定等于10% B.一定大于10%
C.一定小于10% D.三种情况均有可能
6.(2008年甸南中考试题)
20℃时,氯化钠的溶解度是36克。把20g氯化钠中加入 50g水,充分溶解后,溶液中溶质的质量分数为 ( )
A.36% B.40% C.26.5% D.28.6%
5、(2008年黄冈市九年级化学中考试题)
在4个小烧杯里分别盛有等质量的下列物质,在空气中放置一段时间后,烧杯内物质的总质量显著增加且溶质质量分数减小的是 ( )
A浓盐酸 B浓硫酸 C石灰水 D蔗糖溶液
4.(常州市2008年中考化学试题)下列物质分别和等质量、等质量分数的硫酸恰好完全反应后,所得溶液中溶质质量分数最大的是 ( )
A.Zn B.Zn(OH)2 C.ZnO D.ZnCO3
3.(南阳市2008年中考试题)
由Mg(OH)2和MgO组成的混合物,测得其中含镁元素的质量分数为48%。取该混合物10g,将其投入110g的稀硫酸中恰好完全反应,所得溶液中溶质的质量分数为 ( )
A.12% B.24% C.20% D.30%
1.(安丘市2008年中考化学试题)
某同学在配制50g溶质量分数为5%的食盐溶液的实验中,称量时将砝码放在左盘(1g以下用游码),食盐放在右盘;量水时仰视液面读数。这样配制的食盐溶液中的质量分数
( )
A.等于5% B.大于5%
C.小于5% D.不能确定
例1.下列说法中不正确的是( )
①溶液都是无色透明、均一、稳定的混合物。②同种溶质的饱和溶液一定比它的不饱和溶液浓。③糖水是溶液,盐水是溶液,混合在一起,既有糖又有盐,就不是溶液了。④在某种溶质的饱和溶液中再加入这种溶质,溶液的质量随之增大。⑤一杯调好的糖水,喝第一口特别甜,越喝越不甜,说明后来喝的糖水要变稀些。⑥把饱和溶液温度升高时,若溶液质量不变,则溶液质量也不变。
A.②④⑤⑥ B.①③④⑤ C.①②③④⑤ D.①②③⑤⑥
[解析]此题是有关溶液、饱和溶液概念的判断。溶液不一定无色,故①错。溶液的饱和与否与温度有关,②没有指明温度也不正确。溶液中的溶质可以是一种也可以是多种,故③ 不对。饱和溶液在同条件下不再溶解同种溶质,故④不正确。溶液是均一的,这只是味觉的迟钝造成的错误,故⑤也不正确。⑥正确。
例2.欲将某温度下接近饱和的硝酸钾溶液变成饱和溶液,不能采取的措施是( )
A.加入硝酸钾晶体 B.蒸发一定量水
C.给溶液加热 D.给溶液降温
[解析]本题关键在于充分理解饱和溶液与不饱和溶液的转化条件。因为硝酸钾的溶解度随温度升高而增大。因此降低溶液温度可达到目的。另外,向溶液中加入硝酸钾晶体或蒸发溶剂亦可达到目的。这三种措施单独使用或同时使用都可以。
例3.下图为A、B两种物质的溶解度曲线。回答下列问题:
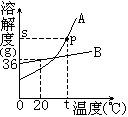 (1)图中P点的含义是____。
(1)图中P点的含义是____。
(2)t℃时,A物质的溶解度___B物质的溶解度(填“大于”、
“小 于”或“等于”)
(3)B物质属于____溶物质(填“易”、“可”、“微”或“难”)
(4)当B中含有少量A时,可用____法提纯B。
[解析]本题主要考查溶解度曲线表示意义,溶解度与溶解性关系
以及结晶法的原理。
例4.某溶液中含有四种离子Na+、Mg2+、Cl-、SO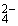 ,其中:Na+、Mg2+、Cl-离子个数比为4:7:6,若Na+离子个数为4a,则SO
,其中:Na+、Mg2+、Cl-离子个数比为4:7:6,若Na+离子个数为4a,则SO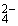 离子个数为____。
离子个数为____。
[解析]解决此类问题的关键是充分理解溶液中电荷守恒原理:所有阳离子带的正电荷总数等于所有阴离子带的负电荷总数。依题意可知:溶液中Mg2+、Cl-的个数分别为7a、6a个。设此时溶液SO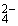 离子数为x,则4a×1+7a×2=6a×1+2x,x=6a。
离子数为x,则4a×1+7a×2=6a×1+2x,x=6a。
14、白色粉末M是由Na2CO3和NaHCO3组成的混合物。取甲、乙、丙三份质量不同的M样品分别跟50克相同的稀盐酸充分反应,得到的气体质量与M的质量关系如下表:
|
实验组别 |
甲 |
乙 |
丙 |
|
稀盐酸质量/克 |
50 |
50 |
50 |
|
加入M的质量/克 |
3.80 |
6.20 |
7.20 |
|
生成气体的质量/克 |
1.76 |
2.62 |
2.62 |
试计算M中Na2CO3和NaHCO3的质量分数各是多少?
13、人吸入空气,排出CO2等气体。为了证明人呼出的气体中含有CO2且能有效排除空气中CO2的干扰,某学生设计了下图所示的实验装置,为了除去空气中的CO2和检验人呼出的气体中含有CO2,则锥形瓶Ⅰ、Ⅱ中加入的试剂为 ( )

|
|
瓶Ⅰ |
瓶Ⅱ |
|
A |
Ca(OH)2 |
NaOH |
|
B |
NaOH |
Ca(OH)2 |
|
C |
石蕊 |
酚酞 |
|
D |
Na2SO4 |
CaCl2 |
12、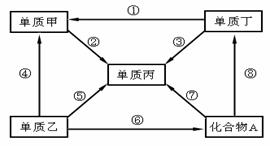 下面是初中化学常见的五种物质之间的转化关 系图(各步反应条件和其他反应物均已略去),甲乙丙丁中有两种金属,其中一种金属在地壳中的元素含量居所有金属的第二位。请回答:
下面是初中化学常见的五种物质之间的转化关 系图(各步反应条件和其他反应物均已略去),甲乙丙丁中有两种金属,其中一种金属在地壳中的元素含量居所有金属的第二位。请回答:
(1)丙、丁分别是 、 。
(2)有单质生成且不属于置换反应的是
(填序号) 。
(3)写出乙 + 水  A + 甲反应的化
A + 甲反应的化
学方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com