
题目列表(包括答案和解析)
3、实验步骤以及注意事项:
(1)先通一段时间的一氧化碳,目的是为了排尽试管中的空气,防止在加热时发生爆炸。
(2)点燃酒精灯,高温加热反应。
(3)当氧化铁被还原后,停止高温加热,继续通入一氧化碳,目的是为了让贴在一氧化碳的环境下冷却,防止高温下的铁再次被空气中的氧气氧化。
(4)当试管冷却后,在停止通入一氧化碳。
(5)尾气处理:由于反应中一氧化碳气体排出,造成空气污染,因此要进行尾气处理。
例:钢铁的冶炼是人类文明的一个重要标志,右图是模拟炼铁的实验装置图。
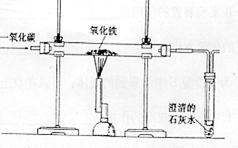 (1)请你写出冶炼生铁的化学方程式
(1)请你写出冶炼生铁的化学方程式
,
(2)请写出一种证明产物中含铁粉的方法:
(3)此装置有不完善的地方,请写出其中一种改进的方法 。
解析:根据题给信息,能够很轻松写出该反应的化学方程式,3CO+Fe2O3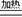 3CO2+2Fe;
3CO2+2Fe;
要想进一步证明产物中含有金属铁,应该根据铁的有关性质来寻找方法,如能被磁铁吸引、能与盐酸反应生成气体、能与硫酸铜溶液反应生成红色的铜等。该装置中最不完善地方就是尾气的处理问题,应该点燃或者用气球收集起来。
答案:(1)3CO+Fe2O3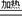 3CO2+2Fe
3CO2+2Fe
(2)用磁铁吸引,或者取出少量加入到酸溶液中,由气泡产生。
(3)用点燃的酒精灯烧掉有毒的尾气或者用气球收集。
2、实验装置(如右图):
1、反应原理:3CO+Fe2O3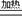 3CO2+2Fe
3CO2+2Fe
3、合金比它的各组成成分金属具有更好的强度和硬度,以及机械加工性能。例如,硬铝(含铜、镁、锰、铝)的硬度和强度都比纯铝大,几乎相当于钢材,而且密度还小。
例:在生产和生活中,大量使用的不是纯金属,而是它们的合金。合金与纯金属比较,其优越的性能有(答出一条即可) ,原因是 。
解析:这道题主要考查了合金的特性以及产生这些特性的原因。根据我们所认识的有关合金的知识可知,合金的特性主要由耐腐蚀性、熔点低、硬度和强度大;造成合金这种特性的主要原因是金属的组成和结构发生了变化。
答案:硬度大(或熔点高或不易被腐蚀等)金属的组成和结构发生了变化
2、一般地说,合金的熔点比它的各组成成分金属的熔点都低。例如,铝硅合金的熔点为564℃,比铝、硅的熔点都低。铋、铅、锡、镉制得的武德合金因为溶点低,可制成电路的保险丝,以及自动灭火和防爆完全装置等。
合金是在金属中加热熔化某些金属或非金属,制得具有金属特性的物质。合金可以是金属与金属、金属与非金属的混合物。但是,制造合金并不是把金属(或非金属)融合在一块,合金的形成是有条件的。金属之间在形成合金时,一般要求一种金属的熔点不能高于另一种金属的沸点,它们必须在某一温度下均能呈熔化状态。
制得的合金的性能是完全不一样的,但是它们一般都具有以下特性:
1、合金比它的各种成分金属具有许多良好的物理的、化学的、机械上的等方面的性能。例如,由铁、铬、镍制得的不锈钢,具有很强的耐腐蚀性能。
2、几种常见金属的特性
铁:铁制品在潮湿的空气中容易生锈,是世界上年产量最高的金属,容易被磁铁吸引。
铜:在潮湿的空气中,表面会生成绿色的铜绿(碱式碳酸铜)
铝:在空气中能形成一层纸你的氧化物薄膜,起到了保护作用,耐强酸的腐蚀。
例:下列有关金属和金属材料的说法不正确的是( )
A铁有良好的导热性,常用来制作炊具 B铜的化学性质不活泼,在潮湿的空气中不会生锈
C.废旧电池中汞的回收可减少对环境的污染 D.铝表面易形成致密的氧化膜可阻止铝进一步被氧化
解析:铁做炊具是利用了它的导热性;回收废旧电池,是因为金属汞有剧毒;而铝的氧化膜起到了保护作用。铜在潮湿的空气中会与氧气、二氧化碳、水共同作用生成碱式碳酸铜[Cu2(OH)2CO3]。因此,B中的说法是错误的。
答案:B。
1、金属的物理性质及其应用:
|
金属的物理性质 |
体现金属物理性质的应用 |
|
具有金属光泽 |
贵重金属可做装饰品 |
|
机械强度大 |
可制作多种工具等 |
|
延展性好 |
汽车外壳、钢丝绳等 |
|
导电性好 |
做电线、电缆 |
|
导热性好 |
铁锅、铝铲等 |
27、(9分)小明在探究CO2和NaOH是否发生反应时,设计出下列三种装置进行实验:
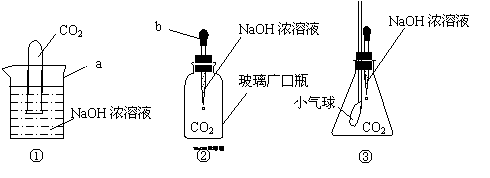
请回答以下几个问题:
(1)写出上图中标有字母的仪器名称:a ,b 。
(2)以上三个实验中,①③有明显现象,请你帮小明记录他观察到的实验现象:
实验① 。实验③ 。
(3)实验②因选用仪器不当导致未能观察到明显现象,请你帮小明寻找一种物品替代该装置中的广口瓶,以使实验取得成功,你将选用的物品是 ,改进后能看到的实验现象是 。
(4)请你进一步设计实验来检验CO2和NaOH溶液反应生成了Na2CO3,并将有关的实验操作、现象、结论填入下表:
|
实验操作 |
实验现象 |
结 论 |
|
|
|
|
26、(14分)现有下图所示的实验装置:
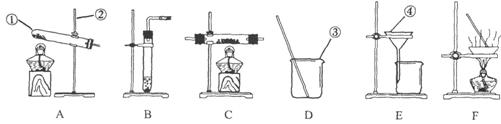
(1)(4分)写出图中指定仪器的名称:① ;② ;③ ;④ 。
(2)(2分)A装置可用于(填一个具体实验名称,下同) 的实验。B装置可用于 的实验。
(3)(6分)现有稀H2SO4、CuO、Fe粉3种物质,请设计两种制取铜的实验方案。填写下表。
|
实验方案 |
有关反应的化学方程式 |
选用装置(填字母代号) |
|
方案一 |
① ② |
|
|
方案二 |
① ② |
|
(4)(2分)用水、生石灰、碳酸钠制取固体NaOH,应选用装置(填字母代号) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com