
题目列表(包括答案和解析)
 工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.
工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.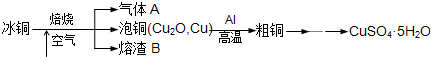
| ||
| ||
| 滴定剂 |
| 5bc |
| 4a |
| 5bc |
| 4a |
工业上冶炼冰铜(mCu2O·nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体。
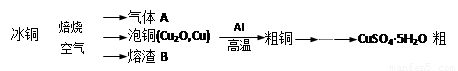
完成下列填空:
(1)气体A中的大气污染物可选用下列试剂中的 (填序号)吸收。
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d. 氨水
(2)用稀H2SO4 浸泡熔渣B,取少量所得溶液,滴加 (填物质名称)溶液后呈红色,说明溶液中存在Fe3+,检验溶液中还存在Fe2+的方法是 (注明试剂、现象)。
|

(3)泡铜冶炼粗铜的化学方程式是 。
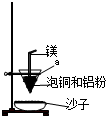
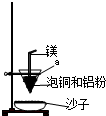
(4)装置中镁带的作用是 。泡铜和铝粉混合物表面覆盖少量白色固体a,
a是 (填名称)。沙子能否换成水? (填“能”或“不能”)。
(5)用滴定法测定CuSO4·5H2O的含量。取a g试样配成100 mL溶液,取20.00mL用c mol /L 滴定剂(H2Y2–,滴定剂不与杂质反应)滴定至终点,消耗滴定剂bmL,滴定反应:Cu2+ + H2Y2–=CuY2–+ 2H+。则CuSO4·5H2O质量分数的表达式是 。
(6)下列操作会导致CuSO4·5H2O含量的测定结果偏高的是_____________。
a.滴定临近终点时,用洗瓶中的蒸馏水洗下滴定管尖嘴口的半滴标准液至锥形瓶中
b.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00mL进行滴定
c.滴定前,滴定管尖端有气泡,滴定后气泡消失
工业上冶炼冰铜(mCu2O·nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体。
完成下列填空:
(1)气体A中的大气污染物可选用下列试剂中的 (填序号)吸收。
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d. 氨水
(2)用稀H2SO4 浸泡熔渣B,取少量所得溶液,滴加 (填物质名称)溶液后呈红色,说明溶液中存在Fe3+,检验溶液中还存在Fe2+的方法是 (注明试剂、现象)。
|

 工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.
工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.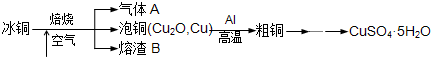
 ?CuY2-+2H+.则CuSO4?5H2O质量分数的表达式是______.
?CuY2-+2H+.则CuSO4?5H2O质量分数的表达式是______.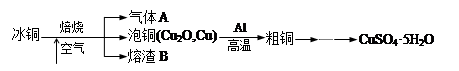
|

第Ⅰ卷 (共66分)
一、(本题共10分)
1.B 2.A 3.D 4.C 5.D
二、(本题共36分)
6.A 7.C 8.D 9.B 10.B 11.D 12.C 13.A 14.B 15.D 16.C 17.B
三、(本题共20分)
18.A、B 19.C、D 20.A、B 21.C 22.A、D
四、(本题共24分)
23.(本题共8分)
(1)氢(1分)
(2)第二周期、ⅣA(1分)1s22s22p63s23p5(各1分)
(3)Cl(1分)
(4)B、C(2分)
(5)B、D(2分)
24.(本题共8分)
(1)+2Sn,Fe2(SO4)3(各1分)
 (2)SnCl2→SnCl4(各1分)
(2)SnCl2→SnCl4(各1分)
(3)
(4)2:1(2分)
25.(本题共8分)
(2)放热(1分)
(3)逆 增大 增大 不变(各1分)
(4)B、C(2分)
五、(本题共24分)
26.(本题共14分)
(1)储液瓶(B瓶)内导管中液面会上升,观察上升液面在1分钟内明显下降(2分)
(2)品红(1分)Mg+2H+→Mg2++H2↑(2分)
(3)① 106.5(1分) ② 25.5(2分) ③ 4.08%(1分) ④ C(1分)
(4)① ②(2分) 0.243(106.5―VB)(1―a%)(2分)
27.(本题共10分)
(1)A、C(2分)
(2)除去AlO2杂质(1分)
(3)2CrO42-+2H+→Cr2O72-+H2O(2分)
(4)① 将混合物放入烧杯中,加水,充分搅拌直到固体不再溶解。(2分)
② 蒸发(1分) ④ 冷却,结晶(2分)
六、(本题共20分)
28.(本题共9分)
(1)醛基(酚)羟基 醚键(2分)
(2)(a)取代反应(1分)
 |
(b)
(3) (1分+1分+2分)
29.(本题共11分)
(1)羧基(1分) 氧化反应(1分)
 CH3CHO+2Cu(OH)
2 CH3COOH+Cu2O↓+2H2O(2分)
CH3CHO+2Cu(OH)
2 CH3COOH+Cu2O↓+2H2O(2分)
 |
(3)
 |
(2分)
(4)四(2分); (1分)
七、(本题共16分)
30.(本题共7分)
(2)0.43(或43%)(2分)
31.(本题共9分)
(1)NaOH 1.50×10-3mol Na2CO3 5.00×10-4mol(2分)
(2)8.00mL(2分)
(3)0.201mg CO2/(g?h)(3分)
本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com