
2.各种放射线的性质比较
|
种类 |
本质 |
质量(u) |
电荷(e) |
速度(c) |
电离性 |
贯穿性 |
|
α射线 |
氦核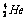 |
4 |
+2 |
0.1 |
最强 |
最弱,纸能挡住 |
|
β射线 |
电子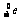 |
1/1840 |
-1 |
0.99 |
较强 |
较强,穿几mm铝板 |
|
γ射线 |
光子 |
0 |
0 |
1 |
最弱 |
最强,穿几cm铅版 |
放射性元素衰变时,通常会同时放出α、β和γ三种射线,即α、β衰变核反应同时放出γ射线(释放能量)。在某些特殊情况下,某些放射性元素只放出α或只放出β射线。但任何情况下都不会只放出γ射线,γ射线只能伴随α或β射线放出。
三种射线在匀强磁场、匀强电场、正交电场和磁场中的偏转情况比较:
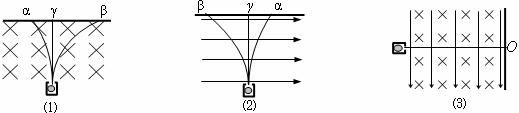 如(1)、(2)图所示,在匀强磁场和匀强电场中都是β比α的偏转大,γ不偏转;两图区别是:在磁场中偏转轨迹是圆弧,在电场中偏转轨迹是抛物线。(3)图中γ肯定打在O点;如果α也打在O点,则β必打在O点下方;如果β也打在O点,则α必打在O点下方。
如(1)、(2)图所示,在匀强磁场和匀强电场中都是β比α的偏转大,γ不偏转;两图区别是:在磁场中偏转轨迹是圆弧,在电场中偏转轨迹是抛物线。(3)图中γ肯定打在O点;如果α也打在O点,则β必打在O点下方;如果β也打在O点,则α必打在O点下方。
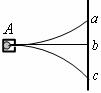 [例题3]如图所示,铅盒A中装有天然放射性物质,放射线从其右端小孔中水平向右射出,在小孔和荧光屏之间有垂直于纸面向里的匀强磁场,则下列说法中正确的有
[例题3]如图所示,铅盒A中装有天然放射性物质,放射线从其右端小孔中水平向右射出,在小孔和荧光屏之间有垂直于纸面向里的匀强磁场,则下列说法中正确的有
A.打在图中A、b、c三点的依次是α射线、γ射线和β射线
B.α射线和β射线的轨迹是抛物线
C.α射线和β射线的轨迹是圆弧
D.如果在铅盒和荧光屏间再加一竖直向下的匀强电场,则屏上的亮斑可能只剩下b
解:由左手定则可知粒子向右射出后,在匀强磁场中α粒子受的洛伦兹力向上,β粒子受的洛伦兹力向下,轨迹都是圆弧。由于α粒子速度约是光速的1/10,而β粒子速度接近光速,所以在同样的混合场中不可能都做直线运动(如果一个打在b,则另一个必然打在b点下方。)本题选AC。
[例题4]如图所示,是利用放射线自动控制铝板厚度的装置。假如放射源能放射出α、β、γ三种射线,而根据设计,该生产线压制的是3mm厚的铝板,那么是三种射线中的____射线对控制厚度起主要作用。当探测接收器单位时间内接收到的放射性粒子的个数超过标准值时,将会通过自动装置将M、N两个轧辊间的距离调___一些。
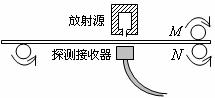 解:α射线不能穿过3mm厚的铝板,γ射线又很容易穿过3mm厚的铝板,基本不受铝板厚度的影响。而β射线刚好能穿透几毫米厚的铝板,因此厚度的微小变化会使穿过铝板的β射线的强度发生较明显变化,即是β射线对控制厚度起主要作用。若超过标准值,说明铝板太薄了,应该将两个轧辊间的距离调节得大些。
解:α射线不能穿过3mm厚的铝板,γ射线又很容易穿过3mm厚的铝板,基本不受铝板厚度的影响。而β射线刚好能穿透几毫米厚的铝板,因此厚度的微小变化会使穿过铝板的β射线的强度发生较明显变化,即是β射线对控制厚度起主要作用。若超过标准值,说明铝板太薄了,应该将两个轧辊间的距离调节得大些。
1.天然放射现象
1896年法国人贝克勒尔首先发现了铀的放射性现象。随后居里夫妇发现了有更强放射性的元素钋和镭。天然放射现象的发现,说明原子核是可分的。因为知道了三种射线的本质后,通过思考分析即能断定:α粒子的质量、电性与电量与原子核外电子大不相同;β射线中的电子能量远大于核外电子的能量;γ射线能量也大于核外层电子受激辐射的X射线能量。所以三种射线是由原子核发出的。
4.光谱和光谱分析
(1)炽热的固体、液体和高压气体发出的光形成连续光谱。
(2)稀薄气体发光形成线状谱(又叫明线光谱、原子光谱)。
根据玻尔理论,不同原子的结构不同,能级不同,可能辐射的光子就有不同的波长。所以每种原子都有自己特定的线状谱,因此这些谱线也叫元素的特征谱线。
根据光谱鉴别物质和确定它的化学组成,这种方法叫做光谱分析。这种方法的优点是非常灵敏而且迅速。只要某种元素在物质中的含量达到10-10g,就可以从光谱中发现它的特征谱线。
3.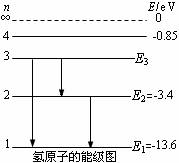 玻尔模型(引入量子理论,量子化就是不连续性,整数n叫量子数。)
玻尔模型(引入量子理论,量子化就是不连续性,整数n叫量子数。)
1913年丹麦人玻尔提出“玻尔原子理论”,20世纪20年代,海森堡等科学家提出“量子力学的原子理论”。
(1)玻尔的三条假设(量子化)
①轨道量子化rn=n2r1r1=0.53×10-10m
②能量量子化: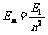 E1=-13.6eV
E1=-13.6eV
③原子在两个能级间跃迁时辐射或吸收光子的能量hν=Em-En
(2)从高能级向低能级跃迁时释放出光子;从低能级向高能级跃迁时可能是吸收光子,也可能是由于碰撞(用加热的方法,使分子热运动加剧;分子间的相互碰撞可以传递能量)。原子从低能级向高能级跃迁时只能吸收一定频率的光子;而从某一能级到被电离可以吸收能量大于或等于电离能的任何频率的光子。(如在基态,可以吸收E≥13.6eV的任何光子,所吸收的能量除用于电离外,都转化为电离出去的电子的动能)。
(3)玻尔理论的局限性。由于引进了量子理论(轨道量子化和能量量子化),玻尔理论成功地解释了氢光谱的规律。但由于它保留了过多的经典物理理论(牛顿第二定律、向心力、库仑力等),所以在解释其他原子的光谱上都遇到很大的困难。
[点拔1]原子模型的发现比较:
|
实验基础 |
理论内容与模型 |
成功 |
困难 |
发现电子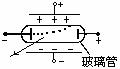 阴极射线(电子)在电场(或磁场)中偏转,射到阴极玻璃管发出荧光。 |
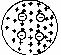 原子中正电荷均匀分布,电子如枣镶嵌在内。 |
可解释一些原子受激发产生原子光谱的事实。 |
|
α粒子散射性现象: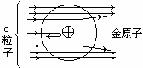 绝大多数过金原子仍向前进,少数发生较大偏转,极少数甚至反弹。 |
(1)原子中心有核,核外有电子绕核旋转。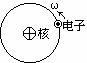 (2)带正电原子核几乎集中原子全部质量,带负电的电子质量很小。(3)核带正电荷数与核外带负电荷数相等。(4)电子绕核旋转的向心力即核对它的为库仑引力。 |
圆满解释α散射,可推算各元素原子核带的正电荷数,可估计出原子核的大小<10-14m(原子半径约10-10m) |
据经典电磁理论,有加速度的运动电子应不断幅射电磁波,能量不断减少,原子发光应产生连续光谱,最终电子落到核上。但实际上原子光谱为明线(或吸收光谱),原子也是稳定的。 |
氢的原子光谱现象。明线光谱为 |
(1)原子只能处于一系列不连续的能量状态中,这些状态叫定态,各定态的能量值为能级。电子虽绕核旋转,但不向外辐射能量,原子是稳定的。(2)原子从一定态跃迁到另一定态,它辐射或吸收一定频率(或波长)的光子,光子能量由两定态的能量差决定,即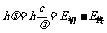 。(3)原子的不同能量状态跟电子沿不同轨道相对应,原子定态不连续,则电子的轨道也不连续。 。(3)原子的不同能量状态跟电子沿不同轨道相对应,原子定态不连续,则电子的轨道也不连续。 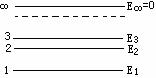 |
表明了卢瑟福核式结构学说困难。圆满解释氢原子光谱的规律。 |
解释有两个以上电子的复杂原子光谱遇到困难。 |
|
复杂原子的光谱现象 |
核外电子无确定轨道,电子在原子内各处出现几率不同。 |
克服了玻尔理论的困难 |
不能给出原子一个直图景。 |
[点拔2]对“一个卫星环绕地球”与“一个电子环绕氢原子核”卢瑟福结构模型进行类比分析。
地球引力场中的卫星所受地球的万有引力作为向心力。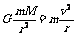 (
(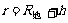 )
)
原子核(正电荷)电场中的电子受核的库仑引力作为向心力。
(1)卫星、电子的环绕速度和动能与距离的关系:
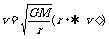 ,
,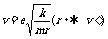
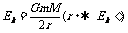 ,
,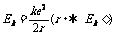
(2)若规定距地球和原子核无穷远时,卫星、电子势能为零:
地球的卫星:重力势能EP=0、动能Ek=0;地球系统总能量(机械能)=0
电子:电势能ε=0、动能EK=0;原子系统总能量=0
环行的卫星与电子的动能、势能、系统的总能量:
卫星要克服大气阻力做功,损耗机械能转化为内能;
↓E总=Ep↓+Ek↑(EP减少多,Ek增加少,E总减少)
环绕速度v增大,高度h(r)降低,沿螺旋线最终坠入大气层烧毁或溅落于地球上;
据经典电磁理论,速度变化的电子要辐射电磁波能量,使它总能量减少;
↓E总=ε↓+Ek↑(ε减少多,Ek增加少,E总减少)
环绕速度v增大,与核距离减小,辐射电磁波(光)的频率逐渐增大,(波长逐减)为生成连续光谱,沿螺旋线最终落于核上;
(3)根据玻尔理论,氢原子的电子为什么最终不落在核上?为什么原子发光生成原子光谱?
电子在某一定态轨道上虽有加速度,但不辐射电磁波能量,所以电子不会落到核上,原子是稳定的。这是因为宏观的经典电磁理论并不适用于微观电子的运动。
氢原子定态能量的减少,是由于高能级的激发态向低能级定态或基态跃迁,辐射一定能量光子造成。由于各定态有确定能量差,所以能生成有确定光子能量(hv)或确定光波频率(v)、波长(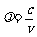 )的明线光谱或吸收光谱。
)的明线光谱或吸收光谱。
[例题1]氢原子基态能量E1=-13.6eV,电子绕核运动半径r1=0.53×10-10m.求氢原子处于n=4激发态时:(1)原子系统具有的能量?(2)电子在轨道上运动的动能?(3)电子具有的电势能?(4)向低能级跃迁辐射的光子频率最多有多少种?其中最低频率为多少(保留两位有效数字)?
解:(1)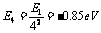
(2)因为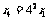 ,
,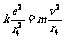 ,所以
,所以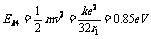 。
。
(3)因为E4=Ek4+ε4,所以ε4=E4-Ek4=-0.85-0.85=-1.7eV。
(4)最多有六种:从n=4→3;3→2;2→1;4→2;4→1;3→1。
能级差最小的是n=4→n=3,所辐射的光子能量为: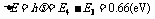 ,
,
最低频率: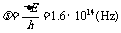
[思考]已知氢原子基态能量E1,氢原子在量子数为n的激发态时,电子的动能和电势能各为多少?处于量子数为n激发态的氢原子最多能辐射多少种频率的光谱线?
学生讨论: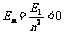 ,
,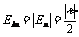 ,
,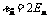 ,
, 。
。
[例题2]用光子能量为E的单色光照射容器中处于基态的氢原子。停止照射后,发现该容器内的氢能够释放出三种不同频率的光子,它们的频率由低到高依次为ν1、ν2、ν3,由此可知,开始用来照射容器的单色光的光子能量可以表示为:①hν1;②hν3;③h(ν1+ν2);④h(ν1+ν2+ν3)以上表示式中
A.只有①③正确 B.只有②正确 C.只有②③正确 D.只有④正确
C.只有②③正确 D.只有④正确
解:该容器内的氢能够释放出三种不同频率的光子,说明这时氢原子处于第三能级。根据玻尔理论应该有hν3=E3-E1,hν1=E3-E2,hν2=E2-E1,可见hν3=hν1+hν2=h(ν1+ν2),所以照射光子能量可以表示为②或③,答案选C。
2.卢瑟福的核式结构模型(行星式模型)
α粒子散射实验是用α粒子轰击金箔,结果是绝大多数α粒子穿过金箔后基本上仍沿原来的方向前进,但是有少数α粒子发生了较大的偏转。这说明原子的正电荷和质量一定集中在一个很小的核上。
1911年英国人卢瑟福由α粒子散射实验提出:在原子的中心有一个很小的核,叫原子核,原子的全部正电荷和几乎全部质量都集中在原子核里,带负电的电子在核外空间运动。
由α粒子散射实验的实验数据还可以估算出原子核大小的数量级是10-15m。
1.汤姆生模型(枣糕模型)
1897年,英国人汤姆生研究阴极射线时发现了电子。电子的发现说明原子是可分的。
127.一切伟大的行动和思想,都有一个微不足道的开始。
126.如果你希望成功,以恒心为良友,以经验为参谋,以小心为兄弟,以希望为哨兵。
125.世界上只有一样东西是任何人都不能抢走的,那就是智慧。
124.当你感到悲哀痛苦时,最好是去学些什么东西。学习会使你永远立于不败之地。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com