
1ЃЎ[2008жщКЃвЛФЃ]вбжЊAЁЂBЁЂCЁЂDКЭEЮхжжЗжзгЫљКЌдзгЕФЪ§ФПвРДЮЮЊ1ЁЂ2ЁЂ3ЁЂ4КЭ6ЃЌЧвЖМКЌга18ИіЕчзгЃЌгжжЊBЁЂCКЭDЪЧгЩСНжждЊЫиЕФдзгзщГЩЃЌЧвDЗжзгжаСНжждзгИіЪ§БШЮЊ1ЃК1ЁЃ
ЧыЛиД№ЃК
(1)ЁЁ зщГЩAЗжзгЕФдзгЕФКЫЭтЕчзгХХВМЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(2)ЁЁ BКЭCЕФЗжзгЪНЗжБ№ЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁКЭЁЁЁЁЁЁЁЁ ЃЛCЗжзгЕФСЂЬхНсЙЙГЪЁЁЁЁЁЁЁЁ ЁЁаЮЃЌИУЗжзгЪєгкЁЁЁЁЁЁЁЁЁЁЁЁ Зжзг(ЬюЁАМЋадЁБЛђЁАЗЧМЋадЁБ)ЃЛ
(3)ЁЁЯђDЕФЯЁШмвКжаМгШыЩйСПТШЛЏЬњШмвКЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(4)ЁЁ ШєНЋ1molEдкбѕЦјжаЭъШЋШМЩеЃЌжЛЩњГЩ1molCO2КЭ2molH2OЃЌдђEЕФЗжзгЪНЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
|
(3)гаЮоЩЋЦјЬхВњЩњЁЁЁЁЁЁЁЁЁЁЁЁ 2H2O2ЃНЃНЃН2H2O+O2ЁќЁЁ (4)CH4OЁЃ
2 [2008УЏУћвЛФЃ]AlКЭSiЁЂGeКЭAsдкдЊЫижмЦкБэН№ЪєКЭЗЧН№ЪєЙ§ЖЩЮЛжУЩЯЃЌдкЦфЕЅжЪКЭЛЏКЯЮядкНЈжўвЕЁЂЕчзгЙЄвЕКЭЪЏгЭЛЏЙЄЕШЗНУцгІгУЙуЗКЁЃЧыЛиД№ЯТСаЮЪЬтЃК
 (1) As ЕФМлВуЕчзгЙЙаЭЮЊ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(1) As ЕФМлВуЕчзгЙЙаЭЮЊ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2) AlCl3ЪЧЛЏЙЄЩњВњжаЕФГЃгУДпЛЏМСЃЌШлЕуЮЊ192.6ЁцЃЌШлШкзДЬЌвдЖўОлЬхA12C16аЮЪНДцдкЃЌЦфжаТСдзггыТШдзгЕФГЩМќРраЭЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3)ГЌИпЕМШШОјдЕФЭИпЮТФЩУзЕЊЛЏТС(AlN)дкОјдЕВФСЯжаЕФгІгУЙуЗКЃЌAlNОЇЬхгыН№ИеЪЏРрЫЦЃЌУПИіAlдзггыИіNдзгЯрСЌЃЌгыЭЌвЛИіAlдзгЯрСЌЕФNдзгЙЙГЩЕФПеМфЙЙаЭЮЊЁЃдкЫФДѓОЇЬхРраЭжаЃЌAlNЪєгкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ОЇЬхЁЃ
(4)SiКЭC ЭЌжїзхЃЌSiЁЂCКЭ0ГЩМќЧщПіШчЯТЃК
дкCКЭ0жЎМфПЩвдаЮГЩЫЋМќаЮГЩCO2ЗжзгЃЌЖјSiКЭOдђВЛФмКЭЬМФЧбљаЮГЩгаЯоЗжзгдвђЪЧ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ(5)SiCl4(l)ГЃгУзїбЬЮэМСЃЌдвђSiДцдк3dЙьЕРЃЌФмЭЌH20 (l)ХфЮЛЖјОчСвЫЎНтЃЌдкГБЪЊЕФПеЦјжаЗЂбЬЃЌЪдгУЛЏбЇЗНГЬЪНБэЪОЦфдРэЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(l) 4s24p3( l Зж) (2)ЙВМлМќ(ЛђІвМќ) (lЗж)
(3) 4 (lЗж)е§ЫФУцЬх(lЗж)дзг(2Зж) (4) SiвЛ0ДѓгкCвЛ0ЕФМќЃЌC=0ЕФМќФмДѓгкSi=OЕФМќФмЃЌЫљвдSiКЭOГЩЕЅМќЃЌЖјCКЭOвдЫЋМќаЮГЩЮШЖЈЗжзг( 2 Зж)
(5)SiCl4(l) + 3H2O (l) = H2Si03 (s) + 4HCl(aq) ( 2 Зж)
бЁаогаЛњЛЏбЇ5
3.дЊЫиЕчРыФмКЭдЊЫиЕчИКад
ЕквЛЕчРыФмЃКЦјЬЌЕчжаадЛљЬЌдзгЪЇШЅ1ИіЕчзгЃЌзЊЛЏЮЊЦјЬЌЛљЬЌе§РызгЫљашвЊЕФФмСПНазіЕквЛЕчРыФмЁЃГЃгУЗћКХI1БэЪОЃЌЕЅЮЛЮЊkJ/molЁЃЁЁ
(1).дзгКЫЭтЕчзгХХВМЕФжмЦкад.
 ЫцзХдзгађЪ§ЕФдіМг,дЊЫидзгЕФЭтЮЇЕчзгХХВМГЪЯжжмЦкадЕФБфЛЏ:УПИєвЛЖЈЪ§ФПЕФдЊЫиЃЌдЊЫидзгЕФЭтЮЇЕчзгХХВМжиИДГіЯжДгns1ЕНns2np6ЕФжмЦкадБфЛЏ.
ЫцзХдзгађЪ§ЕФдіМг,дЊЫидзгЕФЭтЮЇЕчзгХХВМГЪЯжжмЦкадЕФБфЛЏ:УПИєвЛЖЈЪ§ФПЕФдЊЫиЃЌдЊЫидзгЕФЭтЮЇЕчзгХХВМжиИДГіЯжДгns1ЕНns2np6ЕФжмЦкадБфЛЏ.
(2).дЊЫиЕквЛЕчРыФмЕФжмЦкадБфЛЏ.
ЫцзХдзгађЪ§ЕФЕндіЃЌдЊЫиЕФЕквЛЕчРыФмГЪжмЦкадБфЛЏ:
ЁяЭЌжмЦкДгзѓЕНгвЃЌЕквЛЕчРыФмгаж№НЅдіДѓЕФЧїЪЦЃЌЯЁгаЦјЬхЕФЕквЛЕчРыФмзюДѓЃЌМюН№ЪєЕФЕквЛЕчРыФмзюаЁЃЛ
ЁяЭЌжїзхДгЩЯЕНЯТЃЌЕквЛЕчРыФмгаж№НЅМѕаЁЕФЧїЪЦ.
ЫЕУїЃК
ЂйЭЌжмЦкдЊЫиЃЌДгзѓЭљгвЕквЛЕчРыФмГЪдіДѓЧїЪЦЁЃЕчзгбЧВуНсЙЙЮЊШЋТњЁЂАыТњЪБНЯЯрСкдЊЫивЊДѓМДЕк ЂђA зхЁЂЕк ЂѕA зхдЊЫиЕФЕквЛЕчРыФмЗжБ№ДѓгкЭЌжмЦкЯрСкдЊЫиЁЃBeЁЂNЁЂMgЁЂP
Ђк.дЊЫиЕквЛЕчРыФмЕФдЫгУЃК
a.ЕчРыФмЪЧдзгКЫЭтЕчзгЗжВуХХВМЕФЪЕбщбщжЄ.
b.гУРДБШНЯдЊЫиЕФН№ЪєадЕФЧПШѕ.ЁЁ I1дНаЁЃЌН№ЪєаддНЧПЃЌБэеїдзгЪЇЕчзгФмСІЧПШѕ.
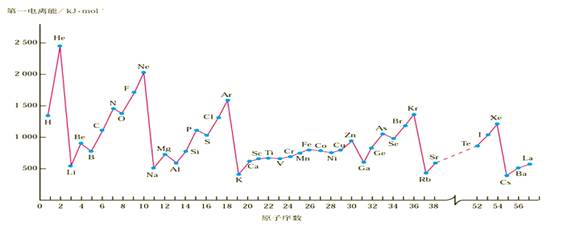
(3).дЊЫиЕчИКадЕФжмЦкадБфЛЏ.
дЊЫиЕФЕчИКадЃКдЊЫиЕФдзгдкЗжзгжаЮќв§ЕчзгЖдЕФФмСІНазіИУдЊЫиЕФЕчИКадЁЃ
ЫцзХдзгађЪ§ЕФЕндіЃЌдЊЫиЕФЕчИКадГЪжмЦкадБфЛЏЃКЭЌжмЦкДгзѓЕНгвЃЌжїзхдЊЫиЕчИКадж№НЅдіДѓЃЛЭЌвЛжїзхДгЩЯЕНЯТЃЌдЊЫиЕчИКадГЪЯжМѕаЁЕФЧїЪЦ.
ЕчИКадЕФдЫгУ:
a.ШЗЖЈдЊЫиРраЭ(вЛАу>1.8ЃЌЗЧН№ЪєдЊЫиЃЛ<1.8ЃЌН№ЪєдЊЫи).ЁЁЁЁ
b.ШЗЖЈЛЏбЇМќРраЭ(СНдЊЫиЕчИКадВюжЕ>1.7ЃЌРызгМќЃЛ<1.7ЃЌЙВМлМќ).
c.ХаЖЯдЊЫиМлЬЌе§ИК(ЕчИКадДѓЕФЮЊИКМлЃЌаЁЕФЮЊе§Мл).
d.ЕчИКадЪЧХаЖЯН№ЪєадКЭЗЧН№ЪєадЧПШѕЕФживЊВЮЪ§(БэеїдзгЕУЕчзгФмСІЧПШѕ).
Р§8.ЯТСаИїзщдЊЫиЃЌАДдзгАыОЖвРДЮМѕаЁЃЌдЊЫиЕквЛЕчРыФмж№НЅЩ§ИпЕФЫГађХХСаЕФЪЧ
ЁЁ AЃЎKЁЂNaЁЂLiЁЁЁЁЁЁ BЃЎNЁЂOЁЂCЁЁЁЁ CЃЎClЁЂSЁЂPЁЁЁЁЁЁ DЃЎAlЁЂMgЁЂNa
Р§9.вбжЊXЁЂYдЊЫиЭЌжмЦкЃЌЧвЕчИКадXЃОYЃЌЯТСаЫЕЗЈДэЮѓЕФЪЧ
AЃЎXгыYаЮГЩЛЏКЯЮяЪБЃЌXЯдИКМлЃЌYЯде§Мл
BЃЎЕквЛЕчРыФмПЩФмYаЁгкX
 CЃЎзюИпМлКЌбѕЫсЕФЫсадЃКXЖдгІЕФЫсадШѕгкYЖдгІЕФЫсад
CЃЎзюИпМлКЌбѕЫсЕФЫсадЃКXЖдгІЕФЫсадШѕгкYЖдгІЕФЫсад
DЃЎЦјЬЌЧтЛЏЮяЕФЮШЖЈадЃКHmYаЁгкHmX
Р§10.ЦјЬЌжааддзгЪЇШЅвЛИіЕчзгзЊЛЏЮЊЦјЬЌе§РызгЫљашвЊЕФзюЕЭФмСПНазіЕквЛЕчРыФм(I1)ЃЌЦјЬЌе§РызгМЬајЪЇШЅЕчзгЫљашзюЕЭФмСПвРДЮГЦЮЊЕкЖўЕчРыФм(I2)ЁЂЕкШ§ЕчРыФм(I3)ЁЁЯТБэЪЧЕкШ§жмЦкВПЗждЊЫиЕФЕчРыФмЃлЕЅЮЛЃКeV(ЕчзгЗќЬи)ЃнЪ§Он.
|
дЊЫи |
I1/eV |
I2/eV |
I3/eV |
|
Мз |
5.7 |
47.4 |
71.8 |
|
вв |
7.7 |
15.1 |
80.3 |
|
Бћ |
13.0 |
23.9 |
40.0 |
|
ЖЁ |
15.7 |
27.6 |
40.7 |
ЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.МзЕФН№ЪєадБШввЧП ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁB.ввЕФЛЏКЯМлЮЊ+1Мл
C.БћвЛЖЈЮЊЗЧН№ЪєдЊЫи ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁD.ЖЁвЛЖЈЪЧН№ЪєдЊЫи
Р§11.дкЯТУцЕФЕчзгНсЙЙжа,ЕквЛЕчРыФмзюаЁЕФдзгПЩФмЪЧ
A.ns2np3 ЁЁЁЁB.ns2np5 ЁЁЁЁC.ns2np4 ЁЁЁЁЁЁD.ns2np6
Р§12.ЕквЛЕчРыФмI1ЪЧжИЦјЬЌдзгX(g)ДІгкЛљЬЌЪБЃЌЪЇШЅвЛИіЕчзгГЩЮЊЦјЬЌбєРызгX+(g)ЫљашЕФФмСП.ЯТЭМЪЧВПЗждЊЫидзгЕФЕквЛЕчРыФмI1ЫцдзгађЪ§БфЛЏЕФЧњЯпЭМ.
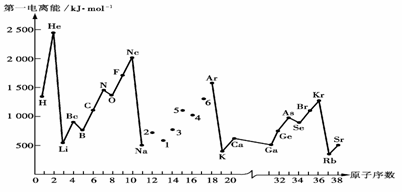
ЧыЛиД№вдЯТЮЪЬтЃК
(1).ШЯецЗжЮіЩЯЭМжаЭЌжмЦкдЊЫиЕквЛЕчРыФмЕФБфЛЏЙцТЩЃЌНЋNa--ArжЎМфСљжждЊЫигУЖЬЯпСЌНгЦ№РДЃЌЙЙГЩЭъећЕФЭМЯё.
(2).ДгЩЯЭМЗжЮіПЩжЊЃЌЭЌвЛжїзхдЊЫидзгЕФЕквЛЕчРыФмI1БфЛЏЙцТЩЪЧ______________ЃЛ
(3).ЩЯЭМжа5КХдЊЫидкжмЦкБэжаЕФЮЛжУЪЧ________________________________________ЃЛ
 (4).ЩЯЭМжа4ЁЂ5ЁЂ6Ш§жждЊЫиЕФЦјЬЌЧтЛЏЮяЕФЗаЕуОљБШЭЌжїзхЩЯвЛжмЦкЕФдЊЫиЦјЬЌЧтЛЏЮяЕЭКмЖрЃЌдвђЪЧЃК__________________________________.
(4).ЩЯЭМжа4ЁЂ5ЁЂ6Ш§жждЊЫиЕФЦјЬЌЧтЛЏЮяЕФЗаЕуОљБШЭЌжїзхЩЯвЛжмЦкЕФдЊЫиЦјЬЌЧтЛЏЮяЕЭКмЖрЃЌдвђЪЧЃК__________________________________.
Р§12.(1).МћЩЯЭМ(гв)ЁЁЁЁЁЁ (2).ДгЩЯЕНЯТвРДЮМѕаЁЁЁЁЁЁЁЁЁ
 (3).ЕкШ§жмЦкЃЌЂѕAзхЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3).ЕкШ§жмЦкЃЌЂѕAзхЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(4).вђЭЌжїзхЩЯвЛжмЦкЕФдЊЫиЕФЧтЛЏЮяЗжзгМфДцдкЧтМќЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁ
Р§13.1932ФъУРЙњЛЏбЇМвБЋСжЪзЯШЬсГіСЫЕчИКадЕФИХФю.ЕчИКад(гУXБэЪО)вВЪЧдЊЫиЕФвЛжжживЊаджЪЃЌШє x дНДѓЃЌЦфдзгЮќв§ЕчзгЕФФмСІдНЧПЃЌдкЫљаЮГЩЕФЗжзгжаГЩЮЊДјИКЕчКЩЕФвЛЗН.ЯТУцЪЧФГаЉЖЬжмЦкдЊЫиЕФ x жЕЃК
|
дЊЫиЗћКХ |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
x жЕ |
0.98 |
1.57 |
2.04 |
2.55 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
ЂХ.ЭЈЙ§ЗжЮі x жЕБфЛЏЙцТЩЃЌШЗЖЈNЁЂMgЕФ x жЕЗЖЮЇЃК
ЁЁЁЁЁЁЁЁ ЃМx (N)ЃМЁЁЁЁЁЁ ЃЌЁЁ ЁЁЁЁЁЁЁЁЃМx (Mg)ЃМЁЁЁЁЁЁЁЁ .
ЂЦ.ЭЦВтxжЕгыдзгАыОЖЕФЙиЯЕЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛИљОнЖЬжмЦкдЊЫиЕФxжЕБфЛЏЬиЕуЃЌЬхЯжСЫдЊЫиаджЪЕФЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ БфЛЏЙцТЩ.
ЂЧ.ФГгаЛњЛЏКЯЮяНсЙЙжаКЌSЃNМќЃЌЦфЙВгУЕчзгЖдЦЋЯђЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (аДдзгУћГЦ).
ЂШ.ОбщЙцТЩИцЫпЮвУЧЃКЕБГЩМќЕФСНдзгЯргІдЊЫиЕФ x ВюжЕЁїxЃО1.7ЪБЃЌвЛАуЮЊРызгМќЃЌЕБЁї xЃМ1.7ЪБЃЌвЛАуЮЊЙВМлМќ.ЪдЭЦЖЯAlBr3жаЛЏбЇМќРраЭЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ .
ЂЩ.дЄВтжмЦкБэжаЃЌ x жЕзюаЁЕФдЊЫиЮЛгкЁЁЁЁЁЁ жмЦкЁЁЁЁЁЁЁЁ зх.(ЗХЩфаддЊЫиГ§Эт)
Р§13.(1).2.55ЁЁ 3.44ЁЁЁЁ 0.93ЁЁЁЁ 1.57ЁЁ ЁЁ
(2).ЕчИКадЫцдзгАыОЖМѕаЁЖјдіДѓЃЌжмЦкадЁЁ
(3).ЕЊЁЁ ЁЁ(4).ЙВМлМќЁЁ ЁЁ(5).6ЃЌIA
ЁКзлКЯФЃФтбЕСЗЁЛ
2.(ЙЙдьдРэ)
СЫНтЖрЕчзгдзгжаКЫЭтЕчзгЗжВуХХВМзёбЕФдРэЃЌФмгУЕчзгХХВМЪНБэЪО1-36КХдЊЫидзгКЫЭтЕчзгЕФХХВМ.
(1).дзгКЫЭтЕчзгЕФдЫЖЏЬиеїПЩвдгУЕчзгВуЁЂдзгЙьЕР(бЧВу)КЭзда§ЗНЯђРДНјааУшЪі.дкКЌгаЖрИіКЫЭтЕчзгЕФдзгжаЃЌВЛДцдкдЫЖЏзДЬЌЭъШЋЯрЭЌЕФСНИіЕчзг.
(2).дзгКЫЭтЕчзгХХВМдРэ.
Ђй.ФмСПзюЕЭдРэ:ЕчзгЯШеМОнФмСПЕЭЕФЙьЕРЃЌдйвРДЮНјШыФмСПИпЕФЙьЕР.
Ђк.ХнРћВЛЯрШндРэ:УПИіЙьЕРзюЖрШнФЩСНИізда§зДЬЌВЛЭЌЕФЕчзг.
Ђл.КщЬиЙцдђ:дкФмСПЯрЭЌЕФЙьЕРЩЯХХВМЪБЃЌЕчзгОЁПЩФмЗжеМВЛЭЌЕФЙьЕРЃЌЧвзда§зДЬЌЯрЭЌ.
КщЬиЙцдђЕФЬиР§:дкЕШМлЙьЕРЕФШЋГфТњ(p6ЁЂd10ЁЂf14)ЁЂАыГфТњ(p3ЁЂd5ЁЂf7)ЁЂШЋПеЪБ(p0ЁЂd0ЁЂf0)ЕФзДЬЌЃЌОпгаНЯЕЭЕФФмСПКЭНЯДѓЕФЮШЖЈад.Шч24Cr [Ar]3d54s1ЁЂ29Cu [Ar]3d104s1.
(3).еЦЮеФмМЖНЛДэЭМКЭ1-36КХдЊЫиЕФКЫЭтЕчзгХХВМЪН.
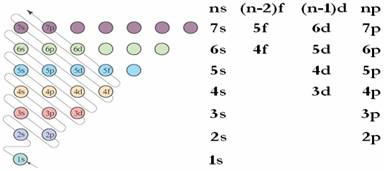
ЂйИљОнЙЙдьдРэЃЌЛљЬЌдзгКЫЭтЕчзгЕФХХВМзёбЭМЂХМ§ЭЗЫљЪОЕФЫГађЁЃ
ЂкИљОнЙЙдьдРэЃЌПЩвдНЋИїФмМЖАДФмСПЕФВювьЗжГЩФмМЖзщШчЭМЂЦЫљЪОЃЌгЩЯТЖјЩЯБэЪОЦпИіФмМЖзщЃЌЦфФмСПвРДЮЩ§ИпЃЛдкЭЌвЛФмМЖзщФкЃЌДгзѓЕНгвФмСПвРДЮЩ§ИпЁЃЛљЬЌдзгКЫЭтЕчзгЕФХХВМАДФмСПгЩЕЭЕНИпЕФЫГађвРДЮХХВМЁЃ
Р§3.БэЪОвЛИідзгдкЕкШ§ЕчзгВуЩЯга10ИіЕчзгПЩвдаДГЩ
A.310ЁЁЁЁЁЁЁЁЁЁЁЁ B.3d10ЁЁЁЁЁЁЁЁЁЁ C.3s23p63d2ЁЁ ЁЁЁЁЁЁD. 3s23p64s2
Р§4.ЯТСаЕчзгХХВМжаЃЌдзгДІгкМЄЗЂзДЬЌЕФЪЧ
 A.1s22s22p5ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
B. 1s22s22p43s2ЁЁ ЁЁЁЁ
A.1s22s22p5ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
B. 1s22s22p43s2ЁЁ ЁЁЁЁ
C. 1s22s22p63s23p63d44s2 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁD. 1s22s22p63s23p63d34s2
Р§5.ЯТСаЙигкМлЕчзгЙЙаЭЮЊ3s23p4ЕФСЃзгУшЪіе§ШЗЕФЪЧ
A.ЫќЕФдЊЫиЗћКХЮЊOЁЁЁЁЁЁЁЁЁЁЁЁ
B.ЫќЕФКЫЭтЕчзгХХВМЪНЮЊ1s22s22p63s23p4
C.ЫќПЩгыH2ЩњГЩвКЬЌЛЏКЯЮяЁЁЁЁЁЁ
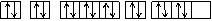 D.ЦфЕчзгХХВМЭМЮЊЃК
D.ЦфЕчзгХХВМЭМЮЊЃК
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ 1sЁЁ 2sЁЁЁЁ 2pЁЁЁЁ 3sЁЁЁЁ 3p
Р§6ЃЎАДЫљЪОИёЪНЬюаДЯТБэгаађКХЕФБэИёЃК
|
дзгађЪ§ |
ЕчзгХХВМЪН |
МлВуЕчзгХХВМ |
жмЦк |
зх |
|
17 |
Ђй |
Ђк |
Ђл |
Ђм |
|
Ђн |
1s22s22p6 |
Ђо |
Ђп |
Ђр |
|
Ђс |
Ђт |
3d54s1 |
ЂЯ |
ЁЁЂіB |
Р§6ЃЎЂй.1s22s22p63s23p5ЁЁ Ђк.3s23p5ЁЁ Ђл.3ЁЁ Ђм.ЂїAЁЁ Ђн.10ЁЁ Ђо.2s22p6
Ђп.2ЁЁ Ђр.0ЁЁ Ђс.24ЁЁ Ђт.1s22s22p63s23p63d54s1ЁЁ ЂЯ.4ЁЁ
Р§7.(1).ЩщдзгЕФзюЭтВуЕчзгХХВМЪНЪЧ4s24p3ЃЌдкдЊЫижмЦкБэжаЃЌЩщдЊЫиЮЛгк__________
жмЦкЁЁЁЁЁЁЁЁ зхЃЛзюИпМлбѕЛЏЮяЕФЛЏбЇЪНЮЊЁЁЁЁЁЁЁЁЁЁ ЃЌЩщЫсФЦЕФЛЏбЇЪНЪЧЁЁЁЁЁЁЁЁЁЁ .
(2).вбжЊЯТСадЊЫидкжмЦкБэжаЕФЮЛжУЃЌаДГіЫќУЧзюЭтВуЕчзгЙЙаЭКЭдЊЫиЗћКХЃК
Ђй.Ек4жмЦкЂєBзхЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
Ђк.Ек5жмЦкЂїAзхЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ .
Р§7.(1).4ЁЁ ЂѕAЁЁ As2O5ЁЁ Na3AsO4
(2).Ђй.3d24s2ЁЁ TiЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЂк.5S25p5ЁЁ I
1.ЕчзгдЦЃКгУаЁКкЕуЕФЪшУмРДУшЪіЕчзгдкдзгКЫЭтПеМфГіЯжЕФЛњЛсДѓаЁЫљЕУЕФЭМаЮНаЕчзгдЦЭМ.РыКЫдННќЃЌЕчзгГіЯжЕФЛњЛсДѓЃЌЕчзгдЦУмЖШдНДѓЃЛРыКЫдНдЖЃЌЕчзгГіЯжЕФЛњЛсаЁЃЌЕчзгдЦУмЖШдНаЁ.
ЕчзгВу(ФмВу)ЃКИљОнЕчзгЕФФмСПВювьКЭжївЊдЫЖЏЧјгђЕФВЛЭЌЃЌКЫЭтЕчзгЗжБ№ДІгкВЛЭЌЕФЕчзгВу.дзггЩРяЯђЭтЖдгІЕФЕчзгВуЗћКХЗжБ№ЮЊKЁЂLЁЂMЁЂNЁЂOЁЂPЁЂQ.
дзгЙьЕР(ФмМЖМДбЧВу)ЃКДІгкЭЌвЛЕчзгВуЕФдзгКЫЭтЕчзгЃЌвВПЩвддкВЛЭЌРраЭЕФдзгЙьЕРЩЯдЫЖЏЃЌЗжБ№гУsЁЂpЁЂdЁЂfБэЪОВЛЭЌаЮзДЕФЙьЕРЃЌsЙьЕРГЪЧђаЮЁЂpЙьЕРГЪЗФДИаЮЃЌdЙьЕРКЭfЙьЕРНЯИДдг.ИїЙьЕРЕФЩьеЙЗНЯђИіЪ§вРДЮЮЊ1ЁЂ3ЁЂ5ЁЂ7.
Р§1.ЯТСаЙигкЧтдзгЕчзгдЦЭМЕФЫЕЗЈе§ШЗЕФЪЧ
A.ЭЈГЃгУаЁКкЕуРДБэЪОЕчзгЕФЖрЩйЃЌКкЕуУмЖШДѓЃЌЕчзгЪ§ФПДѓ
B.КкЕуУмЖШДѓЃЌЕЅЮЛЬхЛ§ФкЕчзгГіЯжЕФЛњЛсДѓ
C.ЭЈГЃгУаЁКкЕуРДБэЪОЕчзгШЦКЫзїИпЫйдВжмдЫЖЏ
D.ЕчзгдЦЭМЪЧЖддЫЖЏЮоЙцТЩадЕФУшЪі
Р§2.ЯТСагаЙиШЯЪЖе§ШЗЕФЪЧ
A.ИїФмМЖЕФдзгЙьЕРЪ§АДsЁЂpЁЂdЁЂfЕФЫГађЗжБ№ЮЊ1ЁЂ3ЁЂ5ЁЂ7
B.ИїФмВуЕФФмМЖЖМЪЧДгsФмМЖПЊЪМжСfФмМЖНсЪј
C.ИїФмВуКЌгаЕФФмМЖЪ§ЮЊn -1ЁЁЁЁЁЁЁЁЁЁЁЁ
D.ИїФмВуКЌгаЕФЕчзгЪ§ЮЊ2n2
29ЃЎ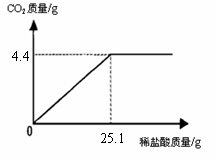 (7Зж) ФГАрвЛДЮЩчЛсЪЕМљЛюЖЏЪЧЕНСЌдЦИлМюГЇВЮЙлЃЌИУГЇжївЊВњЦЗжЎвЛЪЧаЁЫеДђ(ЬМЫсЧтФЦ)ЁЃВЮЙлНсЪјЃЌЭЌбЇУЧДјЛивЛаЉЛЏбщЪвРяЗЯЦњЕФаЁЫеДђбљЦЗЃЌРДВтЖЈЦфжаЬМЫсЧтФЦЕФжЪСПЗжЪ§(МйЩшИУбљЦЗжажЛКЌгаТШЛЏФЦвЛжждгжЪ)ЁЃШЁбљЦЗ9.3
gж№ЕЮМгШыЯЁбЮЫсЃЌЩњГЩCO2ЦјЬхЕФжЪСПгыЕЮМгЯЁбЮЫсЕФжЪСПЙиЯЕШчгвЭМЫљЪОЃЌЧѓЃК(МЦЫуНсЙћгУАйЗжЪ§БэЪОЃЌБЃСєЕНаЁЪ§ЕуКѓвЛЮЛЪ§зж)
(7Зж) ФГАрвЛДЮЩчЛсЪЕМљЛюЖЏЪЧЕНСЌдЦИлМюГЇВЮЙлЃЌИУГЇжївЊВњЦЗжЎвЛЪЧаЁЫеДђ(ЬМЫсЧтФЦ)ЁЃВЮЙлНсЪјЃЌЭЌбЇУЧДјЛивЛаЉЛЏбщЪвРяЗЯЦњЕФаЁЫеДђбљЦЗЃЌРДВтЖЈЦфжаЬМЫсЧтФЦЕФжЪСПЗжЪ§(МйЩшИУбљЦЗжажЛКЌгаТШЛЏФЦвЛжждгжЪ)ЁЃШЁбљЦЗ9.3
gж№ЕЮМгШыЯЁбЮЫсЃЌЩњГЩCO2ЦјЬхЕФжЪСПгыЕЮМгЯЁбЮЫсЕФжЪСПЙиЯЕШчгвЭМЫљЪОЃЌЧѓЃК(МЦЫуНсЙћгУАйЗжЪ§БэЪОЃЌБЃСєЕНаЁЪ§ЕуКѓвЛЮЛЪ§зж)
(1)бљЦЗжаЬМЫсЧтФЦЕФжЪСПЗжЪ§ЁЃ
(2)ЧЁКУЭъШЋЗДгІЪБЃЌЫљЕУШмвКжаШмжЪЕФжЪСПЗжЪ§ЁЃ
СЌдЦИлЪа2009ФъИпжаЖЮбЇаЃеаЩњЭГвЛЮФЛЏПМЪд
28ЃЎ(12Зж) ФГЛЏбЇаЫШЄаЁзщгавЛДЮЛюЖЏЕФФкШнЪЧЃКЖдвЛАќИЩдяЕФКьЩЋЗлФЉзщГЩНјааЬНОПЁЃЧыФуВЮгыВЂЛиД№гаЙиЮЪЬтЁЃ
[НЬЪІЬсаб]ЫќгЩCu ЁЂFe2O3 ЁЂFe(OH)3Ш§жжЙЬЬхжаЕФвЛжжЛђСНжжзщГЩЁЃ
[ЬсГіВТЯы]КьЩЋЗлФЉПЩФмЕФзщГЩгаЃК
ЂйжЛгаCuЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЂкжЛгаFe2O3ЁЁЁЁЁЁ
ЂлжЛга Fe(OH)3 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЂмЪЧFe2O3 ЁЂFe(OH)3ЕФЛьКЯЮяЁЁЁЁ
ЂнЪЧCu ЁЂFe2O3ЕФЛьКЯЮяЁЁ ЂоЪЧCu ЁЂFe(OH)3ЕФЛьКЯЮя
 [зЪСЯЛёЯЄ](1)2Fe(OH)3 ЁЁЁЁFe2O3
+3H2OЁЁ ЁЁЁЁ
[зЪСЯЛёЯЄ](1)2Fe(OH)3 ЁЁЁЁFe2O3
+3H2OЁЁ ЁЁЁЁ
(2)АзЩЋЮоЫЎCuSO4гіЫЎБфРЖ
 (3)CuдкFeCl3ШмвКжаЗЂЩњЗДгІЃК2FeCl3+CuЁЁЁЁ 2FeCl2+CuCl2
(3)CuдкFeCl3ШмвКжаЗЂЩњЗДгІЃК2FeCl3+CuЁЁЁЁ 2FeCl2+CuCl2
 [ЬНОПЫМТЗ]РћгУЮяжЪЕФаджЪВЛЭЌЩшМЦЪЕбщМгвдечБ№ЃЌЯШЗжБ№ЬНОПЦфжаЪЧЗёКЌгаFe(OH)3 ЁЂCuЕШЃЌж№ВНЫѕаЁЗЖЮЇЃЌШЛКѓдйбЁдёЪЪЕБЕФЪдМСКЭЗНЗЈЭЈЙ§ЪЕбщЬНОПЦфзщГЩЁЃ
[ЬНОПЫМТЗ]РћгУЮяжЪЕФаджЪВЛЭЌЩшМЦЪЕбщМгвдечБ№ЃЌЯШЗжБ№ЬНОПЦфжаЪЧЗёКЌгаFe(OH)3 ЁЂCuЕШЃЌж№ВНЫѕаЁЗЖЮЇЃЌШЛКѓдйбЁдёЪЪЕБЕФЪдМСКЭЗНЗЈЭЈЙ§ЪЕбщЬНОПЦфзщГЩЁЃ
(зАжУФкПеЦјжаЕФЫЎеєЦјЁЂCO2КіТдВЛМЦ)
[ЪЕбщЬНОП]
(1)МзЭЌбЇШЁЪЪСПКьЩЋЗлФЉзАШыЪдЙмжаЃЌАДЭМ28-1
НјааЪЕбщЁЃНсЙћЮоЫЎCuSO4УЛгаБфРЖЃЌДгЖјХХГ§
ВТЯыжаЕФ ЁЁЁјЁЁ ЁЃ(ЬюВТЯыжаЕФађКХ)
(2)дкМзЭЌбЇЪЕбщНсТлЕФЛљДЁЩЯЃЌввЭЌбЇСэШЁЩйСПКьЩЋЗлФЉгкЪдЙмжаЃЌЕЮМгзуСПЯЁбЮЫсЃЌеёЕДКѓЙлВьЃЌЗЂЯжЙЬЬхШЋВПШмНтЃЌШмвКБфЩЋЁЃввЭЌбЇШЯЮЊПЩвдХХГ§ВТЯыжаЕФЂйКЭЂнЃЌЖјБћЭЌбЇШЯЮЊжЛФмХХГ§ВТЯыЂйЃЌФуШЯЮЊ ЁЁЁј ЁЁЕФЙлЕуе§ШЗ(ЬюЁАввЁБЛђЁАБћЁБ)ЁЃ
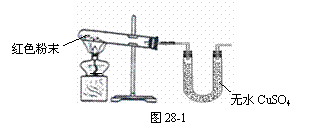
 (3)ЖЁЭЌбЇЮЊНјвЛВНШЗЖЈКьЩЋЗлФЉЕФзщГЩЃЌГЦШЁИУЗлФЉ5.0gзАШыгВжЪВЃСЇЙмжаЃЌАДЭМ28-2дкЭЈЗчГїжаНјааЪЕбщЁЃПЊЪМЪБЛКЛКЭЈШыCOЦјЬхЃЌЙ§вЛЖЮЪБМфКѓдйМгШШЪЙЦфГфЗжЗДгІЁЃД§ЗДгІЭъШЋКѓЃЌЭЃжЙМгШШЃЌШдМЬајЭЈCOЦјЬхжБжСВЃСЇЙмРфШДЁЃЗДгІЧАКѓГЦСПЯрЙизАжУКЭЮяжЪЕФзмжЪСПЃЌЦфЪ§ОнШчЯТБэЃК
(3)ЖЁЭЌбЇЮЊНјвЛВНШЗЖЈКьЩЋЗлФЉЕФзщГЩЃЌГЦШЁИУЗлФЉ5.0gзАШыгВжЪВЃСЇЙмжаЃЌАДЭМ28-2дкЭЈЗчГїжаНјааЪЕбщЁЃПЊЪМЪБЛКЛКЭЈШыCOЦјЬхЃЌЙ§вЛЖЮЪБМфКѓдйМгШШЪЙЦфГфЗжЗДгІЁЃД§ЗДгІЭъШЋКѓЃЌЭЃжЙМгШШЃЌШдМЬајЭЈCOЦјЬхжБжСВЃСЇЙмРфШДЁЃЗДгІЧАКѓГЦСПЯрЙизАжУКЭЮяжЪЕФзмжЪСПЃЌЦфЪ§ОнШчЯТБэЃК
|
ЁЁЁЁ |
ЗДгІЧА |
ЗДгІКѓ |
|
Ђё зщ |
ВЃСЇЙмКЭКьЩЋЗлФЉЕФзмжЪСПЮЊ37.3 g |
ВЃСЇЙмКЭЙЬЬхЮяжЪЕФзмжЪСПЮЊ36.1 g |
|
Ђђ зщ |
ЯДЦјЦПКЭЫљЪЂШмвК ЕФзмжЪСПЮЊ180.0 g |
ЯДЦјЦПКЭЦПжаЮяжЪ ЕФзмжЪСПЮЊ183.1 g |
[НЛСїЬжТл]ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(1)дкзАжУAжаЯШЭЈCOЦјЬхЕФзїгУЪЧЁЁ Ёј ЁЁЁЃ
(2)гІИУбЁдёЁЁ Ёј ЁЁзщЕФЪЕбщЪ§ОнМЦЫуРДШЗЖЈКьЩЋЗлФЉЕФзщГЩЁЃзюжеМЦЫуНсЙћБэУїЃКИУКьЩЋЗлФЉЕФзщГЩЪЧВТЯыжаЕФЕкЁЁ Ёј ЁЁзщ(ЬюађКХ)ЁЃ
(3)аДГіAзАжУжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЁЁ ЁјЁЁ ЃЛЪЕбщжаЙлВьЕНAзАжУжаЕФЯжЯѓЮЊЁЁ ЁјЁЁ ЁЃ
(4)ЮЊСЫЗРжЙШмвКЕЙЮќЃЌБОЪЕбщЭЃжЙМгШШЧАЪЧЗёашвЊЯШЖЯПЊAКЭBЕФСЌНгДІЃПЁЁ ЁјЁЁ (ЬюЁАашвЊЁБЛђЁАВЛашвЊЁБ)ЃЌРэгЩЪЧЁЁ ЁјЁЁ ЁЁЁЃ
[ЗДЫМЦРМл] ЮьЭЌбЇжИГіЃКДгЛЗБЃНЧЖШЃЌЭМ28-2зАжУгабЯжиВЛзужЎДІЁЃФуШЯЮЊгІИУШчКЮИФНјЃПЁЁ ЁјЁЁ ЁЃ
[ЭиеЙбгЩь]гаЭЌбЇЬсГіЖЁЭЌбЇЩЯЪіЪЕбщжаЕФCOЛЙПЩвдгУH2ДњЬцЃЌВЂНЋЭМ28-2жаBзАжУЛЛГЩЪЂгаМюЪЏЛв(ЩњЪЏЛвКЭЧтбѕЛЏФЦЙЬЬхЛьКЯЮя)ЕФИЩдяЙмЃЌРДШЗЖЈИУКьЩЋЗлФЉЕФзщГЩЃЌФуШЯЮЊЪЧЗёПЩааЃП ЁЁЁјЁЁ (ЬюЁАПЩааЁБЛђЁАВЛПЩааЁБ)ЁЃ
27ЃЎ(7Зж) НёФъЮвЪаОХФъМЖЛЏбЇЪЕбщВйзїПМВщЕФЗНЗЈЪЧгЩПМЩњГщЧЉШЗЖЈПМЬтЃЌаЁЛЊЭЌбЇГщЕНЕФЬтФПЪЧЁАвдМІЕАПЧКЭЯЁбЮЫсЮЊдСЯжЦШЁCO2ЁБЁЃаЁЛЊЭъГЩИУЪЕбщЕФВПЗжВйзїЙ§ГЬШчЯТЭМЫљЪОЃК
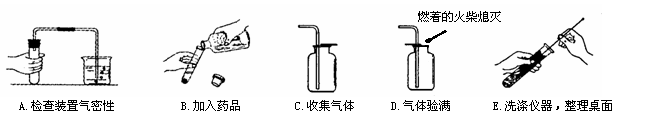
(1)аЁЛЊЩЯЪіВйзїЙ§ГЬжагаУїЯдДэЮѓЕФЪЧЁЁ Ёј ЁЁ(ЬюзжФИађКХ)ЁЃ
(2)ВйзїAжаЃЌаЁЛЊЫЩПЊЪжЦЌПЬКѓЃЌПДЕНЩеБФкЕФЕМЙмжааЮГЩвЛЖЮЁЁ ЁјЁЁ ЃЌжЄУїзАжУВЛТЉЦјЁЃ
(3)ШєвЊбщжЄМІЕАПЧЕФжївЊГЩЗжCaCO3жаЕФCa2+ЃЌжЛвЊдкЗДгІКѓШмвКжаж№ЕЮМгШы ЁЁЁјЁЁ ШмвКЃЌЙлВьЕН ЁЁЁјЁЁ ЯжЯѓМДПЩ(МІЕАПЧжаЕФдгжЪВЛИЩШХЗДгІЯжЯѓ)ЁЃШєЫљМгЪдМСе§ШЗЃЌЕЋЪЕбщИеПЊЪМНзЖЮШДЙлВьВЛЕНгІгаЕФЯжЯѓЃЌдђдвђЪЧ ЁЁЁј ЁЁЁЃ
(4)ШєНЋМІЕАПЧЛЛЮЊаПСЃЃЌРћгУЩЯЪіЪЕбщжаЩцМАЕНЕФвЧЦїКЭвЉЦЗПЩвджЦШЁСэвЛжжГЃМћЦјЬхЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЁЁЁј ЁЁЁЃ
26ЃЎ(9Зж) A-JОљЮЊГѕжаЛЏбЇжаЕФГЃМћЮяжЪЃЌвбжЊAЁЂBЕФзщ
ГЩдЊЫиЯрЭЌЃЌBЪЧзюГЃгУЕФШмМСЃЛГЃЮТЯТCЁЂEОљЮЊЮоДЬМЄад
ЦјЮЖЕФЦјЬхЃЌЧвCЮЊЕЅжЪЃЛAЁЂBЁЂDЁЂEЁЂJОљЮЊбѕЛЏЮяЃЌJ
ЪЧГЃгУЕФИЩдяМСЃЛFЁЂGЪЧДжбЮжаКЌгаНЯЖрЕФПЩШмаддгжЪЃЌЫќ
УЧЕФбєРызгЪЧгВЫЎжаКЌгаНЯЖрЕФН№ЪєРызгЃЛHЁЂIОљЮЊАзЩЋФб
ШмгкЫЎЕФбЮЃЌЦфжаHФмШмгкЫсЃЌЖјIШДВЛШмгкЫсЁЃA-JжЎМф
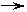 ЕФзЊЛЏЙиЯЕШчЭМЫљЪО(ЦфжаЁАЁЁЁЁ
ЁБДњБэЮяжЪжЎМфЕФзЊЛЏЙи
ЕФзЊЛЏЙиЯЕШчЭМЫљЪО(ЦфжаЁАЁЁЁЁ
ЁБДњБэЮяжЪжЎМфЕФзЊЛЏЙи
ЯЕЃЌВПЗжЗДгІЮяЁЂЩњГЩЮяКЭЗДгІЬѕМўвбТдШЅ)ЁЃ
(1)аДГіЯТСаЮяжЪЕФЛЏбЇЪНЃКBЁЁ ЁјЁЁ ЃЛDЁЁ ЁјЁЁ ЃЛI ЁЁЁјЁЁ ЃЛJЁЁ ЁјЁЁ ЁЃ
 (2)аДГіЯТСазЊЛЏЕФЛЏбЇЗДгІЗНГЬЪНЃКAЁЁЁЁ C ЁЁЁјЁЁ ЃЛЁЁ HЁЁЁЁ G ЁЁЁјЁЁ
ЃЛ
(2)аДГіЯТСазЊЛЏЕФЛЏбЇЗДгІЗНГЬЪНЃКAЁЁЁЁ C ЁЁЁјЁЁ ЃЛЁЁ HЁЁЁЁ G ЁЁЁјЁЁ
ЃЛ
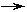 ХаЖЯЃКHЁЁЁЁ GЕФЗДгІЪєгкЛљБОЗДгІРраЭжаЕФЁЁ
ЁјЁЁ ЗДгІЁЃ
ХаЖЯЃКHЁЁЁЁ GЕФЗДгІЪєгкЛљБОЗДгІРраЭжаЕФЁЁ
ЁјЁЁ ЗДгІЁЃ
25ЃЎ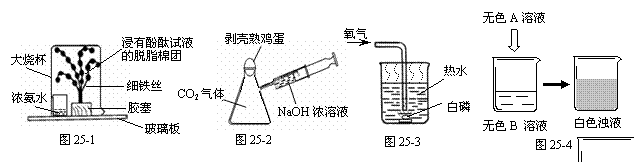 (8Зж) 2009ФъДКНкСЊЛЖЭэЛсЩЯЃЌСѕЧЋЕФФЇЪѕБэбнМЄЦ№СЫШЫУЧЧПСвЕФКУЦцаФЃЌВЂдкШЋЙњЗЖЮЇФкЯЦЦ№СЫФЇЪѕБэбнЕФШШГБЁЃдкбЇаЃПЦММНкЛюЖЏжаЃЌвЛЮЛОХФъМЖЭЌбЇИјЕЭФъМЖЭЌбЇБэбнСЫвЛзщЛЏбЇаЁФЇЪѕЃЌЧыФуРћгУЫљбЇЛЏбЇжЊЪЖНвПЊЦфжажЎУеЁЃ
(8Зж) 2009ФъДКНкСЊЛЖЭэЛсЩЯЃЌСѕЧЋЕФФЇЪѕБэбнМЄЦ№СЫШЫУЧЧПСвЕФКУЦцаФЃЌВЂдкШЋЙњЗЖЮЇФкЯЦЦ№СЫФЇЪѕБэбнЕФШШГБЁЃдкбЇаЃПЦММНкЛюЖЏжаЃЌвЛЮЛОХФъМЖЭЌбЇИјЕЭФъМЖЭЌбЇБэбнСЫвЛзщЛЏбЇаЁФЇЪѕЃЌЧыФуРћгУЫљбЇЛЏбЇжЊЪЖНвПЊЦфжажЎУеЁЃ
ФЇЪѕвЛЁАЦцЛЈБфЩЋЁБ
ЕРОпШчЭМ25-1ЫљЪОЃЌИУФЇЪѕжаПЩЙлВьЕНЁАЬњЪїЁБЩЯНўгаЮоЩЋЗгЬЊЪдвКЕФУоЭХгЩАзЩЋБфЮЊ ЁЁЁјЁЁ ЩЋЁЃИУФЇЪѕжаУЛгаЩцМАЕФаджЪЪЧЁЁ ЁјЁЁ (ЬюзжФИађКХ)ЁЃ
AЃЎАБЗжзгЪЧВЛЖЯдЫЖЏЕФЁЁ BЃЎАБЗжзггавЛЖЈжЪСПЁЁ ЁЁ
CЃЎХЈАБЫЎОпгаЛгЗЂадЁЁЁЁ DЃЎАБЦјЕФЫЎШмвКЯдМюад
ФЇЪѕЖўЁАЦПЭЬМІЕАЁБ
ЕРОпШчЭМ25-2ЫљЪОЃЌНЋзЂЩфЦїжаNaOHХЈШмвКзЂШыЦПжаЃЌЦЌПЬКѓЛсПДЕНМІЕАБЛЁАЭЬЁБШыЦПжаЁЃИУФЇЪѕжаЩцМАЕФЛЏбЇЗДгІЮЊЁЁ ЁјЁЁ (гУЛЏбЇЗНГЬЪНБэЪО)ЁЃ
ФЇЪѕШ§ЁАЫЎжаЩњЛ№ЁБ
ЕРОпШчЭМ25-3ЫљЪОЃЌЕБЭЈЙ§ЕМЙмЯђШШЫЎжаЭЈШыбѕЦјЪБЃЌАзСздкЫЎЯТШМЩеЁЃИУФЇЪѕЫЕУїШМЩеашвЊЕФЬѕМўЮЊЃКЂйПЩШМЮяЃЛЂкДяЕНШМЩеЫљашвЊЕФЁЁ ЁјЁЁ ЃЛЂлгаГфзуЕФЁЁ ЁјЁЁ ЁЃ
ФЇЪѕЫФЁАЁЎЧхЫЎЁЏБфЁЎХЃФЬЁЏЁБ
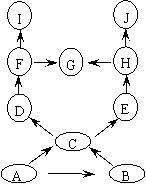 ЕРОпШчЭМ25-4ЫљЪОЃЌЕБAШмвКМгЕНЩеБжаЃЌЮоЩЋШмвКБфГЩАзЩЋзЧвКЁЃШєAЮЊЫсШмвКЃЌдђAЁЂBЕФПЩФмзщКЯЃКAЮЊЁЁ Ёј ЁЁЁЁЃЛBЮЊЁЁ ЁјЁЁ
ЁЃ(жЛашаДвЛзщ)
ЕРОпШчЭМ25-4ЫљЪОЃЌЕБAШмвКМгЕНЩеБжаЃЌЮоЩЋШмвКБфГЩАзЩЋзЧвКЁЃШєAЮЊЫсШмвКЃЌдђAЁЂBЕФПЩФмзщКЯЃКAЮЊЁЁ Ёј ЁЁЁЁЃЛBЮЊЁЁ ЁјЁЁ
ЁЃ(жЛашаДвЛзщ)
24ЃЎ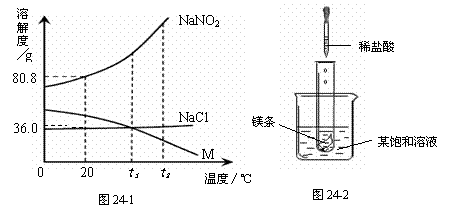 (6Зж) NaNO2(бЧЯѕЫсФЦ)ЁЂNaClКЭЮяжЪM (ВЛКЌНсОЇЫЎ)ЕФШмНтЖШЧњЯпШчЭМ24-1ЫљЪОЃЌЧыИљОнЭМЯёКЭгаЙиаХЯЂЛиД№ЯТСаЮЪЬтЃК
(6Зж) NaNO2(бЧЯѕЫсФЦ)ЁЂNaClКЭЮяжЪM (ВЛКЌНсОЇЫЎ)ЕФШмНтЖШЧњЯпШчЭМ24-1ЫљЪОЃЌЧыИљОнЭМЯёКЭгаЙиаХЯЂЛиД№ЯТСаЮЪЬтЃК
(1)t2 ЁцЪБЃЌNaNO2ЁЂNaCl
КЭMЕФШмНтЖШгЩДѓЕНаЁЕФЫГ
ађЪЧЁЁ Ёј ЁЁЁЃ
(2)ШчЭМ24-2ЫљЪОЃЌЕБЭљЪд
ЙмжаМгШы5mLЯЁбЮЫсЪБЃЌЪд
ЙмФкСЂПЬВњЩњДѓСПЦјХнЃЌЭЌЪБ
ЗХШШЪЙЩеБжаБЅКЭШмвКБфЛызЧ
(ВЛПМТЧЫЎЗжеєЗЂ)ЁЃЧыХаЖЯЃК
ИУБЅКЭШмвКжаЕФШмжЪЪЧNaNO2ЁЂ
NaClКЭMжаЕФ ЁЁЁј ЁЁЁЃ
(3)ЗжБ№НЋNaNO2ЁЂNaClКЭMЕФБЅКЭШмвКДгt2ЁцНЕЮТЕНt1ЁцЪБЃЌШ§жжШмвКжаШмжЪЕФжЪСПЗжЪ§гЩДѓЕНаЁЕФЫГађЪЧ ЁЁЁј ЁЁЁЃ
(4)NaNO2гаЖОЃЌЦфЭтЙлКЭЯЬЮЖгыЪГбЮКмЯрЫЦЃЌвђДЫвЊЗРжЙвђЮѓЪГNaNO2ЖјЗЂЩњжаЖОЪТЙЪЁЃЮЊСЫЧјБ№NaNO2ЁЂNaClЙЬЬхЃЌФГЛЏбЇаЫШЄаЁзщЭЌбЇВщдФзЪСЯЛёЕУШчЯТаХЯЂЃК NaNO2ЕФЫЎШмвКГЪМюадЃЌNaClЕФЫЎШмвКГЪжаадЃЛNaNO2ШлЕуЮЊ271 ЁцЃЌNaClШлЕуЮЊ801 ЁцЁЃ
Ђй аЁУїЭЌбЇЩшМЦЕФМјБ№ЪЕбщЗНАИШчЯТЃК
20ЁцЪБЗжБ№ШЁNaNO2ЁЂNaClИї5.0gгкСНжЛаЁЩеБжаЃЌЗжБ№МгШы10mLЫЎ(ЫЎЕФУмЖШНќЫЦПДзї1g/cm3)ЃЌгУВЃСЇАєГфЗжНСАшКѓЙлВьЁЃФуШЯЮЊДЫЗНАИЪЧЗёПЩаа Ёј (ЬюЁАПЩааЁБЛђЁАВЛПЩааЁБ)ЁЃ
Ђк ИУаЁзщЦфЫћЭЌбЇгжЩшМЦГігыаЁУїВЛЭЌЕФЪЕбщЗНАИЃЌВЂЛёЕУГЩЙІЁЃФуШЯЮЊИУЗНАИПЩФмЪЧ ЁЁЁјЁЁ (жЛЬюаДвЛжжЗНАИВЂМђЕЅа№Ъі)ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com