
1.之所以说财产等级制度重新分配了国家的政治权利,依据主要是
A.为后来雅典民主政治的发展开辟的道路
B.新兴工商业奴隶主逐渐跻身于统治阶层的行列
C.平民逐渐跻身于统治阶层行列
D.贵族阶层被排挤出国家政权之外
34.(11分)某研究性学习小组为证明在同温同压下,相同浓度相同体积的酸性不同的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积。设计的简易实验装置如下图。该实验的主要操作步骤如下:
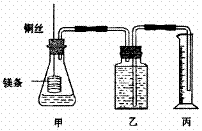
①配制浓度均为1 mol/L盐酸和醋酸溶液;
②用 量取10.00 mL 1mol/L盐酸和醋酸溶液分别加入两个锥形瓶中;
③分别称取除去表面氧化膜的镁带a g,并系于铜丝末端,a的数值至少为 ;
④在广口瓶中装足量的水,按图连接好装置;检查装置的气密性;
⑤将铜丝向下移动,使足量镁带浸入酸中(铜丝不与酸接触),至反应完全,记录 ;
⑥反应结束后,待温度恢复到室温,若丙中液面高于乙中液面,读取量筒中水的体积前,
应将量筒缓缓上下移动,使乙、丙中液面相平,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题:
(1)用文字表述④检查该装置气密性的操作与观察方法: 。
(2)写出Mg与醋酸反应的离子方程式_____________________________________________。
(3)本实验中丙应选用 (填序号)的量筒。 A、100 mL B、200 mL C、500 mL
(4)若水蒸气的影响忽略不计,在实验室条件下,气体摩尔体积:Vm= 。
(5)简述速率不等的原因 ,铜丝不与
酸接触的原因是 。
33.
 (12分)
(12分) 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属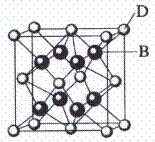 同一周期,又知E是周期表中1-18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图。
同一周期,又知E是周期表中1-18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图。 请回答:
请回答:
 (1)A元素的名称是
;
(1)A元素的名称是
;
 (2)B的基态原子轨道表示式为
,C的原子结构示意图为
,
(2)B的基态原子轨道表示式为
,C的原子结构示意图为
,
B与A形成的化合物比C 与A形成的化合物沸点高,其原因是 .
 (3)E属元素周期表中第
周期,第 族的元素,其元素名称是 ,它的+2价离子的电子排布式为
:
(3)E属元素周期表中第
周期,第 族的元素,其元素名称是 ,它的+2价离子的电子排布式为
:
 (4)从图中可以看出,D跟B形成的离子化合物的电子式为
;该离子化合物晶体的密度为ag·cm-3,则晶胞的体积是
(只要求带单位列出计算表达式)。
(4)从图中可以看出,D跟B形成的离子化合物的电子式为
;该离子化合物晶体的密度为ag·cm-3,则晶胞的体积是
(只要求带单位列出计算表达式)。
32.(9分)右图为一定量AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系。试回答:
(1) A点时已参加反应的AlCl3和 NaOH的物质的
量之比为 。
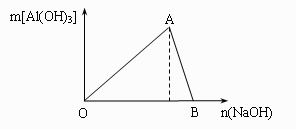
(2) OA段曲线所表示的反应的离子方程式是
___________________。AB段曲线所表示的反应的离子方程式是___________________。
(3) B处溶液中存在的浓度最大的离子是 (填离子符号)。向B处生成的溶液中通入二氧化碳,可观察到的现象是 。
(3) 向含有0.1mol NH4Al(SO4)2溶液中逐滴加入5mol·L-1NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有刺激性气味的气体逸出;最后白色沉淀逐渐减少并最终消失。请在右图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。

31. (8分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,回答下列问题:
(8分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,回答下列问题:
族 周期 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为 。(元素符号)
 (2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
。(化学式)
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
。(化学式)
 (3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式
。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式
。
 (4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

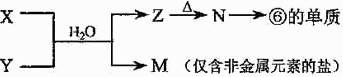
 X溶液与Y溶液反应的离子方程式为
,
X溶液与Y溶液反应的离子方程式为
,
 N→⑥ 的化学方程式为
。
N→⑥ 的化学方程式为
。
30.由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如右图转化关系(部分生成物和反应条件略去)。下列推断不正确的是 ( )
A.若A是单质,B和D的反应是OH-+HCO3- =H2O+CO32-,
则E一定能还原Fe2O3
B.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
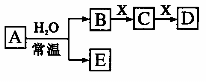 C.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
C.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
D.若D为CO,C能和E反应,则A一定为Na2O2
第II卷( 非选择题 共40分 )
29.为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1g样品加热至质量不在改变,其质量变为w2g,则该样品的纯度(质量分数)是 ( )
A.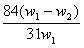 B.
B. C.
C.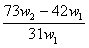 D.
D.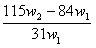

28.把镁铝合金用稀硫酸溶解,加入氢氧化钠溶液的体积与生成沉淀
的质量关系如右图,则合金中镁和铝的质量比是( )
A.2∶3 B.8∶9 C.4∶3 D.4∶9
27.向20mL2mol/LAlCl3溶液中加入30mLNaOH溶液,充分反应后得到0.78g白色沉淀,则NaOH溶液的物质的量浓度为( )
A.1 mol/L B. 2mol/L C. 5mol/L D. 8mol/L
26.向一定量的Na2CO3溶液中缓慢滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中的离子数目也相应地发生变化(如图所示)。
下列说法正确的是 ( )
A.a表示C1-
B.b表示CO32-
C.c表示Na+
D.d表示HCO3-

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com