
����Ŀ��ͬѧ���ڿ���ѧϰ���֪�����ƺ�þ�Ż�����CO2���������ͨ���������Ϸ���Mg����CO2��ȼ�գ�2Mg��CO2![]() 2MgO��C����û���ҵ��й����ܷ���CO2��Ӧ�Ľ��ܣ���ͬѧ��Ϊ���ܷ���������CO2��þ�ķ�Ӧ�����ܵĻ�ѧ����ʽΪ_______________��
2MgO��C����û���ҵ��й����ܷ���CO2��Ӧ�Ľ��ܣ���ͬѧ��Ϊ���ܷ���������CO2��þ�ķ�Ӧ�����ܵĻ�ѧ����ʽΪ_______________��
����ͬѧ��չ��������̽����
[ʵ��]��ȼ�ŵ�������װ�и����CO2�ļ���ƿ�У�������CO2�м���ȼ�ա�
[��������]Na2O�ǰ�ɫ���壬����CO2��Ӧ����Na2CO3����H2O��Ӧ����NaOH��
[�������]ͬѧ����Ϊ����CO2��ȼ�յIJ���Ӧ����Mg��CO2��ȼ�յIJ������������ͬ�����Բ�����������·��ֲ��룺ͨ�����۷���������________(�����)�϶��Ǵ���ģ������ǣ�______________________________________��
[��֤����]��Na2O��C����________��C����NaOH��C����Na2O��Na2CO3��C
ͨ�����۷���������________(�����)�϶��Ǵ���ģ������ǣ�__________________��
[��֤����]
���� | ʵ����� | ��Ҫʵ������ | ���ۣ�ȼ�ղ����жϣ� |
��1�� | ��������������ˮ�� | �����ܽ⣬�Թܵײ��к�ɫ���� | ȼ�ղ����п϶���___ |
��2�� | ȡ��1�����������ϲ���Һ�����������BaCl2��Һ | _________________ | ȼ�ղ����п϶���Na2CO3 |
��2�� | ȡ��2�����������ϲ���Һ������_____��Һ | ��Һ��ɺ�ɫ | ȼ�ղ����п϶���___ |
�ڲ���(2)��BaCl2��Һ������������Ŀ����____________________________________��
�ڲ���(3)��Ҳ����ͨ�������________�������м���(��дһ���Լ�)
[����]����________(�����)��ȷ��
���𰸡�4Na��CO2![]() 2Na2O��C �� NaOH������Ԫ�ض���Ӧ����û����Ԫ�� Na2CO3 �� NaOH������Ԫ�ض���Ӧ����û����Ԫ�� C(̼) �а�ɫ�������� ��̪ Na2O ��ȫ��ȥ̼���ƣ�����̼���Ƹ����������Ƶļ��� CuSO4��Һ ��
2Na2O��C �� NaOH������Ԫ�ض���Ӧ����û����Ԫ�� Na2CO3 �� NaOH������Ԫ�ض���Ӧ����û����Ԫ�� C(̼) �а�ɫ�������� ��̪ Na2O ��ȫ��ȥ̼���ƣ�����̼���Ƹ����������Ƶļ��� CuSO4��Һ ��
��������
����Ŀ��������Ϣ��֪������Mg��CO2��ȼ�յĻ�ѧ����ʽ���жϣ��ƺͶ�����̼�з�Ӧ���������ƺ�̼����ƽ���ɣ����������ͨ�����۷���������ۿ϶��Ǵ���ģ���ΪNaOH������Ԫ�ض���Ӧ����û����Ԫ�أ���������������ˮ�У������ܽ⣬�Թܵײ��к�ɫ���壬һ����̼��ȡ(1)���������ϲ���Һ�����������BaCl2��Һ���а�ɫ�������ɣ��϶���Na2CO3��ȡ(2)���������ϲ���Һ�������̪��Һ����Һ��ɺ�ɫ��ȼ�ղ����п϶���Na2O���������BaCl2��Һ��Ŀ���ǣ���ȫ��ȥ̼���ƣ�����̼���Ƹ����������Ƶļ��飻�ڲ���( 3 )��Ҳ����ͨ������CuSO4��Һ��CuCl2��Һ������ɫʯ����Һ�ȣ����м��飻ͨ��̽����֪�����������ȷ�ġ�


 ���Ӣ��������ϵ�д�
���Ӣ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС�������������Ϊ���⣬������һϵ�е�ʵ��̽�����
̽��1���о����������������������ƺ�����ķ�Ӧ�̶ȡ�
ʵ������ | ʵ������ | ��������� |
ȡ��Ӧ��������Һ���Թ��У�������廯����___________�� | _________ | ������� |
̽��2���о���������������ᡢ�����п��Ӧ
ͨ��̽��ʵ�飬ͬѧ�Ƿ��������������Һ�����Ժ�п��Ӧ�����������������ֹ�ͬ�����ԭ��Ϊ________________________________________________________________________��
̽��3��̽��δ֪����Ũ�����ͭ��ȡ���塣
��֪![]() ��NO2�ܺ�ˮ��Ӧ���������NO��NO��NO2���ǿ�������Ⱦ�
��NO2�ܺ�ˮ��Ӧ���������NO��NO��NO2���ǿ�������Ⱦ�
(1)���ø÷�Ӧ��ȡ���������ķ���װ�ã�Ӧѡ��ͼ��ʾװ���е�________���ռ�NO2�ķ���Ϊ________��
(2)��ӦNO��X��NO2�У�X�Ļ�ѧʽӦΪ________������Ũ�����ͭ��ȡNO��Ӧ���õ��ռ�������________________________________________________________________________��
̽��4����ȤС��ͬѧ��ʢ�г���ʯ��ˮ1000g�Ĵ��ձ��м���10g̼������Һ��ǡ����ȫ��Ӧ�����ȥ������ʣ��Һ��������Ϊ1009.8g����ô����̼������Һ��������������Ϊ________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(7��)��ͼ�Ƕ������Ȼ��Ʒ�Ӧ��ϵ�Ĺ�����������
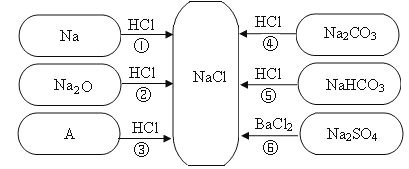
��ش��������⣺
(1)����A�dz����ļд��A�Ļ�ѧʽ��______��
(2)д����Ӧ�ٵĻ�ѧ����ʽ��___________________��
(3)˵��NaHC03��ҽ���ϵ�һ����;��______________ ��
(4)��Ӧ�ۡ��ܡ��ݡ����ܹ����е�ԭ����_______________��
(5)ʵ��������200g 8����NaCl��Һ����Ҫˮ��������___________g�����ƹ�����Ϊ�˼ӿ�NaCl���ܽ⣬���Բ�ȡ�Ĵ�ʩ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ1��a��b��c�������ʵ��ܽ������,�ش���������:
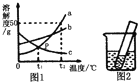
��1��P������________________________��
��2��t2��ʱ,��50��a���ʷ���50gˮ�г���ܽ�õ���Һ������Ϊ____g
��3��t2��ʱ,a��b��c�������ʵ��ܽ���ɴ�С������˳��Ϊ_________.
��4��t1��ʱ,��ʢ��c�ı�����Һ��С�Թܷ���ʢˮ���ձ��У���ͼ2��,��ˮ�м��붨�����������ƹ����,�Թ��е���Һ�����,ԭ����__________��
��5����t2��ʱ,a��b��c�������ʵı�����Һ������t1��,������Һ�����ʵ����������ɴ�С��˳����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ء�
(1)��ʳ������Ӫ�������ǽ����Ļ�����֤������ʳ���У������������________(����ĸ��ţ���ͬ)�����ṩ���������ʵ���________��

��A ��ͷ��������B ˮ������������C ����
(2)�����ճ������е����������Լ��ٻ�����Ⱦ����________��
A ������������ʻ
B ������մ�������
C ����ʹ�ò���Ļǽ
D ���������Լ��ˮ
(3)____________����Ϊ��ʯȼ�ϣ��Dz�����������Դ��Ŀǰ���������úͿ������ܡ���ϫ�ܺ�________(���һ�ּ���)������Դ���ɽ�ʡ��ʯȼ�ϣ����ٻ�����Ⱦ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ֧�Թ��з���һС��þ��(�Ѳ�ȥ����Ĥ)�������Թ��м���һ���������ᣬþ��������_____��������Ӧ�Ļ�ѧ����ʽ��_____��
[��������]Ϊ���ٴι۲�������Ӧ����С��ͬѧ�ýϳ���þ����������ʵ�飬���������쳣�����Թ��г����˰�ɫ������
[ʵ����֤1]С��ͬѧ�������ʵ��IJ�ͬ����ƶԱ�ʵ�鷽����̽�������쳣�����ԭ��
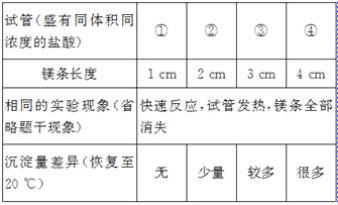
[�ó�����]þ�������ᷴӦ������ɫ������_____�йء�
[��]��ɫ������ʲô���ʣ�
[��������]��20 ��ʱ��100 gˮ��������ܽ��Ȼ�þ54.8 g��
��þ������ˮ��Ӧ����һ�ּ��������
���Ȼ����Ȳ�����ˮҲ������ϡ���ᡣ
[��������]����һ��þ����������Ȼ�þ����������������þ�������������_____(�û�ѧ����ʽ��ʾ)��
[ʵ����֤2]����ɫ����ϴ�Ӹɾ����ֱ�ȡ����������A��B��C�Թ��У��������ʵ�飺
�Թ� | ���� | ���� | ���� |
A | ������������ | _____����ɫ����_____ | ����һ����ȷ�������ְ�ɫ�������������� |
B | ��������ˮ | ��ɫ����_____ | ���������ȷ |
C | ��������ϡ���� | ��ɫ������ʧ | ԭ��ɫ�����к��е������ǣ�Mg2+��_____ |
�����μӼ�����������Һ | ���ִ�����ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���ڰ�ɫ��ΰ�1��6�Ŀ�Ѩ�У��ֱ�μ�2����ɫʯ����Һ��
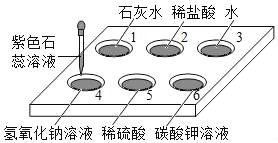
��֪����Ѩ1��ʯ��ˮ ��2��ϡ���� 3��ˮ 4������������Һ 5��ϡ���� 6��̼�����Һ
��1����Ѩ6����Һ��Ϊ��ɫ��˵��̼�����Һ��_____������ԡ����ԡ�����
��2����Һ��Ϊ��ɫ�Ŀ�Ѩ��_____�����Ѩ��ţ���ͬ����
��3����Ϊ�հ���ʵ��Ŀ�Ѩ��_____��
��4�������Ѩ4�еμ�ϡ���ᣬ��Һ��Ϊ��ɫ���û�ѧ����ʽ������ԭ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϡ����������ټ��뵽һ������ϡ�������Ƶ���Һ�У������ֻ������Է�Ӧ��������Һ���¶ȡ�pH����ʵʱ�ⶨ���õ���������ͼ��ʾ��
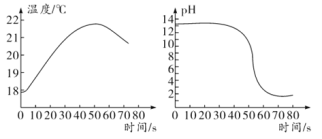
����֤����������ȷ����
A. ����pH��С�ҵ���7����ʵ�������ж�ϡ������ϡ�������Ʒ����˻�ѧ��Ӧ
B. �÷�Ӧ��Լ��60 sʱǡ����ȫ��Ӧ
C. ��Ӧ��ϵ�¶����ߣ��Ƿ�Ϊϡ�����ϡ����������Һ��ϡ�������£�����Ҫͨ��ʵ��֤��
D. ����������������Ļ�ѧ��Ӧ��������ͨ����ⷴӦ�����ʧ�������ʵ�������������֤
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ķ�˼�����ش����⣺
��1��ˮֱͨ�����ܷ����ֽⷴӦ����Ӧ�Ļ�ѧ����ʽ_____�������õ�16�������壬����������Ӧ�õ�_____�������塣
��2�������������������������У���ʼ�۲����������������ʧ����Һ_____����Ӧ�Ļ�ѧ����ʽ_____����Ӧһ��ʱ����ֻ�۲쵽������_____��������Ӧ����ʽ_____��
��3�����ڴ��ʯ��ˮ��ϸ��ƿ�г�������һ���ɫ��������̼��ƣ�������ԭ�����û�ѧ����ʽ��ʾ_____��ϴ�Ӹ��Լ�ƿʱӦ�ü�����_____��Ӧ����ʽ_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com