
【题目】海水的综合利用主要流程如下图。
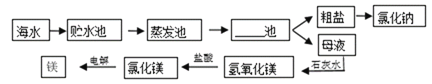
(1)上述工业生产流程图中横线上应该填写______。
(2)根据海水晒盐的工业流程,下列说法中正确的是_____(填字母)
a海水进入贮水池,海水的成分基本不变
b在蒸发池中,海水中氯化钠的质量逐渐增加
c粗盐提纯制成精盐需要用到过滤操作
d母液是氯化钠的饱和溶液
(3)制取金属镁,需要在高温熔化状态下电解氯化镁,写出该反应化学方程式___,该反应需要在氩气或者密闭的环境中进行,理由是___。
(4)如图,A——H是初中化学常见的物质。根据图示回答下列问题。
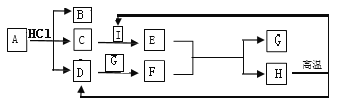
①A物质是焙制糕点的发酵粉主要成分之一,请写出B物质的一种用途____。
②H是常用的建筑材料之一,请写出D与G反应的化学方程式____。
③C与I反应的现象是____。
④该流程没有涉及到的化学基本反应类型是___。
【答案】结晶 acd MgCl2![]() Mg+Cl2↑ 高温情况下,镁要与氧气反应,氩气化学性质稳定起保护作用 调味剂、融雪剂、选种(合理即可) CO2+2NaOH=Na2CO3+H2O 放出热量 置换反应
Mg+Cl2↑ 高温情况下,镁要与氧气反应,氩气化学性质稳定起保护作用 调味剂、融雪剂、选种(合理即可) CO2+2NaOH=Na2CO3+H2O 放出热量 置换反应
【解析】
(1)海水蒸发后要经过结晶池。
(2)
a.海水进入贮水池,海水的成分基本不变,正确;
b.在蒸发池中,水分逐渐被蒸发,海水中氯化钠的质量没有改变,溶质的质量分数逐渐增加,故错误;
c.粗盐提纯制成精盐的过程中,结晶池需要用到过滤操作,故正确;
d.结晶池中获得的母液是氯化钠的饱和溶液,正确。故选acd。
(3)氯化镁在高温下电解生成镁和氯气,反应的方程式为:MgCl2![]() Mg+Cl2↑。镁是一种活泼的金属,在高温下易于氧气反应生成氧化镁,故该实验需要在氩气的环境下进行,氩气起到保护作用,防止金属镁被氧化。
Mg+Cl2↑。镁是一种活泼的金属,在高温下易于氧气反应生成氧化镁,故该实验需要在氩气的环境下进行,氩气起到保护作用,防止金属镁被氧化。
(4)A物质是焙制糕点的发酵粉主要成分之一,故A是碳酸氢钠,碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳和水,H是建筑材料,且在高温的条件下能生成I和D,故H是碳酸钙,D是二氧化碳,I是氧化钙;生成的B和C 是氯化钠或水,C能与I反应生成E,则C是水,B是氯化钠,E是氢氧化钙,氢氧化钙能与F反应生成碳酸钙和G,则F可能是碳酸钠,G可能是氢氧化钠。经分析,推断合理。
①B是氯化钠,可以做调味品。②D是二氧化碳,G是氢氧化钠,反应的方程式为:CO2+2NaOH=Na2CO3 +H2O.③C是水,I是氧化钙,水和氧化钙反应放出大量的热量。④该流程没有涉及到的化学基本反应类型是置换反应。


 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:初中化学 来源: 题型:
【题目】生活中处处有化学,联系学过的化学知识,按要求完成下列各题:
(1)高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂,高铁酸钠中铁元素的化合价是:_____;从物质分类的角度看,该物质属于_______(填序号).
①酸 ②化合物 ③盐 ④碱 ⑤氧化物
(2)如图为“胃酸完全抑制剂”的标签.服用“胃酸完全抑制剂”后在胃内发生中和反应的化学反应方程式是____.

(3)医生往往给胃病患者喝钡餐(主要成分是BaSO4)作胃病检查,但可溶性重金属钡盐是剧毒物质,前不久马大叔误食碳酸钡而中毒,后来医生立即让他服泻盐MgSO4 来解毒,解毒的原理是(填化学方程式)_______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验室制取和收集气体的装置图,回答有关问题。
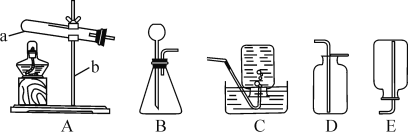
(1)写出装置图中仪器a、b的名称:a____,b____。
(2)写出实验室用装置A制取氧气的一个化学方程式:________________________。
(3)若用装置C收集氧气,导管口开始有气泡放出时,不宜立即收集。当____时,再把导管口伸入盛满水的集气瓶。集气瓶中的氧气收集满时可观察到水槽中有____________。
(4)若用装置B制取CO2,为了防止CO2从长颈漏斗逸出,正确的操作是____。收集CO2应选用装置_____,原因是____________。CO2的验满方法是_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化氢分解的产物与其他物质有如下转化关系.请根据所学知识按要求填空:
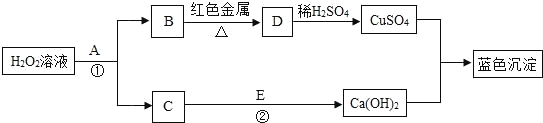
(1)A 在反应①中起____作用,D 的化学式为____.
(2)反应②的化学反应方程式为____.
(3)蓝色沉淀属于____(填“酸”“碱”或“盐”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了检验在氢气和二氧化碳的混合气体中是否混入一氧化碳,用如下装置进行实验
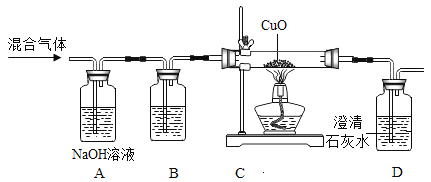
(1)装置A中的氢氧化钠溶液能够除去混合气体中的二氧化碳气体,已知氢氧化钠的化学性质与氢氧化钙相似,则A中发生的反应方程式为_______________________________(提示:此反应生成物中没有沉淀);装置B中盛放的试剂是石灰水,目的是______________________。
(2)装置C中氧化铜一定发生的反应方程式是_____________________________现象是____________________________________。
(3)当观察到__________________________现象时,说明混合气体中一定含有一氧化碳,此时装置C中氧化铜发生的另一个反应的方程式是___________________________。
(4)如果混合气体中有一氧化碳,应该在D装置的排气管口采取的措施是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的转化关系如图所示(“→”表示反应能一步实现,部分反应物、生成物和反应条件均已略去),下列说法错误的是
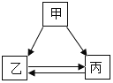
A. 若甲是一种黑色固体,乙和丙可能是组成元素相同的两种气体
B. 若乙是最常用的溶剂,丙是单质,则甲可能CO2
C. 若甲是纯碱,乙是一种常见的温室气体,则丙可能是碳酸钙
D. 若甲、乙、丙是实验室的三大强酸,则丙可能是硝酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CuCl常用作有机合成催化剂,实验室以初级铜矿粉(主要成分为硫化亚铜(Cu2S)及少量Fe2O3等)为原料制备活性CuCl。实验过程如下:
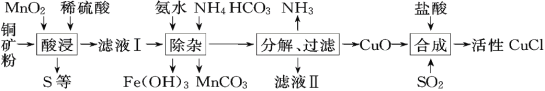
(资料)
①MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
②Cu(OH)2可溶于氨水形成深蓝色硫酸四氨合铜[Cu(NH3)4SO4]溶液;
③[Cu(NH3)4SO4]常温稳定,在热水中会分解生成NH3;
④CuCl在空气中易被氧化。
(1)酸浸时,为了提高浸取率可采取的措施有______(任写一点); “酸浸”过程中发生的化学反应有:①Cu2S+2MnO2+4H2SO4=2______+2MnSO4+S+4H2O、②______。从后续生产的角度分析,酸浸时稀硫酸不宜过量太多的原因是______。
(2)除杂过程中加足量氨水的作用①使Fe3+沉淀;②中和过量的硫酸;③______。
(3)①“分解”实验条件及现象如下表所示。
温度/℃ | 压强/kPa | 时间/min | 残液颜色 | |
A | 110 | 101.3 | 60 | 浅蓝色 |
B | 100 | 74.6 | 40 | 很浅 |
C | 90 | 60.0 | 30 | 无色透明 |
则“分解”实验条件应选______(填字母)。
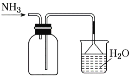
②“分解”生成的NH3可以回收利用。在实验室用如图装置来收集NH3,当集气瓶收集满NH3时观察到的现象是______。
(4)请补充从“合成”所得混合物中得到CuCl的实验操作步骤:过滤、洗涤、______。
A 真空干燥 B 在氩气中干燥 C 在空气中烘干
(5)若要制得99.5g CuCl,理论上至少需要硫化亚铜含量为60%的铜矿粉多少克______?(请写出计算过程,结果保留到小数点后一位)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化亚铜用途广泛,在潮湿的空气中易变质。制备反应方程式:2CuCl2+Na2SO3=2CuCl↓+2NaCl+SO3,工业制备流程如下:
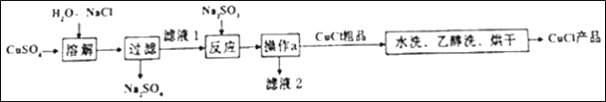
下列说法不合理的是( )
A. “过滤”得硫酸钠固体,说明常温下硫酸钠的溶解度比氯化铜小
B. CuCl难溶于水和乙醇
C. “反应”中产生的三氧化硫会迅速和水化合生成H2SO3
D. “滤液2”中的氯化钠可循环利用
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是工业上用软锰矿(主要成分为MnO2)制备高锰酸钾的一种工艺流程图:
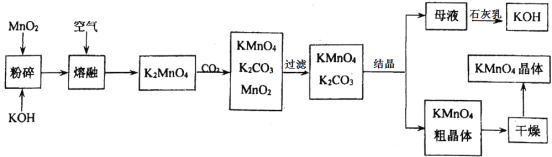
(资料) 在反应过程中有元素化合价变化的反应称为氧化还原反应。在氧化还原反应中,所含元素化合价降低的反应物称为氧化剂,所含元素化合价升高的反应物称为还原剂,且化合价升高总数等于化合价降低总数。
(1)将软锰矿粉碎的目的是_________________;
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要化学反应方程式______;
(3)上述流程中可以循环利用的物质是______;
(4)结晶后,干燥高锰酸钾晶体温度不宜过高的原因是(方程式表示)_____________。
(5)四种基本反应类型中一定不属于氧化还原反应的是_______;
A 化合反应 B 分解反应 C 置换反应 D 复分解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com