
【题目】明末宋应星于崇祯十年(公元1637年)所著《天工开物》,炼锌工艺的现存文字记载:“每炉甘石(ZnCO3)十斤,装载入一泥罐中,封裹泥固,以渐砑干,勿使见火拆裂。然后逐层用煤炭饼垫盛。其底铺薪,发火煅红,罐中炉甘石熔化成团。冷定毁罐取出。每十耗其二,即倭铅(金属锌)也。”如图。
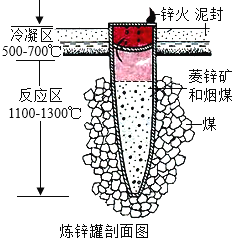
(1)“此物(“锌火”)无铜收伏,入火即成烟飞去”(宋应星语)。意思是锌的沸点(907℃)较低,宜与铜熔合制成黄铜。黄铜_____(填“是”或“不是”)金属材料。
(2)此图罐中烟煤作用是作_____剂。
(3)炉甘石的主要成分为ZnCO3,与碳酸钙同属于碳酸盐。往炉甘石中加入盐酸后,有气体产生,将产生的气体通入澄清石灰水,澄清石灰水变浑浊。写出炉甘石(ZnCO3)与稀盐酸反应的化学方程式:_____。
【答案】是 还原 ZnCO3+2HCl=ZnCl2+H2O+CO2↑
【解析】
碳酸锌和稀盐酸反应生成氯化锌、水和二氧化碳,在高温的条件下,碳酸锌分解为氧化锌和二氧化碳,碳与氧化锌在高温的条件下反应生成锌和二氧化碳。
(1)金属材料包括纯金属和合金,故黄铜是金属材料。
(2)烟煤的主要成分是碳,在高温的条件下,碳酸锌分解为氧化锌和二氧化碳,在罐中,碳与氧化锌在高温的条件下反应生成锌和二氧化碳,碳能夺取氧化锌中的氧将其还原为锌,故此图罐中烟煤作用是作还原剂。
(3)炉甘石(ZnCO3)与稀盐酸反应生成氯化锌、水和二氧化碳,反应的化学方程式为ZnCO3+2HCl=ZnCl2+H2O+CO2↑。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质间的反应如图所示,下列选项符合图示反应关系的是:
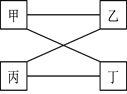
选项 | 甲 | 乙 | 丙 | 丁 |
A | CuO | H2SO4 | CO2 | O2 |
B | Na2SO4 | Ba(OH)2 | HCl | Ba(NO3)2 |
C | NaOH | CO2 | Ca(OH)2 | MgCl2 |
D | Mg | Cu(OH)2 | NaOH | H2SO4 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的转化关系如图所示(“→”表示反应可以一步实现)。 下列物质符合甲、乙、丙要求的有
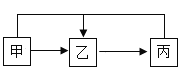
A.Na2CO3 NaOH Ca( OH)2
B.C CO2 CO
C.Ca(OH)2 CaCO3 CO2
D.H2SO4 H2 Cu
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是“汽车尾气催化转换器”将汽车尾气中的有毒气体转化为无毒气体的微观模拟图,请回答下列问题:
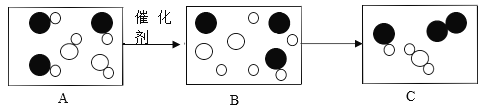

(1)在C图中将相关的粒子补充完整; __________
(2)此变化前后未发生改变的粒子是________。
(3)此反应中反应物均属于氧化物的微观判断依据是_____。
(4)画出比1个一氧化氮分子多3个电子,且带一个单位负电荷的粒子的结构示意图_。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属M与AgNO3溶液反应的化学方程式为:M+2AgNO3=M(NO3)2+2Ag。则下列说法错误的是( )
A.M的金属活动性比Ag强B.金属M可能是铝
C.该反应属于置换反应D.该反应前后M的化合价发生了改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验方案不能达到实验目的是
A.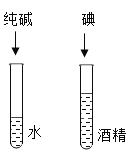 探究影响溶解性的因素
探究影响溶解性的因素
B.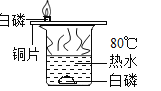 证明可燃物燃烧需要氧气
证明可燃物燃烧需要氧气
C.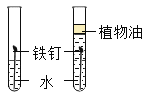 探究铁钉生锈与氧气有关
探究铁钉生锈与氧气有关
D.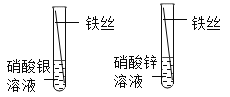 比较Fe、Ag 、Zn的金属活动性
比较Fe、Ag 、Zn的金属活动性
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象分别与选项中的操作相对应,其中不合理的是( )
A.  向一定量的稀醋酸中加入水
向一定量的稀醋酸中加入水
B.  向一定量的锌粉中加入盐酸
向一定量的锌粉中加入盐酸
C.  加热一定量的高锰酸钾固体
加热一定量的高锰酸钾固体
D.  一定温度时向一定量的石灰水中加入氧化钙
一定温度时向一定量的石灰水中加入氧化钙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如下图所示(假设铁片除有Fe2O3外,不含其他杂质)。
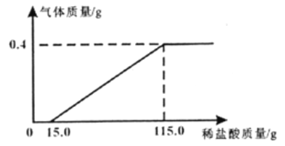
(1)生成氢气的质量为________g;
(2)所用稀盐酸中溶质的质量分数为________;
(3)计算该铁片中Fe2O3的质量分数为_______________(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组为探究“铁丝和盐酸反应的快慢与什么因素有关”,取相同质量的铁丝和足量的盐酸反应得到下表中的三组实验数据,请回答下列问题:
实验编号 | 盐酸的质量分数/% | 反应温度/°C | 铁丝消失的时间/s |
① | 3 | 20 | 300 |
② | 6 | 20 | 200 |
③ | 6 | 40 | 40 |
(1)写出铁丝和盐酸反应的化学方程式:________________。
(2)实验②和③可探究________对铁丝和盐酸反应快慢的影响。若欲探究浓度对铁丝和盐酸反应快慢的影响,应选择的实验编号是____________。
(3)根据上表中的实验数据,可得出的结论是_______(写出一点即可)。
(4)如果把上表中实验②的反应温度改为25°C,请推测铁丝消失的时间t的取值范围:__________。
(5)实验除了用铁丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量该反应的快慢吗?你的方法有________(写一点即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com