
【题目】运用溶解度表与溶解度曲线回答下列问题:
温度/°C | 10 | 30 | 50 | 60 | |
溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
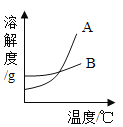
(1)B是 _____________(填“氯化钠”或“硝酸钾”)的溶解度曲线。
(2)60℃时,向100g水中加入100g硝酸钾,所得溶液的溶质质量分数为_____________,当该溶液从60℃降温到30℃时,析出晶体的质量为_____________g。
(3)现有50℃A物质的不饱和溶液,在不减少溶剂的情况下,欲使其变成饱和溶液,下列措施肯定不能实现的是_____(填序号)。
①降低温度 ②升高温度 ③加入A物质
【答案】氯化钠 50% 54.2 ②
【解析】
分析氯化钠和硝酸钾的溶解度表和曲线,解答相关问题。
(1)根据溶解度表,在10℃时氯化钠的溶解度大于硝酸钾的溶解度,在30℃时氯化钠的溶解度小于硝酸钾的溶解度,所以B是氯化钠的溶解度曲线。
(2)在60℃时,硝酸钾的溶解度为110g,向100g水中加人100g硝酸钾, 100g硝酸钾完全溶解在100g水中,所得溶液的溶质质量分数为![]() 。在30℃时硝酸钾的溶解度为45.8g,也就说100g水中最多能溶解硝酸钾45.8g,当该溶液从60℃降温到30℃时,析出晶体的质量为
。在30℃时硝酸钾的溶解度为45.8g,也就说100g水中最多能溶解硝酸钾45.8g,当该溶液从60℃降温到30℃时,析出晶体的质量为![]() 。
。
(3)A物质的溶解度是随温度的升高而增大,现有50℃A物质的不饱和溶液,在不减少溶剂的情况下,欲使其变成饱和溶液,可以采用降低温度或加入A物质,而升高温度A物质的溶解度增大,不可能变成饱和溶液。故选②。


科目:初中化学 来源: 题型:
【题目】如图是实验室常用的两种气体制备、收集或净化的多种功能装置。
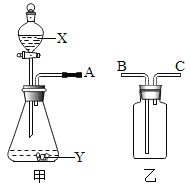
(1)若制备的气体是氢气,且产生的气体中不含有酸性杂质气体,则试剂X常用_____,用图示的乙装置收集氢气,A端应与_____(填“B”或“C”)端相连。
(2)若制备的气体是氧气,且Y是黑色粉末,则甲中发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镓是种奇妙的金属, 放在手心马上熔化,犹如荷叶上的水珠流来流去。请阅读信息后回答:

(1)金属镓________________(填物理性质)。
(2)镓原子的核电荷数为______;镓原子结构示意图中x的数值___________________。
(3)镓原子在化学反应中容易_____电 子(填“得到”或“失去”),镓的氧化物的化学式___________________。
(4)氮化镓(GaN)是第三代半导体材料,般采用GaCl3与NH3在一定 条件下反应制得,同时得到另一种化合物。该反应的化学方程式为___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学方程式表示下列事实
(1)纯净的氢气在空气中燃烧:_____。
(2)服用含氢氧化铝的药物治疗胃酸过多症:_____。
(3)向盛有少量碳酸钠溶液的试管里滴入澄清石灰水:_____。
(4)锻烧石灰石制取生石灰:_____。
(5)实验室用高锰酸钾制备氧气:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小华利用一瓶稀盐酸和相关的仪器,测定黄铜合金(Cu-Zn合金)样品的组成(不考虑黄铜中的其他杂质)。将30 mL稀盐酸分三次加入到10 g黄铜样品的粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 | 第二次 | 第三次 | |
连续加入稀盐酸的体积/mL | 10 | 10 | 10 |
生成氢气的质量/g | 0.08 | 0.08 | 0.04 |
(1)从上表数据分析,小华用10g合金粉末总共收集到氢气_____g
(2)求该合金中铜的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在拓展性课程活动中,小鑫利用以下常见物品验证酸的一些性质。
[实验物品]白醋(含3%的醋酸)、食品干燥剂(主要成分是CaO)、鸡蛋壳、牵牛花汁液、铁钉、纯碱。
[查阅资料]牵牛花汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝色。
[实验探究]
实验序号 | 实验操作 | 实验现象 | 实验结论或解释 |
一 | 将牵牛花汁液滴人白醋中 | 溶液显红色 | 白醋显____(填“酸”“中”或“碱”)性。 |
二 | 将足量的白醋加入放有铁钉的试管中 | 没有看到明显的气泡产生 | / |
三 | 在鸡蛋壳上滴加白醋,将产生的气体通入澄清石灰水中 | 有气泡产生,澄清石灰水变浑浊 | 写出澄清石灰水变浑浊的化学反应方程式:____ |
四 | 向白醋中加入纯碱 | 有气泡冒出 | 白醋能与碱反应 |
[交流与评价]
(1)小鑫对实验二中的现象很疑惑,于是提出猜想:气泡不明显可能与酸的浓度和种类有关。
要验证与酸的浓度有关,应选择下列试剂中的_____________(填字母)。
A 3%的盐酸 B 5%的醋酸 C 5%的盐酸
(2)小鑫想利用pH试纸进一步测定白醋的酸碱度,具体操作方法是____________________。
(3)小露认为实验四不能得到“白醋能与碱反应”的结论,理由是_________________。
[实验验证]小露利用已有物品验证酸与碱的反应,请你帮助完成下列实验设计。
步骤 | 操作 | 现象 |
1 | 将食品干燥剂加入适量清水中,搅拌后静置 | 放出大量的热 |
2 | 取步骤1中的上层清液, | ___________ |
[反思总结]科学来源于生活,生活中的许多事物能更好地帮助我们学习和理解科学。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国自2018开始对首艘001A型国产航母进行海试,这标志着我国在航海及军事领域取得重大突破。生产航母需要用到许多金属材料,根据所学知识填空。
(1)常温下大多数金属都是固体,但体温计中的金属却是液体,该金属是___________。
(2)建造航母使用了钛合金,构成金属钛的粒子是______ ( 填“原子”“分子”或“离子”) ,工业制取钛的反应为: ![]() ,X的化学式为___________。
,X的化学式为___________。
(3)金属矿物资源储量有限,且不能再生,请说出一种保护金属资源的方法:________。
(4)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是___________(填序号)。
A.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B. ZnCl2 溶液中加入足量铁粉后,再加入CuCl2溶液
C. ZnCl2 溶液中加入足量铜粉后,再加入铁粉
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年“五·一”假期,小丽随爸爸到乡下省亲,期间看到许多漂亮的大理石,于是好带了一些回来,想去学校实验室测定这此大理石中CaCO3的含量。他称取了20克大理石样品置于烧杯中,然后将250g稀盐酸分成五等份,依次加入烧杯充分反应,记录有关实验数据如下表所示(大理石中其他分均不溶于水,也不参与化学反应)。
加入次数 | 一 | 二 | 三 | 四 | 五 |
加入稀盐酸的质量 | 50 | 50 | 50 | 50 | 50 |
烧杯中剩余固体的质量 | 15 | 10 | 5 | 5 | m |
试求:(1)m的值应为_____;
(2)实验中大理石样品所含CaCO3的质量分数?_____
(3)实验中所用稀盐酸的溶质质量分数?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)化学用语是最简明、信息丰富、国际通用的语言,请用化学用语填空:
①2个铝原子____________________。
②二氧化氮分子____________________。
③3个镁离子____________________。
④五氧化二磷中氧元素的化合价____________________。
(2)写出符号“2H2O”中数字的含义: H2O前面的“2”表示____________________。H右下角的“2”表示____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com