
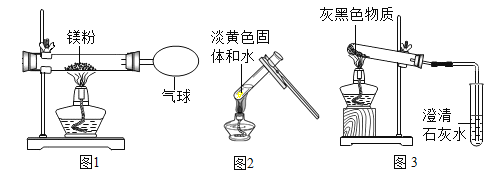
【题目】小明为验证质量守恒定律,做了镁粉在空气中燃烧的实验(如图1),该反应的化学力程式是______。实验结束,他发现镁粉在空气中充分燃烧后,产物中还有少量黄色固体。为了弄清黄色固体的成分,小明进行了如下实验探究:
(查阅资料)
①镁能与氮气剧烈反应生成黄色的氮化镁(![]() )固体。
)固体。
②氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(设计实验)小明用图2所示的实验(部分操作没有画出),验证黄色固体为![]() ,请完成下列实验报告。
,请完成下列实验报告。
操作步骤 | 实验现象 | 实验结论 |
取少量黄色固体于试管中,加入适量水,加热,并将湿润的红色石蕊试纸放在试管口 | _______ | 黄色固体为 |
(交流与思考)小明发现久置的镁条上有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?他叫来了小亮、小红一起进行了实验探究:
(猜想)小明认为可能是![]() ;
;
小亮认为可能是![]() ;
;
小红认为可能是![]() 。
。
小红认为小明的猜想是错误的,其理由是___________。
(查阅资料2)①![]() 受热分解产生两种氧化物。
受热分解产生两种氧化物。
②![]() 受热分解产生三种氧化物。
受热分解产生三种氧化物。
(实验探究)小亮进行实验(见图3),发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体。
(实验分析)实验后,小亮认为小红的猜想也是错误的,其理由是___________。
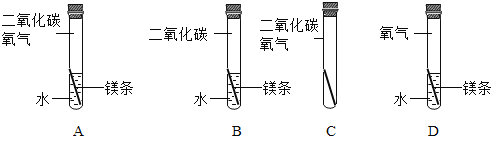
(实验反思)要验证小亮的猜想,实际上只需证明灰黑色“外衣”的形成是否需要二氧化碳即可。为了证明这一猜想,需要进行如图所示实验中的___________(填序号,下同)和___________。
【答案】 有气泡产生,湿润的红色石蕊试纸变蓝
有气泡产生,湿润的红色石蕊试纸变蓝 ![]() 是白色固体
是白色固体 ![]() 中没有碳元素 A D
中没有碳元素 A D
【解析】
[题文]
镁粉在空气中燃烧生成氧化镁,反应的化学方程式为: 。
。
[猜想]
小明认为可能是![]() ,而
,而![]() 是白色固体,所以小明猜想是错误的。
是白色固体,所以小明猜想是错误的。
[实验分析]
实验后,澄清石灰水变浑浊,说明有二氧化碳生成,所以小红的猜想也是错误的,其理由是![]() 中没有碳元素,分解不能生成二氧化碳气体。
中没有碳元素,分解不能生成二氧化碳气体。
[实验反思]
要验证小亮的猜想,实际上只需证明灰黑色“外衣”的形成是否需要二氧化碳即可。为了证明这一猜想,根据控制变量法,需要进行A实验和D实验即可,因为A、D中的水、镁和氧气条件相同,A有二氧化碳,D没有二氧化碳,如果A中镁条表面形成灰黑色“外衣”,而D中镁条表面不变灰黑色,则小亮的猜想正确,反之则错误。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:初中化学 来源: 题型:
【题目】某化学兴趣小组设计了一组“吹气球”实验,三套装置如下图:
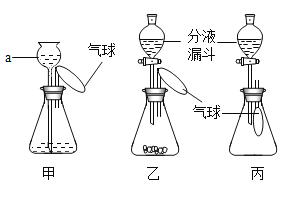
(1)甲装置:
①仪器![]() 的名称为_____________;
的名称为_____________;
②向![]() 中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性___________
中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性___________
(2)乙装置:
①若生成![]() 使气球胀大,则锥形瓶中所装的固体物质可以是__________;反应的方程式为:____________
使气球胀大,则锥形瓶中所装的固体物质可以是__________;反应的方程式为:____________
②若生成![]() 使气球胀大,则反应的化学方程式为___________
使气球胀大,则反应的化学方程式为___________
③若锥形瓶中装有![]() 固体,分液漏斗中加入少量水,则气球胀大的主要原因是_________
固体,分液漏斗中加入少量水,则气球胀大的主要原因是_________
(3)丙装置:若锥形瓶中盛满![]() ,欲使气球胀大,则分液漏斗中的液体可以是_____________
,欲使气球胀大,则分液漏斗中的液体可以是_____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】冬季雾霾频发。某校社会实践小组的同学们,对某地区雾霾的成分、成因、危害及防治产生了浓厚的兴趣并开启了项目性学习之旅。
[信息检索]雾是浮游在空中的大量微小水滴。霾是可吸入颗粒物浓度较高造成的能见度较低的现象。霾的主要成分肯含有可溶性硫酸盐、硝酸盐、铵盐、不溶性有机物、黑碳、金属元素和其它元素。
[提出问题]探究霾中是否含有黑碳
活动:同学们设计了如图所示的创新实验。( 图中残渣为霾的样品)
[实验步骤]①滴入过氧化氢溶液制取O2,排出装置内空气后,再在导管口接上气球。
②向右边的凹槽内滴入澄清的石灰水。
③接通电源,用用热电阻丝点燃残渣。
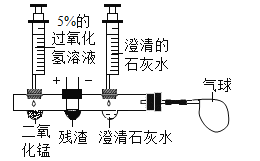
[实验现象]残渣剧烈燃烧,澄清石灰水浑浊,气球变大。
上述现象中澄清石灰水变浑浊的方程式是____,针对上述活动你得到的结论是_____,理由是_________。
[交流研讨][能力发展]请你联系实际填写关于雾霾的问卷调查表:
项目 | 雾霾频发的成因 | 控制雾霾频发的做法 | 政府采取的应急措施 |
① | 能源结构不同 | 推广太阳能发电 | 人工降雨 |
② | 烧散煤取暖 | _________ | 向空中或地面洒水 |
③ | _____________ | 推广新能源汽车 | 私家车限号出行 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学校的元旦联欢会上,某同学表演了“水能生火”魔术.他向包有过氧化钠(![]() )粉末的脱脂棉上滴水,脱脂棉燃烧起来.小晨很感兴趣,于是他和同学们进行探究.
)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小晨很感兴趣,于是他和同学们进行探究.
(提出问题)过氧化钠与水反应生成什么物质?为什么脱脂棉会燃烧?
(查阅资料)物质燃烧需要同时满足以下条件:可燃物;温度达到可燃物的着火点(即物质燃烧所需的最低温度);可燃物与氧气接触.
(猜想假设)①可能有一种气体和另一种物质生成 ②反应过程中可能有能量变化
(设计装置)实验装置如图所示
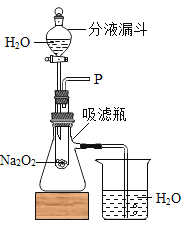
(实验探究)
实验一:探究反应后生成的气体是什么?
(1)另取少量未包有过氧化钠的脱脂棉,直接滴加水,脱脂棉没有燃烧.
(2)如图所示,打开装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是______.
(3)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:_________________.
实验二:继续探究反应后生成的另一种是什么?
小杨猜想另一种物质是![]() ,小晨认为不可能.小晨的依据是:_______________.
,小晨认为不可能.小晨的依据是:_______________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是一种常见的物质,许多化学实验都用到了水。
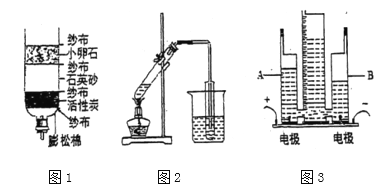
(1)水的净化
①图1是简易净水装置,其中活性炭的作用是_____,小明可用_______来区分净化后的水是硬水还是软水。
②图2是蒸馏装置,与图1相比,图2的净化效果更___________(填“好”或“差”)。
(2)水的组成
图3是简易水电解器,其发生反应的化学方程式是______,通过实验我们知道水由______组成。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】家庭食用碱的主要成分是 Na2CO3,为测定该食用碱中 Na2CO3 的质量分数, 某同学进行了以下实验取 40g 食用碱,平均分为四份,然后分别加入一定质量分数的 CaCl2 溶液,实验数据见下表(假设该食用碱中不含难溶性杂质且杂质均不与CaCl2溶液产生沉淀)

请分析表中数据回答并计算:
(1)m =__________g
(2)40g 该食用碱与足量 CaCl2 溶液反应,最多生成沉淀质量为__________g
(3)该食用碱中 Na2CO3 的质量分数是__________?(写出计算过程,答案精确到 0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家正在设法研究探索“反物质”,所谓的“反物质”是由“反粒子”构成的,“反粒子”与其对应的正粒子具有同的质量和相同的电量,但电荷的符号相反。则下列描述不正确的是
A.“反氢原子”的原子结构示意图为: 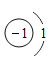
B.“反粒子”中不存在“反中子”
C.一个碳12原子的质量约是一个“反质子”质量的12倍
D.“反氧原子”是由8个带负电荷的质子和8个带正电荷的电子构成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,人类的日常生活与工农业生产都离不开水.
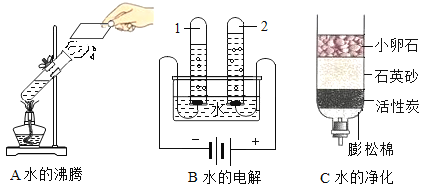
(1)如图所示的3个实验,A中水发生了_________(填“物理”或“化学”)变化;B中试管2内得到的气体为__________;该实验说明水是由___________组成的。C中活性炭的作用是__________,经过此净水器得到的水仍然不是纯水,若想得到纯水可采用的方法是__________。
(2)硬水会给生产、生活带来许多不便。
①检验一份自来水水样是硬水还是软水的方法是向水样中加入___________来鉴别,若看到___________的现象证明是硬水。
②生活中可以通过煮沸的方法来降低水的硬度,硬水在煮沸过程中发生的化学反应之一是:碳酸氢钙→ 碳酸钙+二氧化碳+水,该反应属于基本反应类型中的______反应。
(3)节约用水是每个公民的义务,下列用水方式应该提倡的是_________(填字母序号)。
A用漱口杯接水刷牙 B不间断地边流水边洗衣
C用淘米水、洗菜水浇花、冲厕所 D用喷灌、滴灌的方法浇灌农田和园林
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学们利用学校开放实验室提供的稀盐酸、氯化钠溶液和酚酞溶液进行了如下图所示的传统实验,成功探究出了久置氢氧化钠固体的变质情况。
传统实验研究:
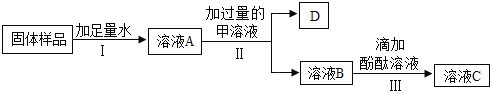
(1)图中甲溶液最好选择_____。(填“稀盐酸”或“CaCl2溶液”)。(资料: CaCl2溶液显中性)
(2)若图中步骤II和步骤III出现:_____现象时,则说明氢氧化钠固体部分变质。
(3)若图中步骤II和步骤III出现:_____现象时,则说明氢氧化钠固体完全变质。
(4)写出步骤II中发生的化学反应方程式: _____。
但在反思的过程中,同学们对为何选用氢氧化钠溶液及其用量的控制对检验变质程度的影响仍然比较困惑,在老师的指导下,兴趣小组的同学们分别利用数字化实验来解决他们的疑惑。
数字化实验研究:1. 实验仪器和药品:仪器:数据采集器、pH传感器、泵动式二氧化碳传感器、电脑、磁力搅拌器、酸式滴定管、铁架台、弹簧夹。
药品:NaOH部分变质的溶液样品、碳酸钠溶液(模拟氢氧化钠完全变质后的溶液)、稀盐酸、CaCl2溶液。
2.分组实验
第一组实验:实验装置如图1所示,用酸式滴定管逐滴滴加稀盐酸和泵动循环二氧化碳传感器探究氢氧化钠溶液的变质情况,形成的“时间-CO2”曲线图(如图3、图4)。
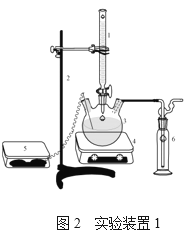
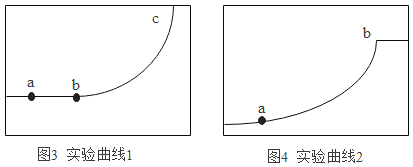
(5)比较分析图3和图4:两图中的a点之前都尚未加入稀盐酸,反应尚未开始,曲线没有发生变化。图3中,a点和b点之间平稳略有轻微上升,b点之后曲线开始明显上升。说明a点到b点之间滴入的稀盐酸主要与_____反应,体现_____优先原理;说明a点到b点略有轻微上升的原因:_____。图4中a点开始滴加稀盐酸,几乎立即产生二氧化碳,说明氢氧化钠_____(“部分”或“完全”)变质。
第一组同学的反思:在传统实验中,没有使用酸式滴定管逐滴滴加稀盐酸,且没有灵敏数字传感器的实验条件下,选用稀盐酸只能检验氢氧化钠是否变质,很难判断氢氧化钠的变质成都。
第二组实验:实验装置如图2所示。用酸式滴定管逐滴滴加CaCl2溶液和PH传感器探究氢氧化钠溶液的变质情况,形成的“时间-pH”曲线图(如图5、图6)

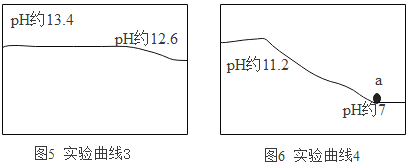
(6)同学们在实验二中都加入课过量的CaCl2溶液,比较分析图5和图6:图5中pH曲线的起止值,说明结束后,溶液是_____性,氢氧化钠_____(“部分”或“完全”)变质。图6中,溶液pH曲线逐渐下降至a点后pH=7,继续滴加CaCl2溶液pH不变,说明原因:_____。
第二组同学的反思:在传统实验的步骤II中需要加入过量CaCl2溶液的目的是_____。
实验反思:传统实验和现代数字化实验是相辅相成的,可以互为补充。化学实验教学要靠这两条腿协调走路。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com