
【题目】戴口罩、勤洗手,给自己居住、生活的环境消消毒,都是预防新型冠状病毒感染的有效方法。其中“84”消毒液能用于日常生活的消毒灭菌。某化学兴趣小组对一瓶 敞口放置的“84”消毒液成分产生兴趣,在老师的指导下进行如下探究:
(提出问题)该敞口久置的“84”消毒液中含有哪些溶质?
(查阅资料)(1)“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO 为有效成分,有腐蚀性,并易与空气中 CO2 反应(2NaClO+CO2+H2O=2HClO+Na2CO3)。
(2)次氯酸(HClO)溶液和次氯酸钠(NaClO)溶液都具有漂白、杀菌、消毒功效。
(3)HClO 不稳定,受热或光照易分解。
(提出猜想)I.“84”消毒液没有变质
II.____________
III.“84”消毒液完全变质
(设计方案)为验证猜想,设计如下方案:
实验操作 | 实验现象 | 结论 |
(1)另取该消毒液少量于试管中,滴加足量 BaCl2 溶液,振荡 | 产生白色沉淀 | 猜想________不成立,反应的化学方程式是____________。 |
(2)向盛有有色布条的烧杯中滴加该消毒液适量,放置一段时间 | 有色布条_________。(填“褪色”或“不褪色” | 猜想 II 不成立,猜想 III 成立 |
(得出结论)综上所述,该敞口放置的“84”消毒液中溶质一定有____________________。
(拓展延伸)
(1)次氯酸钠与盐酸反应会生成有毒的黄绿色气体单质,该气体单质是____________,因此,“84”消毒液____________________(填“能”或“不能”)与洁厕灵(主要成分为盐酸)混合使用。
(2)欲用 40%的 NaClO 溶液稀释配制 25%的溶液 400g,需要加水__________g。
【答案】“84”消毒液部分变质 I Na2CO3+BaCl2═BaCO3↓+2NaCl 不褪色 氯化钠、碳酸钠 氯气 不能 150
【解析】
[提出猜想]根据I.“84”消毒液没有变质和III.“84”消毒液完全变质,可推出II是“84”消毒液部分变质;
[设计方案](1)另取该消毒液少量于试管中,滴加足量 BaCl2 溶液,振荡,产生白色沉淀,是因为氯化钡和碳酸钠反应生成了碳酸钡沉淀和氯化钠,反应的反应化学方程式为:Na2CO3+BaCl2═BaCO3↓+2NaCl,故猜想I不成立;
(2)向盛有有色布条的烧杯中滴加该消毒液适量,放置一段时间,布条不褪色,说明该消毒液中不含有次氯酸钠、次氯酸;
[得出结论]根据查阅资料中提供的信息可知,该敞口久置的“84”消毒液中溶质有氯化钠、碳酸钠;
[拓展延伸](1)由题意可知84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,氯化钠和稀盐酸不反应,因此是次氯酸钠和稀盐酸反应生成氯化钠、水和氯气,因此,“84”消毒液不能与洁厕灵(主要成分为盐酸)混合使用;
(2)根据用水稀释前后溶质的质量不变可知,需要加水的质量:![]()


科目:初中化学 来源: 题型:
【题目】人们的日常生活离不开金属。
(1)奥运场馆“鸟巢”使用了大量的钢铁。钢铁与_______________直接接触容易生锈造成损失,在钢铁表面涂油、刷漆等,都能防止钢铁生锈。
(2)实验室用图示实验模拟炼铁反应的原理,回答下列问题。
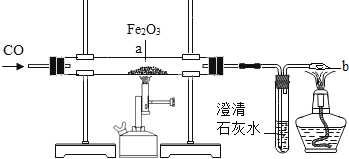
a处可观察到的现象是__________;b处点燃酒精灯的目的是______________。
(3)取某溶液少许放入试管中,向其中加入适量的铁粉,充分反应后,向试管中继续加入足量的另一种金属,溶液中 FeSO4 的质量随时间的变化如图所示。试
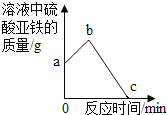
①若 b 点表示的溶液中只含一种溶质,则 a 点表示的溶液中的溶质可能是_____(写出 1 种情况即可),从 a 点到 b 点的过程中,反应的化学方程式是_____。
②若从 b 点到 c 点的过程中,溶液的质量不断增加,则加入的另一种金属是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学课上,同学们利用下列分组实验来探究碱的化学性质:
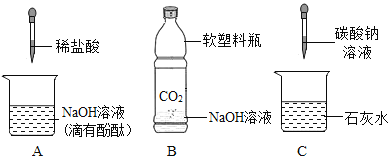
(1)做B组实验的同学看到了明显的现象是_____。
(2)实验结束,同学们将废液(废渣除外)倒入同一只废液缸中,最后发现废液呈无色。
[提出问题]废液中含有什么物质?
[猜想与假设]通过分析上述实验,同学们猜想:废液中一定含有_____。废液中的溶质(忽略酚酞)的成分引发了同学们的热烈讨论,下面是两位同学的发言:
小龙:氯化钠
小江:氯化钠、氯化氢
还可能是_____或_____;
[实验验证]小美同学对可能含有的溶质进行确定,取一定量的废液,向其中滴加几滴碳酸钠溶液,只看到_____的现象,小美确定小江猜想正确;
[反思与评价]小美同学由实验得出的结论_____(填写“正确”或“不正确”)。
[结论与应用]在得知小江同学猜想错误后,老师要求同学们从废液中回收氯化钠固体(利用已有的一种化学药品),你的具体操作方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答有关问题,
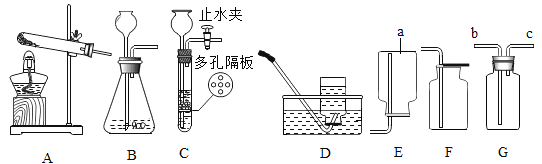
(1)装置图中仪器a的名称为_____。
(2)用氯酸钾和二氧化锰混合制取氧气,可选用的发生装置是_____(填字母),写出该反应的化学方程式_____;若用D装置收集氧气,当导管口气泡_____冒出时,再把导管口伸入盛满水的集气瓶。
(3)实验室用B装置制取二氧化碳的化学方程式为_____,如果用G装置收集气体,气体应从_____(填“b”或“c”)端通入;用C装置代替B装置,收集所需的气体量后,对C装置进行的操作是_____。
(4)氮的氧化物(NO2)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NO2还原成N2,某同学在实验室中对NH3与NO2的反应进行了探究。
(资料:NO2有毒,常温下为红棕色,实验中常用氢氧化钠溶液进行尾气处理;同温同压下,不同气体的体积之比等于分子个数之比。)
现将收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图装置进行实验。
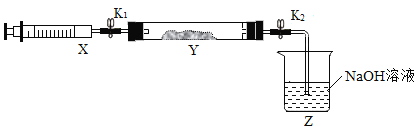
(Ⅰ)打开K1,推动注射器活塞,使X中的气体缓慢通入Y中,Y管中的现象_____,反应方程式是_____。
(Ⅱ)将注射器活塞退回原处并固定,待装置恢复到室温,Y中有少量水珠。
(Ⅲ)打开K2,观察到的现象_____,原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学的一些基本实验,请回答相关问题:
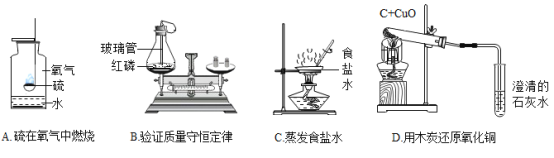
(1)A实验中集气瓶内水的作用是_____。
(2)B实验中气球的作用是_____。
(3)C实验过程中,当蒸发皿中出现_____时,停止加热。
(4)D实验的实验现象是_____。酒精灯网罩的作用是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
酸奶是以新鲜的牛奶为原料,经过杀菌后再向牛奶中添加有益菌,发酵后,再冷却灌装的一种牛奶制品。酸奶不但保留了牛奶的营养,而且某些方面更优于牛奶。
酸奶比牛奶更容易被人体消化吸收,因为在发酵过程中,牛奶中约20%的糖、蛋白质被分解成为小分子,同时产生人体所必需的多种维生素。发酵后产生的乳酸可有效提高钙、磷在人体中的吸收。
酸奶中含有大量乳酸菌,乳酸菌把乳糖转化成乳酸,使得牛奶的酸度升高。酸度可以影响酸奶的口感和营养。研究者选取某种市面常见的酸奶进行实验,数据如下图所示:

酸奶喝得过多会导致胃酸过多,影响胃黏膜及消化酶的分泌,对于健康的人来说,每天250克左右是比较合适的。而且最好不要在空腹时喝含有乳酸菌的酸奶,一般选择饭后喝效果比较好。
近年来,常温酸奶逐渐流行起来。常温酸奶和低温酸奶的加工工艺不同。低温酸奶仅在生牛乳状态时经过一道灭菌处理,乳酸菌可以存活其中,但保存条件苛刻,需低温存储,且保质期较短。而常温酸奶需要进行“巴氏灭菌热处理”,该处理方式会杀灭一切细菌,所以可以常温保存较长时间。
酸奶营养美味,建议在购买的时候,仔细看配料表,根据需求去选择。
依据文章内容回答下列问题。
(1)新鲜牛奶制作酸奶的过程属于_________变化(填“物理”或“化学”)。
(2)酸奶是补钙佳品,这里的“钙”指的是_________(填字母序号)。
A.钙元素 B.钙原子 C.钙单质
(3)酸奶中的蛋白质更易消化和吸收,原因是____________。
(4)由图中数据可知,影响酸奶酸度的因素有____________。
(5)下列说法中,不合理的是____________(填字母序号)。
A.酸奶营养丰富,但要注意适量饮用
B.酸奶适宜在饭前饮用
C.常温酸奶中含有丰富乳酸菌
D.酸奶更有利于人体对钙的吸收
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一变质的氢氧化钠样品,为测量样品中碳酸钠的质量分数,小明称取10.0g样品于烧杯中,将100g足量的稀盐酸慢慢加入到烧杯中。充分反应后,测得烧杯内剩余物质的质量为107.8g。(假设产生的气体完全逸出)。
(1) 生成的二氧化碳气体质量为: 。
(2) 计算样品中碳酸钠的质量分数 (写成计算过程)。
(3) 变质的氢氧化钠占未变质时氢氧化钠总质量的质量分数 (精确度0.1%)。
(4) 现用一定质量的氢氧化钠样品与稀盐酸反应,消耗稀盐酸的质量与其变质的程度 (填“有关系”或“无关系”),理由是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明了解到氢氧化钠有腐蚀性,欲配制 50 g 质量分数为 14%的氢氧化钠溶液制作“叶脉书签”,下列关于配制该溶液的说法不正确的是( )
①若用氢氧化钠固体配制,需称取氢氧化钠固体 7.0 g
②用托盘天平称氢氧化钠固体时,在两盘各放一张质量相等的纸
③选用 200 mL 量筒量取所需水的体积
④实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和试剂瓶,
⑤用量筒量取水时,俯视读数,配得溶液的溶质质量分数偏小
A.①③B.②③⑤C.③⑤D.②④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com