
| A. | 都发光 | B. | 都放热 | C. | 都很剧烈 | D. | 都需加热或点燃 |
分析 燃烧是指可燃物跟空气中的氧气发生的发光、发热的比较剧烈的氧化反应;有些氧化反应进行的比较缓慢,甚至不溶易被察觉,这样的氧化称为缓慢氧化;由缓慢氧化引起的自发燃烧叫自燃.它们的共同点是:都是氧化反应,都能放出热量.
解答 解:A、缓慢氧化不发光,故选项错误;
B、它们的共同点是:都是氧化反应,都能放出热量.故选项正确;
C、缓慢氧化进行的比较缓慢,故选项错误;
D、缓慢氧化和自燃就不需要加热或点燃,故选项错误;
故选B.
点评 本考点考查了燃烧、爆炸、缓慢氧化和自燃的关系,要加强记忆它们的概念,相同点和不同点,在理解和比较的基础上进行应用.本考点的基础性强,主要出现在选择题和填空题中.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:选择题
| A. | 2Cu中的“2”表示2个铜元素 | |
| B. | Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷 | |
| C. | H2S中的“2”表示1个硫化氢分子中含 有2个硫原子 | |
| D. | S2-表示-2价的硫元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.
如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.| 我对气体的猜想是 | |
| 我猜想的依据是 |
| 实验方法及操作 | 可能观察到的现象及结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| $\stackrel{-1}{Cl}$ | $\stackrel{-2}{O}$ | $S\stackrel{-2}{{O}_{4}}$ | |
| $\stackrel{+1}{Na}$ | |||
| $\stackrel{+2}{Ca}$ | |||
| $\stackrel{+3}{Fe}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
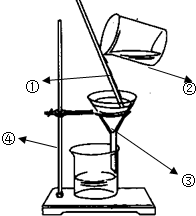 (1)指出图中所标的仪器的名称
(1)指出图中所标的仪器的名称查看答案和解析>>
科目:初中化学 来源: 题型:解答题
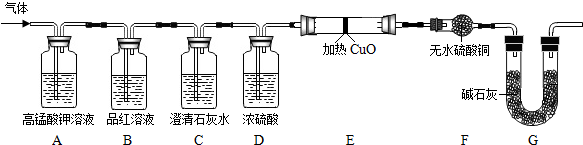
| 实验过程 | 实验现象 | 实验结论 |
| 1°气体通过高锰酸钾溶液. | 高锰酸钾溶液褪色. | 猜想4成立 |
| 2°气体通过澄清石灰水. | 澄清石灰水变浑浊. | |
| 3°气体通过氧化铜和无水硫酸铜. | 黑色氧化铜变红色,无水硫酸铜变蓝色(合理即可). |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com