
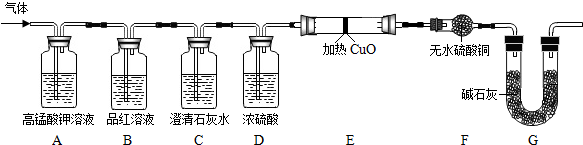
| 实验过程 | 实验现象 | 实验结论 |
| 1°气体通过高锰酸钾溶液. | 高锰酸钾溶液褪色. | 猜想4成立 |
| 2°气体通过澄清石灰水. | 澄清石灰水变浑浊. | |
| 3°气体通过氧化铜和无水硫酸铜. | 黑色氧化铜变红色,无水硫酸铜变蓝色(合理即可). |
分析 (1)根据质量守恒定律化学反应前后原子的种类和个数都不变分析;
(2)根据碱性干燥剂不能干燥酸性气体分析;
(3)根据质量守恒定律反应前后元素的种类不变结合表格实验进行大胆的猜想;
【实验探究】根据二氧化硫、二氧化碳及氢气的性质进行分析.
解答 解:(1)根据质量守恒定律化学反应前后原子的种类和个数都不变,反应前有6个硫原子,反应后出现了3个硫原子,因此缺少3个硫原子,m=3;反应前是12个氢原子,因此n=6,6个水分子提供12个氢原子;故答案为:3;6;
(2)碱石灰是常用的干燥剂,主要成分是氢氧化钠固体和氧化钙,显碱性,而二氧化硫的水溶液显酸性,因此不能用碱石灰干燥;故答案为:不能;
(3)根据质量守恒定律反应前后元素的种类不变结合前3个猜想,因此猜想4可以是多种气体的混合,如含有SO2、CO2、H2(或含有SO2、CO2、不含H2,答一种情况即可);
资料显示二氧化硫能够使高锰酸钾溶液褪色,检验二氧化碳要用澄清的石灰水,氢气具有还原性,还原氧化铜产生水,水能使无水硫酸铜变成蓝色;
故答案为:
猜想4:含有SO2、CO2、H2(或含有SO2、CO2、不含H2,答一种情况即可);
【实验探究】
| 实验过程 | 实验现象 | 实验结论 |
| 1°气体通过高锰酸钾溶液. | 高锰酸钾溶液褪色. | 猜想4成立 |
| 2° 气体通过澄清石灰水. | 澄清石灰水变浑浊. | |
| 3°气体通过氧化铜和无水硫酸铜. | 黑色氧化铜变红色,无水硫酸铜变蓝色(合理即可) |
点评 本题为信息给予题,完成此类题目,可以依据题干提供的内容,获取有用的信息,结合已有的知识进行分析,能够考查学生的分析问题能力.


科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入过量的氯化钙溶液; | 白色沉淀产生 | 该反应的化学方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl; |
| (2)将上述反应后的混合物过滤,取滤液加入酚酞试液.. | 溶液变红色. | 证明猜想Ⅱ正确 |

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 第一组 | 第二组 | 第三组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | 10 | 20 | 30 | 40 | 50 | 31 | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
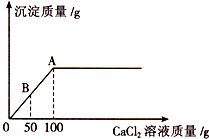 五一节后,小丽带着愉快的心情返回学校.当她来到实验室时,意外地发现实验桌上有瓶敞口放置已久的NaOH溶液,由此,激发了她的探究欲望.
五一节后,小丽带着愉快的心情返回学校.当她来到实验室时,意外地发现实验桌上有瓶敞口放置已久的NaOH溶液,由此,激发了她的探究欲望.| 阴离子 阳离子 | 0H- | N03- | C1- | C032- |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不溶 |
| Ca2+ | 微溶 | 溶 | 溶 | 不溶 |
| Cu2+ | 不溶 | 溶 | 溶 | 不溶 |
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液 | 产生白色沉淀,溶液变红 | NaOH溶液部分变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
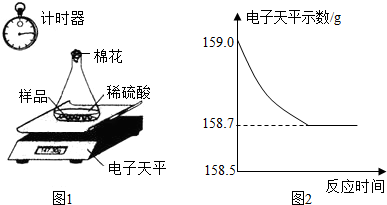
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
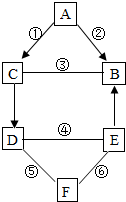 如图A、B、C、D、E、F都是初中化学常见的物质,其中B是常用于光合作用和灭火的气体.已知反应①、②、③的基本反应类型相同,反应④、⑤、⑥中,一个有沉淀生成,另一个有气体生成,还有一个没有明显现象.B、E不含相同元素,D、F只含一种相同元素.它们之间的关系如图所示.(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系)
如图A、B、C、D、E、F都是初中化学常见的物质,其中B是常用于光合作用和灭火的气体.已知反应①、②、③的基本反应类型相同,反应④、⑤、⑥中,一个有沉淀生成,另一个有气体生成,还有一个没有明显现象.B、E不含相同元素,D、F只含一种相同元素.它们之间的关系如图所示.(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 西瓜汁呈碱性 | |
| B. | 上述呈酸性的物质中酱油的酸性最强 | |
| C. | 肥皂水能使无色酚酞溶液变红 | |
| D. | 玉米粥的碱性比牙膏的碱性强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com