
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A | B | C | D | |
实验装置 |
硫在氧气中燃烧 |
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
排水法收集氧气 |
解释 | 集气瓶中的水: 吸收放出的热量 | 量筒中的水: 通过水体积的变化得出氧气体积 | 集气瓶中的水: 冷却溅落熔融物,防止集气瓶炸裂 | 集气瓶中的水: 排出瓶内的空气 |
A. AB. BC. CD. D
【答案】A
【解析】
A、硫在氧气中燃烧生成二氧化硫,集气瓶中水的主要作用是吸收反应生成的二氧化硫,以防止二氧化硫污染环境,该选项解释没有体现水的主要作用;
B、红磷在空气中燃烧生成五氧化二磷,通过进入集气瓶中的水的体积可以判断空气中氧气的含量,量筒中的水的主要作用是通过水体积的变化得出氧气的体积,该选项解释体现了水的主要作用;
C、铁在氧气中燃烧时容易形成高温熔融物,并且高温熔融物容易溅落,集气瓶中的水的主要作用是冷却溅落融熔物,防止集气瓶炸裂,该选项解释体现了水的主要作用;
D、利用排水法收集氢气,开始时装满水是排出集气瓶中的空气,后来是利用排出的水确定什么时间收集满氢气,故D体现了水的主要作用;
故选:A。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:初中化学 来源: 题型:
【题目】为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:
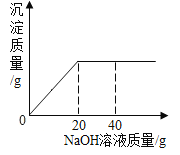
请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数为_________(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列如图所示图象中有关量的变化趋势与对应叙述关系正确的是( )
A. 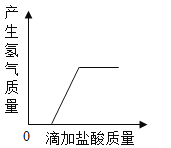 向一定质量的打磨光亮的锌片中滴加盐酸
向一定质量的打磨光亮的锌片中滴加盐酸
B. 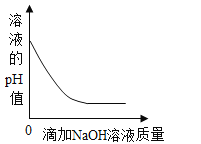 向一定质量的稀硫酸中滴加氢氧化钠溶液
向一定质量的稀硫酸中滴加氢氧化钠溶液
C. 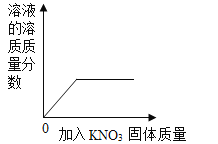 一定温度下向一定量水中加入KNO3固体
一定温度下向一定量水中加入KNO3固体
D. 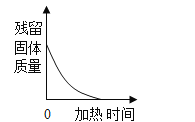 加热一定质量的高锰酸钾制取氧气
加热一定质量的高锰酸钾制取氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】NSR 技术通过 BaO 和 Ba(NO3)2 的相互转化实现 NOx(氮氧化物)的储存和还原,能有效降低柴油发动机在空气过量条件下的 NOx 排放。其工作原理如图所示。下列说法不正确的是
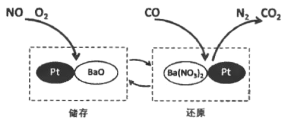
A. 降低 NOx 排放可以减少空气中酸雨的形成
B. 储存时,吸收 NOx (如 NO, NO2)的物质是 Pt
C. 还原时,发生的反应是: ![]()
D. 若有 28 g CO 参与反应,则生成 CO2 的质量为 44g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下水道堵塞是日常生活中经常遇到的问题,下水管里的淤积物主要为油污、食物残渣、毛发等。“管道通”可使堵塞的管道畅通无阻。化学兴趣小组对“管道通”中的物质进行了探究:

(查阅资料)
(1)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西,常用于疏通管道。
(2)铝粉呈银白色。铝粉与强酸、强碱溶液都能迅速反应放出氢气,同时放出大量热。
①铝与盐酸反应的化学方程式为_____。
②铝与氢氧化钠溶液反应的化学方程式为_____=2NaAlO2+3H2↑
(1)(猜想与验证)打开一盒“管道通”,内有一袋白色固体颗粒和一袋银白色粉末。
(1)猜想:白色固体颗粒为氢氧化钠。
实验操作 | 实验现象 |
①将几粒白色颗粒放在表面皿上,露置在空气中片刻。 | _____ |
②将几粒白色颗粒放入盛有少量水的试管中,并用手触摸试管外壁。 | 试管外壁温度升高 |
③向步骤②得到的溶液中放入一段羊毛线,加热一段时间。 | 羊毛线缩小 |
结论:白色固体颗粒为氢氧化钠。
(2)猜想:银白色粉末为铝粉。
实验操作 | 实验现象 |
①取少量该粉末于洁净的试管中,滴加稀盐酸,用手触摸 试管外壁,点燃反应产生的气体 | 产生大量气泡,试管外壁温度明显升高,气体燃烧产生淡蓝色火焰。 |
②取少量该粉末于洁净的试管中,滴加_____,用手触摸 试管外壁,点燃反应产生的气体 |
结论:银白色粉末为铝粉。
(应用)
(2)使用“管道通”时,先将银白色粉状固体添加入被堵塞的管道中,再加入白色固体颗粒,倒入一杯水,堵上管道口。管道内可能出现的现象是_____.(填序号)
A.管道内温度明显升高
B.产生大量气体
C.管道被疏通
(3)“管道通”内的两种物质必须密封保存,否则会发生变质。用化学方程式表示其中的原因:_____、_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】天然气与煤炭、石油等能源相比具有使用安全、热值高、洁净等优势。天然气的主要成分是甲烷,此外还含有少量的乙烷、丙烷、二氧化碳、一氧化碳等。
(1)天然气属于______________(填“混合物”或“纯净物”)。
(2)甲烷燃烧时发生的化学反应的微观示意图如下图所示。其中,![]() 表示碳原子,
表示碳原子,
![]() 表示氧原子,
表示氧原子,![]() 表示氢原子。
表示氢原子。
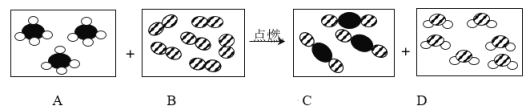
①A中分子为甲烷分子,甲烷分子是由________________构成。
②根据图示信息,写出甲烷燃烧反应的化学方程式______________________。
(3)甲烷不仅可以作为燃料,还可以用于制造多种物质。例如,在高温条件下,甲烷可以生成碳和氢气,该反应方程式为_______________________,基本反应类型为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线。
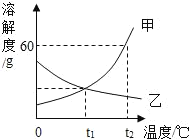
(1)在温度为_____℃时,甲、乙两种物质的溶解度相等;
(2)甲、乙两物质中,通过升温的方法能将接近饱和的溶液变为饱和溶液的是_____;
(3)t2℃时,将8g甲物质投入到10g水中,充分溶解后得到甲溶液的溶质质量分数为_____(精确到0.1%);
(4)用一定的方法,将乙的不饱和溶液变为饱和溶液,下列说法正确的是_____。
a溶剂的质量可能不变
b溶质质量分数一定变大
c溶液的质量可能不变
d溶质的质量一定变大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。某研究性小组对K2SO4和Mn3O4的制备展开了系列研究。
(一)以硫酸工业的尾气SO2制备K2SO4的工艺流程如下:
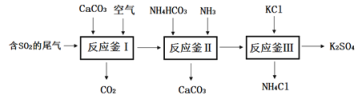
⑴钾肥K2SO4对农作物生长的作用是___________。
A.促进植物茎、叶生长,使叶色浓绿;
B.增强植物的抗寒、抗旱能力
C.增强植物的抗病虫害、抗倒伏能力
⑵反应釜I中发生的反应包括:①碳酸钙高温分解的化学方程式为________;
②CaO + SO2==CaSO3 ③ 2CaSO3+O2==2CaSO4
⑶反应釜III:向反应II 所得(NH4)2SO4溶液中加入KCl溶液充分反应后,经蒸发浓缩、过滤、洗涤、干燥等操作即可制得K2SO4产品。为提高K2SO4产品纯度,过滤时应控制反应液的温度范围为____________(填字母序号,如图为几种盐的溶解度曲线)。
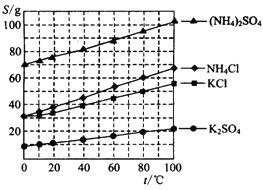
A.0℃-10℃ B. 20℃-30℃ C. 60℃-65℃ D. 80℃-90℃
⑷上述工艺流程中循环利用的物质是_______;证明产品K2SO4中不含杂质的实验方法是_______写出方法、现象)。
(二)实验室以SO2气体为原料制备少量高纯Mn3O4的操作步骤如下:
(步骤I)制备MnSO4溶液:在三颈烧瓶中(装置见图) 加入一定量MnO2和水,先通氮气,再通入SO2和N2混合气体,搅拌反应3小时。停止通SO2,继续反应片刻后过滤得MnSO4溶液。
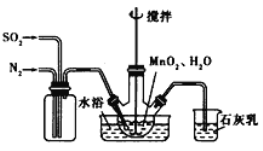
[资料1]亚硫酸(H2SO3)在Mn2+催化作用下被O2氧化为硫酸,硫酸与MnO2在常温下不易发生反应。
⑸烧杯中石灰乳(有效成分为氢氧化钙)的作用为________。
⑹三颈烧瓶中生成MnSO4的反应化学方程式为____________。
⑺步骤I中,先通入氮气的目的是_________。为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有:及时搅拌反应液、_______(任写1条)。
(步骤II)制备MnSO4H2O晶体:利用硫酸锰的溶解度在100℃以上随温度升高而急剧降低的原理,采用压力釜升温加压结晶法后过滤、洗涤、低温干燥得纯净的MnSO4H2O晶体。
(步骤III)制备Mn3O4固体:准确称取101.4mg MnSO4H2O,将MnSO4H2O晶体在空气中高温煅烧,下图是用热重分析仪测定煅烧时温度与剩余固体质量变化曲线。
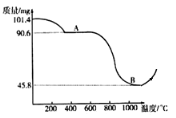
[资料2] MnSO4在空气中高温煅烧生成Mn3O4和三氧化硫,当温度超过1000℃时,Mn3O4又被氧气氧化为Mn2O3或MnO2
⑻该曲线中A段所表示物质的化学式为___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用如图所示装置制取氧气,下列实验操作不正确的是
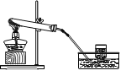
A. 加热前,先将集气瓶注满水用玻璃片盖好,再倒立在水槽中
B. 实验开始时,先将导管口伸入集气瓶,再开始加热
C. 收集O2后,先在水面下盖好玻璃片,再将集气瓶移出水槽
D. 实验结束时,先把导管移离水面,再熄灭酒精灯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com