
【题目】(6分)甲为初中化学常见物质,请根据下列叙述回答问题。
(1)若甲可以用于灭火,将甲通入紫色石蕊试液中,观察到试液变红色,发生反应的化学
方程式为__________。
(2)若甲是一种红色固体氧化物,将甲放入过量的稀盐酸中,观察到固体消失, 。
反应后所得溶液的溶质为__________。
(3)若甲含有4种元素且能与稀盐酸反应产生气泡。向甲的溶液中加入过量氢氧化钠溶液,发生反应生成乙和水,但无明显现象;向反应后的溶液中逐滴滴加稀盐酸,一段时间后产生气泡。甲与氢氧化钠溶液的反应方程式为___________。
(4)若一定量的甲与乙在一定条件下发生反应,下列情况与图像的对应关系正确的是 __________ (填序号)。
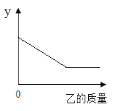
甲 | 乙 | y轴含义 | |
A | 生石灰 | 水 | 固体质量 |
B | 铜锌合金粉末 | 硫酸铜溶液 | 溶液质量 |
C | 工业炼铁的尾气 | 氢氧化钠溶液 | 气体质量 |
D | 密闭容器中的空气 | 红磷 | 反应过程中容器内压强 |
【答案】(1)CO2 + H2O = H2CO3
(2)无色溶液变为黄色 FeCl3、HCl
(3)NaHCO3 +NaOH = Na2CO3 + H2O (4)C
【解析】
试题分析:(1)若甲可以用于灭火,将甲通入紫色石蕊试液中,观察到试液变红色,说明该气体为二氧化碳,所以反应的化学方程式为:CO2 + H2O = H2CO3
(2)若甲是一种红色固体氧化物,将甲放入过量的稀盐酸中,观察到固体消失,说明为氧化铁,发生反应:Fe2O3+6HCl==2FeCl3+3H2O,现象为:无色溶液变为黄色,由于加入的盐酸是过量的,所以反应后所得溶液的溶质为:FeCl3、HCl
(3)若甲含有4种元素且能与稀盐酸反应产生气泡,说明是碳酸氢钠,向氢氧化钠溶液和碳酸氢钠反应后的溶液中逐滴滴加稀盐酸,一段时间后产生气泡,说明溶液中既有氢氧化钠,又有Na2CO3,其实就是说它们反应的产物是Na2CO3,所以甲与氢氧化钠溶液的反应方程式为:NaHCO3 +NaOH = Na2CO3 + H2O
(4)A、在生石灰中加水,发生了反应,固体质量应一直减少为0,错误,B、在铜锌合金粉末中加入硫酸铜溶液,发生反应:CuSO4+Zn==ZnSO4+Cu,根据CuSO4与ZnSO4的质量关系,可以判断溶液质量是增大的,错误,C、工业炼铁的尾气含有二氧化碳和一氧化碳,通过氢氧化钠溶液,二氧化碳被吸收,气体质量减少,正确,D、密闭容器中的空气,点燃红磷,燃烧放热,气体膨胀,所以刚开始压强应增大,错误


 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:
【题目】下列防锈措施不合理的是
A. 钢管存放在干燥的地方 B. 用盐水清洗菜刀
C. 及时清除铁制品表面的锈渍 D. 在铁管表面镀上一层不易锈蚀的金属
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于氧气制取和性质的叙述中,不正确的是( )
A. 实验室制取氧气时,应先加入药品,再检查装置的气密性
B. 在此反应前后,二氧化锰的质量和化学性质都不发生改变
C. 铁丝在纯氧中剧烈燃烧时,火星四射,生成黑色固体
D. 氧气是一种化学性质比较活泼的气体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究实验室中久置的生石灰样品变质情况,同学们进行如下图所示的实验。下列分析和结论不正确的是
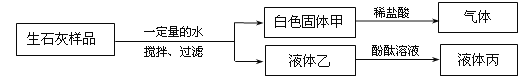
A.该样品已完全变质
B.液体丙呈红色或无色
C.该样品中一定含有碳酸钙
D.白色固体甲可能为Ca(OH)2和CaCO3的混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)实验室制取气体所需的装置如下图所示。
![]()
![]()
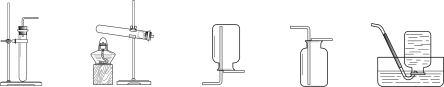
A B C D E
请回答以下问题。
(1)实验仪器a的名称是________。
(2)用过氧化氢溶液和二氧化锰制取氧气的化学方程式为________。用高锰酸钾制取氧气时,所选用的发生装置为________(填字母序号)。
(3)用大理石和稀盐酸制取二氧化碳的化学方程式为________。用装置________(填字母序号)收集一瓶二氧化碳,将燃着的木条放在瓶口,若观察到________,说明瓶中已充满二氧化碳。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验现象的描述中,正确的是
A. 硫在氧气中燃烧发出淡蓝色火焰
B. 铁丝在氧气中剧烈燃烧火星四射,生成四氧化三铁
C. 红磷在空气中燃烧产生大量白雾
D. 木炭在氧气中燃烧发出白光
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)某粗盐中主要成分为NaCl ,还含有的少量MgCl2、CaCl2和少量泥沙。为了除去杂
质,得到纯净的氯化钠,进行如下实验。
(1)除难溶性杂质。将5g的粗盐溶解于足量水中,需用玻璃棒不断搅拌,目的是 ;进行过滤操作时,需要的玻璃仪器有烧杯、玻璃棒和 ;过滤后,将滤液转移到 (填仪器名称)进行加热蒸发,得到固体精盐4g。若所得精盐的产率偏低,可能的原因是 (填字母)。
A.部分粗盐未溶解 B.蒸发时未使用玻璃棒进行搅拌,导致液滴飞溅 C. 过滤时,滤纸破损了
(2)除可溶性杂质。经过上述操作后,精盐中仍存在少量的MgCl2、CaCl2未除去,现设计如下实验进行提纯,提纯的流程如下:
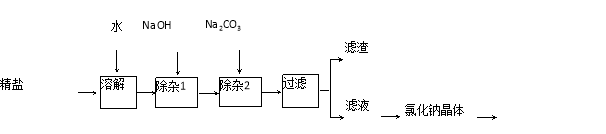
回答下列问题:
①用NaOH为了除去MgCl2杂质,反应的化学方程式为____________________ _。
②NaOH和Na2CO3如果添加过量了,需往滤液中加入适量___________除去。
③过滤后,所得滤渣中含有的物质是 (填化学式)。
④从滤液中得到氯化钠固体的主要操作是蒸发,为了获得纯净的氯化钠,应蒸发至__ _(填序号)。
A.完全蒸干时停止加热 B.快干时停止加热,利用余热蒸干
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com