
【题目】化学发展经历了从定性到定量,从宏观到微观的过程。
(1)下图是某同学验证质量守恒定律的实验装置。
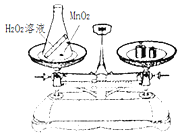
①反应的化学方程式为______________
②该实验方案设计不合理的原因是_________
③若保持装置不变,改变药品即可验证。他用的一组药品是_____________。
(2)水分解的微观过程,可用以下三幅模型图表示。
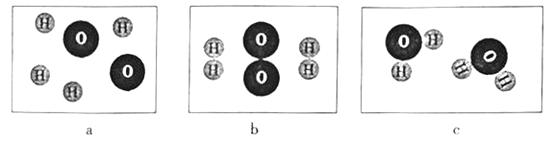
①模型图排列顺序正确的是______(填标号)。
②反应前后保持不变的是_____________(填具体微粒名称)。
【答案】 2H2O2MnO22H2O+O2↑ 反应产生的气体逸散到空气中 硫酸铜溶液和铁钉 cab 氧原子和氢原子
【解析】(1) ①根据过氧化氢溶液在二氧化锰的催化下分解生成水和氧气解答;②根据装置没有密封,反应产生的气体逸散到空气中解答;③根据反应不需要有气体参加,也不产生气体分析解答;(2) ①根据化学变化的实质分析解答;②根据微观示意图分析解答。(1) ①过氧化氢溶液在二氧化锰的催化下分解生成水和氧气,反应的化学方程式为2H2O2MnO22H2O+O2↑;②该实验方案设计不合理的原因是装置没有密封,反应产生的气体逸散到空气中;③验证质量守恒定律,反应不需要有气体参加,也不产生气体可知,故可选择金属与盐溶液进行实验。他用的一组药品是硫酸铜溶液和铁钉;(2) ①化学变化的实质是分子分成原子,原子重新组合成新的分子,故模型图排列顺序正确的是cab;②由图可知,反应前后保持不变的是氧原子和氢原子。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:初中化学 来源: 题型:
【题目】在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种。同学们为了确定该粉末的成分,进行如下探究:
【提出问题】假设l:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;假设3:红色粉末是铜粉和氧化铁粉。
【设计实验方案】同学们对实验作了如下设想和分析:取5g红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如下图)。
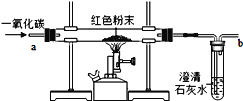
【进行实验】通过实验及分析。若确认假设3成立,则硬质玻璃管中出现的现象是____________。
【反思与评价】(1)实验过程中,硬质玻璃管内发生的化学反应方程式是_________;
(2)实验时通入一氧化碳片刻后再加热的原因是______;
(3)从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是________;
(4)若得到铁的质量为2.24g,则原来混合物中氧化铁粉末的质量分数为_____________。
【知识拓展】实验结束后得到了铜和铁,现为了进一步探究铁和铜的金属活动性强弱,还需要选择的试剂______________(填序号)。
A.碳酸钠溶液 B.稀盐酸 C.氯化锌溶液 D.硝酸铜溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验时学习化学的一条重要途径,请结合下图所示实验回答问题:

(1)实验一中在实验前细铁丝必须打磨,是为了____________________________________。
(2)实验二中活性炭的作用是______________;可以用____________检验处理后的水是否为软水。
(3)实验三证明碳单质具有的化学性质是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年5月12日是我国的第十个“防灾减灾日”,其主题是“行动起来,减轻身边的灾害风险”。下列做法不合理的是

A. 扑灭森林火灾,可将大火蔓延路线前的一片树木砍掉,形成隔离带
B. 室内电器着火,先切断电源,再用灭火器灭火
C. 把燃气热水器安装在浴室内
D. 油库、面粉加工厂、纺织厂等场所要严禁烟火
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的生存和发展离不开能源和资源。
(1)家用燃料的更新过程如下:煤→液化石油气或管道煤气→天然气。
①下列有关家用燃料更新的理由,正确的是___________。
A.天然气属于可再生能源 B.气体燃料比固体燃料利用率更高
C.天然气作为燃料可避免温室效应的发生 D.煤仅用作燃料烧掉浪费资源
②天然气的主要成分是甲烷,在空气中完全燃烧的化学方程式为__________。
(2)人类每年都要从大自然中提取大量的金属,用于满足生产和生活的需要。
①高炉炼铁过程中,焦炭的作用是提供热量和___________。
②生活中将生铁制成铁锅,是利用其__________和延展性,将铁丝放在潮湿的空气中(如图所示),一段时间后,观察到铁丝生锈,原因是铁与_____和_____(均填化学式)同时接触,同时观察到导管内液面上升;打开K,滴加稀盐酸,观察到导管内液面下降且导管口有气泡冒出,用化学方程式解释______。
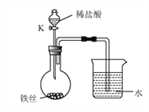
③稀盐酸可以除去铁器表面的铁锈,写出该反应的化学方程式________。实验中若需配制74g质量分数为10%的稀盐酸,需要质量分数为37%的浓盐酸(密度为1.18g/cm3)________ g,加水________mL。若用量筒量取浓盐酸时俯视读数,所配溶液中溶质的质量分数________10%(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
鸡蛋营养价值很高,一个重约50 g的鸡蛋,约含7 g蛋白质。蛋黄中富含卵磷脂,卵磷脂可以阻止胆固醇和脂肪在血管壁上沉积,被称为“血管清道夫”。一般人群每天吃1~2个鸡蛋不会造成血管硬化,但多吃会增加肝、肾负担。
鸡蛋不宜生食,也不建议吃溏心鸡蛋。因为生鸡蛋中含有抗营养因素,会影响营养素的利用,还可能被沙门氏菌污染。烹调鸡蛋达到70~80℃才能杀灭沙门氏菌,当蛋黄凝固时说明温度已接近。所以最好是蛋黄刚凝固时起锅,烹调时间过长会降低鸡蛋的营养价值。
市售鸡蛋常采用三种涂膜保鲜技术,分别是:A-聚乙烯醇溶液涂膜、B-聚乙烯醇和双乙酸钠溶液涂膜、C-聚乙烯醇和氢氧化钙溶液涂膜。三种涂膜剂涂抹于鸡蛋表面后,在温度为20℃、相对湿度为70%的贮藏柜中贮藏30天,测得哈夫单位和蛋黄指数的变化趋势如下图所示,其中CK是对照组,哈夫单位和蛋黄指数的数值越小,鸡蛋越不新鲜。
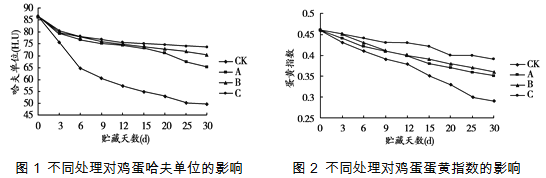
鸡蛋买回家后,在-1℃、相对湿度80%的条件下储存,最长可以保鲜6个月。
依据文章内容回答下列问题:
(1)每100 g鸡蛋,约含蛋白质______g。
(2) C-聚乙烯醇和氢氧化钙溶液涂膜保鲜鸡蛋的过程中,发生反应的化学方程式为___________。
(3)三种涂膜保鲜技术中,保鲜效果最好的是_________________。
(4)在进行涂膜保鲜效果的研究中使用了_________方法。
(5)下列说法正确的是_______。
①鸡蛋营养价值高,每天可以多吃
②鸡蛋煮的时间越长越好,有利于杀灭细菌
③生吃鸡蛋、吃溏心蛋和不吃蛋黄,是不科学的做法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质(均不含结晶水)的溶解度曲线如右图所示。下列说法正 确的是
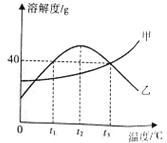
A.t1℃时,甲的溶解度大于乙的溶解度
B.t2℃时,乙的饱和溶液升温或降温均会析出晶体
C.乙溶液从t3℃降温到t1℃,乙溶液中的溶质质量分数会发生改变
D.t3℃时,50g水中加入40g的甲物质充分溶解可得到90g甲的饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图,实验室制取气体,并进行相关的实验探究,根据以下装置回答下列问题:
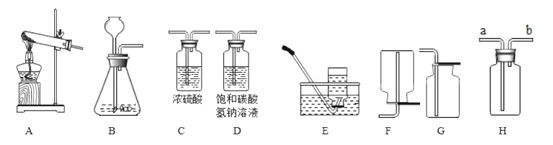
(1)若以 A 装置制取 O2: 写出反应的化学方程式为__。
(2)若以盛满水的 H 装置收集 02 :氧气应从导管__端(填字母)通入。
(3)如果用大理石和浓盐酸制取CO2:
①选用的制取装置(除 H 外均可选)____,为了得到一瓶纯净干燥的二氧化碳,装置的连 接顺序依次为:生成的气体→______→_______→收集装置。
②对于实验室制取 CO2 后剩下的废液进行探究。为检验溶液中是否有盐酸的存在,采用如 下方案进行实验,请判断方案的合理性,并写出你的理由_________。

实验证明,该废液中有盐酸存在。请你再写出一种合理的方案证明废液中含有盐酸:______。
③为了处理废液中的盐酸,得到只含有CaCl2的溶液,你可选择向废液中加入过量的___(填名称),再过滤就能达到目的。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将碳酸钠和硫酸钠的固体混合物6 g放入烧杯中,加入24.5 g稀硫酸,恰好完全反应后烧杯中只剩无色溶液28.3 g(假设CO2全部逸散)。
(1)反应生成气体的质量为________ g。
(2)计算所得溶液中溶质的质量分数为_______(结果精确到0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com