
【题目】第六组同学对上述部分反应前后物质的质量进行了称量,发现有的反应后物质质量增加、而有的质量减少。对此,该组同学展开进一步的定量探究,验证质量守恒定律。
(1)如图所示,实验前天平平衡。

① 将注射器中适量的稀盐酸注入锥形瓶中,反应的化学方程式为______,观察到天平的指针_____(填“偏左”、“偏右”或“在标尺中央”,下同)。
② 上述实验的反应结束后,松开锥形瓶上的橡皮塞,天平的指针__________。
结论:为验证质量守恒定律,若有气体参与或生成的实验必须设计__________(“开放”或“密闭”)装置进行探究。
(2)某同学根据质量守恒定律研究物质W的组成。一定条件下,W在密闭容器内发生反应,反应前后各物质的质量如下图所示:
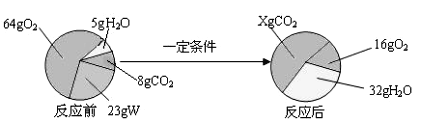
图中X =_______g。物质W由____种元素组成,其中碳、氢原子个数比为_________(填最简比)。
【答案】CaCO3+2HCl═CaCl2+CO2↑+H2O 在标尺中央 偏右 密闭 52 3 1:3
【解析】
(1)①大理石中的碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O,观察到天平的指针在标尺中央;
②上述实验的反应结束后,松开锥形瓶上的橡皮塞,反应生成的二氧化碳逸出装置,天平的指针偏右,结论:为验证质量守恒定律,若有气体参与或生成的实验必须设计密闭装置进行探究;
(2)图中X=23g+(64g-16g)-(32g-5g)+8g=52g;物质W中氧元素质量为:(52g-8g)×![]() +(32g-5g)×
+(32g-5g)×![]() -(64g-16g)=8g,因此W由碳元素、氢元素和氧元素等3种元素组成;其中碳元素、氢元素质量分别为:(52g-8g)×
-(64g-16g)=8g,因此W由碳元素、氢元素和氧元素等3种元素组成;其中碳元素、氢元素质量分别为:(52g-8g)×![]() =12g、(32g-5g)×
=12g、(32g-5g)×![]() =3g,碳、氢原子个数比为:
=3g,碳、氢原子个数比为:![]() :
:![]() =1:3。
=1:3。


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:初中化学 来源: 题型:
【题目】实验室常用的气体发生装置如图一所示。
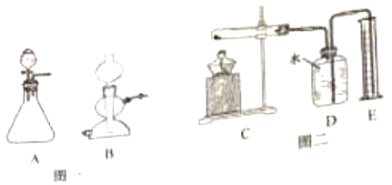
①实验室常用溶质质量分数为5%的过氧化氢溶液制取氧气,“5%”的含义是__。
②含溶质0.2mol的过氧化氢溶液完全分解,可以生成多少克氧气?___根据化学方程式列式计算),用5%的过氧化氢溶液和二氧化锰为原料制取氧气,较合理的发生装置是__(选填装置编号);
③探究溶质质量分数、催化剂质量、温度等因素对过氧化氢分解速率的影响,设计以下实验方案,其中实验甲、乙、丙的目的是__;实验戊中,w=__,t=__。
实验序号 | 过氧化氢溶液溶质质量分数 | 二氧化锰质量(g) | 温度(℃) |
甲 | 10% | 0.5 | 20 |
乙 | 10% | 1 | 20 |
丙 | 10% | 1.5 | 20 |
丁 | 5% | 1.5 | 30 |
戊 | w | 1.5 | t |
④加热氯酸钾和二氧化锰的混合物一段时间,测定生成氧气的体积,用图二所示装置进行实验(装置气密性良好)。试管中发生反应的化学方程式是__;有关该实验的说法合理的是__(选填编号)。
a.实验开始前装置D中必须装满水
b.连接C、D、E装置后点燃酒精灯
c.停止加热后,量筒内液面会下降
d.停止加热前应断开C、D装置,防止液体倒流
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为某小组探究金属化学性质的两组实验。
实验I | 实验II |
|
|
①实验I中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为该实验设计不够合理,理由是______________;
②写出实验II中C试管内反应的化学方程式_____________;
③实验II中要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是_____(填字母序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染。于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属。实验过程如下:
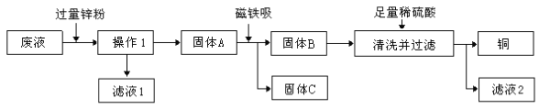
请回答:
(1)操作1是_______,固体A的成分_______。
(2)固体C是_______。滤液1和滤液2中溶质相同,该溶质是_______。
(3)写出加入过量锌粉的其中一个反应的化学方程式______;加入足量稀硫酸发生反应的化学方程式__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】第一组同学就“空气中的氧气”进行如下探究:
(1)定性角度
举例证明空气中含有氧气:___________(写一条)。
(2)定量角度
小组同学进行如图所示实验:将装有足量铁丝的量筒倒扣于水槽中,量筒内液面处于9.0 mL的刻度处;放置一周后,可观察到铁丝变________色,同时量筒内的液面上升到约_________mL刻度处,测得空气中氧气所占的体积分数。
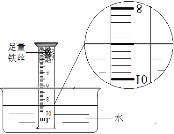
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示进行有关碳及其氧化物的性质实验(图中固定玻璃管的仪器已略去),下列说法正确的是( )
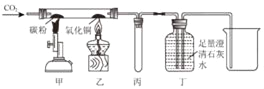
A. 丙装置的作用是收集二氧化碳
B. 该装置的不足之处是未进行尾气处理
C. 甲和乙两处现象分别是黑色粉末减少,黑色粉末逐渐变红
D. 丁装置的作用只是检验乙处发生的反应有二氧化碳生成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类文明与社会进步同金属材料密切相关。
(1)2018年12月29日,南京长江大桥恢复通车。为保证大桥的使用寿命,下列防锈措 施可行的是___。
A.用抗腐蚀性能优异的合金制造造桥零部件B.刷防锈漆
C.桥身表面镀一层黄金D.给某些部位涂油
(2)造桥需要钢铁,工业炼铁的原料有铁矿石、石灰石、___和热空气;钢铁材料分为生铁和钢,这两种铁合金的主要区别就在于___。
(3)将光亮镁条放入一定量的氯化铵溶液中,发现最终生成灰白色固体[Mgx(OH)yClz]外, 还有气体生成。某同学对该现象作如下探究。
(一)生成气体可能是 H2、HCl、NH3 中的一种或几种。
(查阅资料)
①浓硫酸既可以吸收水,也可吸收氨气;
②常温下,氨气和氯化氢气体反应生成白色固体氯化铵(NH4Cl);
③2NH3+3CuO![]() 3Cu+N2+3H2O;
3Cu+N2+3H2O;
④H2+CuO![]() Cu+H2O。
Cu+H2O。
(实验探究)收集气体,将气体通过如图装置(各步反应均完全);
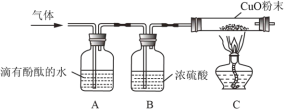
①A装置中出现红色,证明有___;
②A、B 实验装置___(填“能”或“不能”)对调,理由是___;
③C 中玻璃管内观察到___,证明有H2。
(反思与评价)他认为不需要单独检验HCl,就能证明HCl不存在,请你评价这种说法是 否合理并说明理由___。
(二)过滤、洗涤、一定温度下烘干得灰白色固体。
(查阅资料)灰白色固体Mgx(OH)yClz 受热会分解,只生成MgO和HCl。
(实验探究)
取一定量灰白色固体样品,充分加热,得到4g白色固体和3.65g气体。
(结论)
①x : z=___;
②若所得灰白色固体的相对分子质量为153,则所得灰白色固体的化学式是___。
(反思与评价)
由同学认为,不属于任何数据,就可以求出x:z的值,请你说出理由___
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E是初中化学常见的物质,A为一种单质,B为产生温室效应的一种气体,C与B的组成元素相同,D为一种常见的建筑材料。它们之间的转化关系如图所示,其中“![]() ”表示物质间的转化。请回答下列问题:
”表示物质间的转化。请回答下列问题:
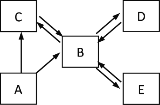
(1)B、D的化学式:B_____ D_____;
(2)写出下列转化的化学方程式:
C![]() B:_____ E
B:_____ E![]() B:_____。
B:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组对CO2展开研究:

Ⅰ.CO2的制备
(1)写出图中标号仪器的名称:①______。
(2)实验室制取CO2的反应原理是为______(写化学方程式)。检查A装置的气密性的一种方法是向分液漏斗中加适量水,堵住右侧导气管,打开分液漏斗活塞,若观察到______,则装置不漏气。
(3)实验发现:制取CO2时,最好选用质量分数为7.5%的稀盐酸。现欲配制100g 7.5%的稀盐酸,需要37%(密度为1.18g / mL)的浓盐酸______mL(计算结果精确到小数点后一位),需要水______mL(精确度同上)。量取水时,若仰视读数(其他操作均正确),则所配稀盐酸的质量分数______7.5%(填“>”或“=”或“<”),配制过程不需要的仪器是______。
A.酒精灯 B.量筒 C.烧杯 D.玻璃棒 E.胶头滴管 F.药匙
Ⅱ.CO2的收集
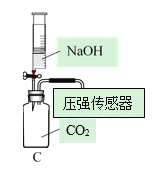
用以下三种方法收集,每种方法均做三次实验,取平均值。将C装置注射器中足量NaOH溶液注入集气瓶中,充分振荡,测集气瓶内气压。(饱和碳酸氢钠溶液可吸收CO2中的HCl气体,NaOH溶液可用来吸收CO2)
方法1:当B装置开始产气泡15s后,用排水法收集 CO2气体,记录集满CO2气体所要的时间为t;
方法2 :当B装置开始产气泡15s后,用向上排空气法收集,收集时间用方法一所用的平均时间t0;
方法3:当B装置开始产气泡15s后,用向上排空气法收集,同时用燃着木条放在集气瓶口,待木条熄灭,立即盖上玻璃片。
实验数据:
方法1 | 方法2 | 方法3 | |
瓶内初始气压(kPa) | 104.2 | 104.2 | 104.2 |
三次实验最终气压平均值(kPa) | 9.3 | 31.8 | 39.7 |
CO2纯度 | 91.1% | 69.5% | X |
数据
(4)三种方法均在15s后开始收集的原因是______。
(5)已知:CO2纯度 =![]() ,则方法3所收集CO2的纯度为______。通过对比,欲收集更高纯度的CO2,应采用______法收集。
,则方法3所收集CO2的纯度为______。通过对比,欲收集更高纯度的CO2,应采用______法收集。
Ⅲ.二氧化碳转化新进展
(6)利用非高热电浆体合成技术可将CO2和甲烷(CH4)反应合成乙酸(CH3COOH),反应的化学方程式为______。
(7)在光催化条件下,CO2和H2反应生成甲烷(CH4)和水,反应的化学方程式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com