
【题目】现欲探究一固体混合物 A的成分,已知其中可能含有NH4NO3、NaCl、BaCO3、Cu(NO3)2四种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理(设过程中所有发生的反应都恰好完全反应)
I.取一定质量的该固体混合物A放入一洁净烧杯中,向其中加入足量水,搅拌,待烧杯中物质充分混合后,过滤,得白色沉淀B和蓝色滤液C.
II向步骤I所得滤液C中滴加适量氢氧化钠溶液,出现的现象如图中所述:

试根据实验过程和发生的现象判断:
(1)白色沉淀B是____________(写化学式)。
(2)固体混合物A中一定存在的物质是____________(写化学式)。
(3)写出实验过程①中生成蓝色沉淀F的化学方程式______________________。
(4)滤液D中一定大量存在的酸根离子为__________(写离子符号)。
(5)若要检验混合物A中不能确定的物质是否存在,可以用无色滤液D进一步实验,请简述实验操作步骤,发生的现象及结论:________________。
【答案】BaCO3 BaCO3、Cu(NO3)2、NH4NO3 Cu(NO3)2+2NaOH = Cu(OH)2↓+2NaNO3 NO3- 取溶液D少许,向其中加入硝酸银和稀硝酸溶液,若出现白色沉淀,证明有氯化钠,否则没有。(只加入硝酸银溶液也可以得满分)
【解析】
固体混合物A加水溶解、过滤后得白色沉淀B和蓝色滤液C,则B为BaCO3,滤液C中一定有Cu(NO3)2;蓝色滤液C加氢氧化钠后得到蓝色沉淀F和气体E,则F为Cu(OH)2,E为NH3,则说明原白色固体A中一定有NH4NO3,题干中的现象不能确定原白色固体中是否有NaCl.
由分析知白色沉淀B是BaCO3;
由分析知,固体混合物A中一定存在BaCO3、Cu(NO3)2、NH4NO3;
蓝色沉淀F是Cu(NO3)2和NaOH反应生成得,化学方程式为:Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3;
混合物A中不能确定的物质是NaCl,NaCl和AgNO3反应会产生白色沉淀,故通过AgNO3来检验:取溶液D少许,向其中加入硝酸银和稀硝酸溶液,若出现白色沉淀,证明有氯化钠,否则没有。


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:初中化学 来源: 题型:
【题目】如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
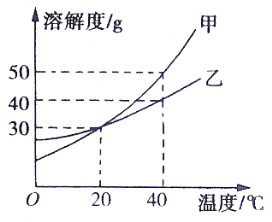
A.20℃时,甲、乙两种固体物质的溶解度都是30
B.40℃时,甲的饱和溶液中溶质质量分数为50%
C.40℃时,将50g乙物质全部溶于水中,恰好能得到150g乙的饱和溶液
D.将130g 20℃甲的饱和溶液升温到40℃,最多还能溶解甲物质20g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是学习化学的重要工具,根据下图回答问题


图一 图二
(1)溴的相对原子质量是 ______________;
(2)溴元素的化学性质与图二___________(填字母)元素的化学性质相似;
(3)溴元素与图二中A元素形成化合物的化学式为 __________________ ;
(4)若图二中C表示离子,则X的数值为 _______________ ;
(5)已经氢溴酸(化学式为:HBr)的化学性质与盐酸类似,请写出铁与氢溴酸反应的化学方程式:___________________________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学完酸碱盐的知识后,某兴趣小组开展了如下的探究,请回答相关问题。
(1)向石灰乳中加入一定量的稀盐酸,得到了澄清溶液,写出发生反应的化学方程式:__________________________。已知氯化钙溶液显中性,现用pH计测得反应后的溶液的pH=4.3,则此时溶液里的粒子示意图正确的是_______(填字母序号)。
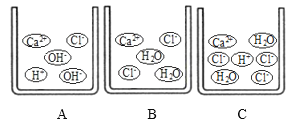
(2)已知常温下氢氧化钙的溶解度为 0.17g。若将石灰乳静置一段时间,则得到的上层澄清液体的溶质质量分数为_____(精确到 0.01%)。
(3)向石灰石中加入稀硫酸,发现反应缓慢,如何提高该反应速率呢?
查阅资料:石灰石与稀硫酸反应生成 CaSO4,同时产生CO2气体;且CaSO4 微溶于水。
Ⅰ.甲同学认为可以用增大稀硫酸浓度的方法来提高该反应速率。取相同质量相同规格的石灰石进行了如下实验:
实验 | ①10%硫酸溶液 | ②20%硫酸溶液 | ③40%硫酸溶液 |
观察1分钟内石灰石表面的气泡放出快慢 | 缓慢 | 明显加快 | 开始很快、又迅速变慢 |
由上述实验现象可知,增大稀硫酸的浓度_____(填“一定”或“不一定”)能提高该反应速率。请推测出现实验③中现象的原因:______________________________
Ⅱ.写出另外一种提高该反应速率方法:_____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示某个化学反应,据图分析判断,下列各项中,不正确的是( )
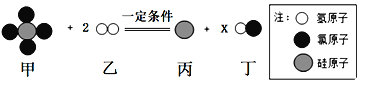
A. 该反应属于置换反应.
B. 反应中乙、丙两物质质量比为2: 7
C. 图示中x的数值为4
D. 反应前后氢元素的化合价发生了改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定某铜锌合金中锌的质量分数,某同学利用该合金与稀硫酸反应,进行了三次实验,所得相关得实验数据记录如下(实验中的误差忽略不计)
第一次 | 第二次 | 第三次 | |
所取合金的质量/g | 25 | 25 | 50 |
所用稀硫酸的质量/g | 120 | 160 | 100 |
生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
(1)从上表数据分析,当所取合金与所用稀硫酸的质量比为_____时,表明合金中的锌与稀硫酸中的硫酸完全反应.
(2)试计算该铜锌合金中锌的质量分数_____.
(3)所用稀硫酸溶液的溶质的质量分数_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下各图像描述的实验现象与对应的实验操作不相符合的是
A.  向稀盐酸和CaCl2的混合溶液中加入纯碱溶液
向稀盐酸和CaCl2的混合溶液中加入纯碱溶液
B.  室温时,向一定量的稀盐酸中加入少量镁条
室温时,向一定量的稀盐酸中加入少量镁条
C.  向一定量碳酸钠和氢氧化钠的混合溶液中逐滴加入稀盐酸,生成气体的质量
向一定量碳酸钠和氢氧化钠的混合溶液中逐滴加入稀盐酸,生成气体的质量
D.  将20℃时的硝酸钾的饱和溶液升温至60℃,溶液中溶质质量分数的变化
将20℃时的硝酸钾的饱和溶液升温至60℃,溶液中溶质质量分数的变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用红磷燃烧测定空气中氧气含量的实验中,用传感器记录集气瓶中压强、温度随时间变化的情况。a 是打开止水夹的时刻,有关说法错误的是( )


A. 反应开始时压强增大是因为温度升高
B. a 点的温度已经接近室温
C. a 点处的压强等于大气压
D. a 点后气压增大是由于水倒吸入集气瓶
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从Na、C、S、H、O、N六种元素中选择适当的元素按要求填空
(1)用适当的数字和符号填空。
①三个钠离子____ ;②一个碳酸根离子_____;③双氧水中氧元素的化合价为-1价____。
(2)写出符合下列要求的物质的化学式;能灭火的气体是___,如食品包装袋中充可防腐的单质是____,溶于水使溶液温度升高的碱是________,能形成硫酸型酸雨的空气污染物是_______;溶于水使溶液温度显著降低的物质是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com