
| 盐酸的化学性质 | 酸的通性(原因: 电离时产生的阳离子全部是氢离子) | |
| 化学性质 | 化学方程式或结论 | |
| 与酸碱指示剂作用 | 能使紫色石蕊试液变红色 | 能与酸碱指示剂作用 |
| 与镁反应 | Mg+2HCl═MgCl2+H2↑ | 与活泼金属反应,生成盐和氢气 |
| 与氧化铁反应 | Fe2O3+6HCl═2FeCl3+3H2O | 与金属氧化物反应,生成盐和水 |
| 与碳酸钠反应 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | 与碳酸盐反应,生成盐、水和二氧化碳 |
分析 根据酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、碳酸盐等反应),据此进行分析解答.
解答 解:酸是电离时产生的阳离子全部是氢离子的化合物,酸具有通性的原因是其电离时产生的阳离子全部是氢离子.
盐酸能与酸碱指示剂作用,能使紫色石蕊试液变红色,说明酸能与酸碱指示剂作用.
盐酸与镁反应生成氯化镁和氢气,反应的化学方程式为:Mg+2HCl═MgCl2+H2↑;可以总结出酸能与活泼金属反应生成盐和氢气.
盐酸与氧化铁反应氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;可以总结出酸能与金属氧化物反应生成盐和水.
盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式是:Na2CO3+2HCl═2NaCl+H2O+CO2↑;可以总结出酸能与碳酸盐反应生成盐、水和二氧化碳.
故答案为:
| 盐酸的化学性质 | 酸的通性(原因: 电离时产生的阳离子全部是氢离子) | |
| 化学性质 | 化学方程式或结论 | |
| 与酸碱指示剂作用 | 能使紫色石蕊试液变 红色 | 能与酸碱指示剂作用 |
| 与镁反应 | Mg+2HCl═MgCl2+H2↑ | 与 活泼金属反应,生成 盐和氢气 |
| 与氧化铁反应 | Fe2O3+6HCl═2FeCl3+3H2O | 与 金属氧化物反应,生成 盐和水 |
| 与碳酸钠反应 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | 与 碳酸盐反应,生成 盐、水和二氧化碳 |
点评 本题难度不大,掌握酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、碳酸盐等反应)并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
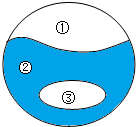 如图所示为物质的分类关系,①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )
如图所示为物质的分类关系,①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 A、B、C、D、E为初中化学常见的几种物质,它们之间有如图所示的转化关系,图中“”表示物质两两之间可以发生反应,“→”表示某一物质可以转化为另一物质,“?”表示两种物质可以互相转化为另一物质.请回答:
A、B、C、D、E为初中化学常见的几种物质,它们之间有如图所示的转化关系,图中“”表示物质两两之间可以发生反应,“→”表示某一物质可以转化为另一物质,“?”表示两种物质可以互相转化为另一物质.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯化钠 食盐 NaCl2 | B. | 碳酸氢钠 纯碱 NaHCO3 | ||
| C. | 氢氧化钙 熟石灰 CaO | D. | 氢氧化钠 烧碱 NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com