
【题目】我们的祖先很早就掌握了用孔雀石[主要成分是Cu2(OH)2CO3]和木炭一起加热进行火法炼铜的工艺,早在3000多年前的商朝就造出“后母戊鼎”等许多精美的青铜器.
有关的化学方程式:①Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑;②C+2CuO
2CuO+H2O+CO2↑;②C+2CuO![]() 2Cu+CO2↑.
2Cu+CO2↑.
在西汉时期就开始湿法炼铜的应用,当时刘安所著的《淮南万毕术》中,就有曾青(硫酸铜溶液)得铁则化为铜的记载,请回答下列问题:
(1)上述反应①属于________反应(选填“分解”、“化合”或“置换”).
(2)青铜属于________(填“氧化物”、“单质”、“化合物”或“混合物”).
(3)写出湿法炼铜发生反应的化学方程式:________.
(4)以“绿色化学”的观点,对照火法炼铜,谈谈湿法炼铜的优点:________.
【答案】分解 混合物 Fe+CuSO4=FeSO4+Cu 节约能源,不污染环境
【解析】
(1)由反应①Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑可知,该反应是一种物质反应生成多种物质,则属于分解反应;
2CuO+H2O+CO2↑可知,该反应是一种物质反应生成多种物质,则属于分解反应;
(2)因青铜是红铜和锡、铅的合金,也是金属治铸史上最早的合金,属于混合物;
(3)铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式Fe+CuSO4=FeSO4+Cu;
(4)相比火法炼铜,湿法炼铜不需要加热,则反应条件简单,且火法炼铜得到的铜易被氧化,即湿法炼铜的优点是反应条件简单,得到的铜不易被氧化,不污染环境.
故答案为:(1)分解;(2)混合物;(3)Fe+CuSO4=FeSO4+Cu;(4)节约能源,不污染环境.


科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线。

(1)甲的溶解度随着温度的升高而_____。
(2)使接近饱和的甲溶液变为饱和溶液的一种方法是_____。
(3)t℃时,甲的饱和溶液中溶质与溶液的质量比为_____。
(4)乙中含有少量甲,提纯乙可采用的方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定空气里氧气的含量,甲、乙、丙三个同学用如图1所示的装置分别进行了实验探究(已知碳与氧气反应生成二氧化碳,二氧化碳气体可与氢氧化钠溶液反应且不生成气体)
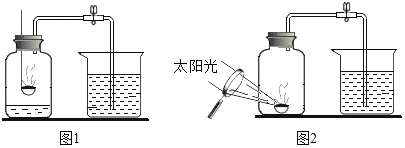
(1)甲同学:点燃红磷立即伸入瓶中并塞上瓶塞。待红磷燃烧停止并冷却后,打开弹簧夹,观察到集气瓶中吸入水的体积约占集气瓶容积的_____
(2)乙同学:用碳替代红磷,完成上述实验,发现集气瓶内并没有吸入水。后来在老师的指导下,他先向集气瓶中加入适量的_____溶液,完成实验,得到了与甲同学相同的实验结果。
(3)某同学对实验进行反思后,提出了改进方法(如图2),你认为改进后的优点是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】.某学校兴趣小组的同学,取学校附近某河的水样,利用如图所示的实验过程对该水样进行了净化处理。请回答下列问题:
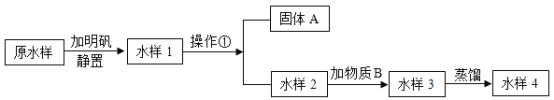
(1)明矾的作用是______________________,操作①的名称是__________,该操作需要用到的玻璃仪器有_________________。如果经过操作①后,所得水样依然浑浊,可能的原因有(答2点)_________________、___________________。
(2)为除去水样2中的一些异味和色素,加入的物质B是__________,利用的是该物质的________性质(填“物理”或“化学”)。
(3)取少量水样3是不是纯水?对此你有无不同的看法_______________。生活中将硬水转化为软水的方法是_____________。
(4)根据净化过程,判断水样1、水样2、水样3和水样4中净化程度最高的______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用甲和乙反应制备燃料丙.根据下列微观示意图得出的结论中,正确的是( )
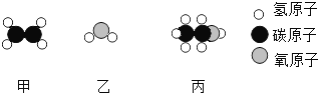
A. 甲的化学式为CH4B. 反应中甲、乙的分子个数比为1:2
C. 甲、乙、丙都是氧化物D. 该反应中分子的种类发生了改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请用提供的药品完成氧气、二氧化碳的制取,结合下列实验装置图回答问题。
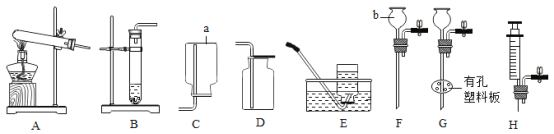
①写出仪器名称:a________、b________;
②氯酸钾制取氧气的发生装置是________;化学方程式是________;有以下主要操作步骤:
a 加热 b 把药品装入试管后固定在铁架台上 c 检查装置的气密性d 熄灭酒精灯 e 用排水集气法收集 f 从水槽中取出导管,符合题意的操作顺序是(写序号)________;
③用装置B制取二氧化碳,无法对反应进行控制,请从图中选取装置________(填序号)取代B中的单孔塞,以控制该反应,使反应随时发生随时停止。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学的发展使人类对空气的认识不断更新。
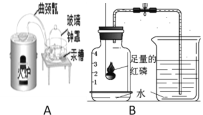
(1)A是拉瓦锡用定量的方法研究空气组成的实验。仿照拉瓦锡实验的原理,我们用装置B测量空气中氧气的含量。A中一部分银白色的液态汞加热后变成红色粉末,反应的表达式是____________。
(2)装置B待红磷熄灭并冷却到室温,打开弹簧夹,观察到烧杯中的液面下降,烧杯和导管中的水进入集气瓶中,____。因为红磷燃烧消耗____,使集气瓶内_____,小于外界大气压,在压强差的作用下,产生上述现象。进入集气瓶中水的体积即为瓶中____。据上述现象,可得出的结论是_____。实验前在玻璃导管中充满水的目的是_____
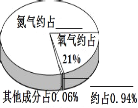
(3)英国科学家瑞利和拉姆塞发现从空气中取得的氮的密度为1.2572kg/m3;而从氨中取得的氮的密度为1.2505kg/m3。根据这个细微的差异,他们发现了密度比氮大的气体氩,对空气的组成做出更准确的判定。两位科学家因此分获诺贝尔奖。目前,人们已用实验方法精确地测定空气的成分,请将空气的成分或体积分数填写在统计图的横线上。____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定 条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如下表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量(g) | 20 | m | 8 | 6 |
反应后质量(g) | 4 | 待测 | 28 | 2 |
关于此反应,下列描述正确的是( )
A. 乙是该反应的催化剂
B. “待测”数值一定为2
C. 反应中甲与丙的质量比为1:7
D. 该反应可能是铜和氧气反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学从定量角度研究双氧水制取氧气的过程,对原实验进行部分改进,增加了称量操作.具体做法是:取10%的双氧水和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下: 若反应后,双氧水分解完全且氧气全部逸出,该同学得出的结论中,不合理的是()
反应过程 | 反应前 | 反应后 |
质量变化(不含容器质量) | 34.3g | 32.7g |
A. 反应速率逐渐加快 B. 最多得到氧气的质量为1.6g
C. 催化剂二氧化锰的质量为0.3gD. 反应得到水和氧气的质量比为9:8
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com