
 如图是超市销售的一种加碘盐标签上的部分文字说明,加碘盐通常在食盐中加碘酸钾(KIO3).关于该碘盐,下列说法正确的是( )
如图是超市销售的一种加碘盐标签上的部分文字说明,加碘盐通常在食盐中加碘酸钾(KIO3).关于该碘盐,下列说法正确的是( )| A. | 碘酸钾的相对分子质量为546 | |
| B. | 每袋该食盐中含碘元素的质量为20mg | |
| C. | 碘酸钾中钾、碘、氧三种元素的质量比为39:127:24 | |
| D. | 该加碘盐属于混合物,其中的碘酸钾属于纯净物 |
分析 A.根据相对分子质量的计算方法来分析;
B.根据标签信息来分析;
C.根据化合物中元素质量比的计算方法来分析;
D.根据混合物与纯净物的概念来分析.
解答 解:A.碘酸钾( KIO3 )的相对分子质量是39+127+16×3=214,故错误;
B.每袋该食盐中含碘元素的质量为0.5kg×20mg/kg=10mg,故错误;
C.碘酸钾中钾、碘、氧三种元素质量比为39:127:(16×3)=39:127:48,故错误;
D.该加碘盐是由氯化钠和碘酸钾组成的物质,属于混合物,其中的碘酸钾属于纯净物,故正确.
故选D.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.


科目:初中化学 来源: 题型:解答题
| 实验方案 | 实验步骤 | 预期现象 | 结论 |
| 方案1 | 取样,滴入适量的硝酸钡溶液 | 出现白色沉淀 | 有硫酸 |
| 方案2 | 取样,滴入盛有锌粒的试管中 | 有气泡产生 | 有硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 操作一:取小苏打样品少量溶于足量水后,加入过量的②(填药品编号,下同),观察,如有沉淀,则继续进行下一步操作. 操作二:待操作一中反应充分后过滤,并在滤液中加入过量的④观察. | 操作一中无沉淀出现[] | 假设一成立 |
| 操作一中有沉淀出现 | 假设二成立 | |
| 操作二中产生气泡 | 假设三成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
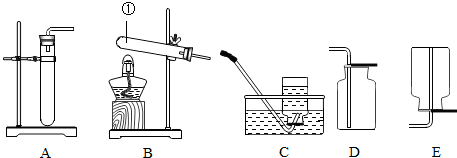
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
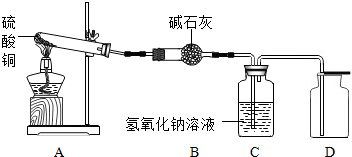
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0克 | 75.0克 | 140.0克 |
| 反应后 | 37.0克 | 79.5克 | 140.0克 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 16% | B. | 10% | C. | 9.2% | D. | 6.5% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 氟原子核内质子数为9 | B. | 氟元素为非金属元素 | ||
| C. | 氟元素的相对原子质量为19g | D. | 氟元素符号为F |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com