
【题目】I.把一定质量的锌粉投入到硫酸亚铁和硫酸铜的混合溶液A中,充分搅拌,过滤。回答下列问题。
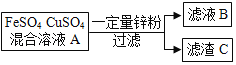
(1)若向滤渣C中加入适量稀硫酸,有气体生成。滤渣C中一定有__,滤液B中除水外,一定有__。
(2)若向溶液A中加入过量的锌粉,写出向滤渣C中加入足量硫酸,发生的反应的化学方程式为__________、_______。
II.为了验证金属活动性强弱和验证质量守恒定律,同学们设计了如图所示的实验。

(1)利用实验一和实验二,既能验证铜、锌金属活动性强弱,同时能验证质量守恒定律,则溶液A可以是__(填序号)。
a.稀硫酸 b.硝酸银溶液 c.氯化亚铁溶液 d.硫酸锌溶液 e.硫酸铜溶液
(2)利用以上试剂设计反应,验证铜和银的金属活动性,化学反应方程式为____,现象为_____。
【答案】Cu、Fe ZnSO4 H2SO4+Fe=FeSO4+H2↑ H2SO4+Zn=ZnSO4+H2↑ c或e Cu+2AgNO3=Cu(NO3)2+2Ag 铜片表面有银白色固体析出,溶液由无色变为蓝色;
【解析】
金属活动性顺序锌>铁>铜,向含有FeSO4、CuSO4混合溶液中加入一定质量锌粉,锌粉会首先置换硫酸铜中的铜,待硫酸铜完全反应后继续与硫酸亚铁发生反应;过滤向滤渣中滴加稀硫酸,有气泡产生,说明滤渣金属中一定含有铁,即锌已经和硫酸亚铁发生反应;既能验证金属活动性又能验证质量守恒定律,所选试剂不能与加入的反应物反应产生气体,同时能比较出金属活动性强弱。
I(1)因为向滤渣中滴加稀硫酸,有气泡产生,说明滤渣中一定有铁粉,即锌已经和硫酸亚铁发生反应,那说明原混合溶液中的铜全部被置换出来,则滤出的固体中一定含有Cu、Fe,至于是否含有Zn,要根据加入锌的量是否过量来决定;
因原混合溶液中的铜全部被置换出来,即滤液中肯定没有CuSO4,至于是否含有FeSO4,要根据加入锌的量是否过量来决定,但是,由于锌和CuSO4、FeSO4反应时生成的都是ZnSO4,所以滤液肯定中有ZnSO4。
(2) 若向溶液A中加入过量的锌粉,滤渣C中一定由Cu、Zn、Fe,加稀硫酸能发生反应的是锌和铁,化学方程式分别为:H2SO4+Fe=FeSO4+H2↑、H2SO4+Zn=ZnSO4+H2↑
II(1)a、稀硫酸能证明铜、锌金属活动性强弱,但不能验证质量守恒定律,故不符合题意;
b、硝酸银溶液与铜、锌都反应,无法证明铜、锌金属活动性,故不符合题意;
c、氯化亚铁溶液与锌反应,与铜不反应,能证明铜、锌金属活动性,而且,反应前后天平平衡能证明质量守恒定律,故符合题意;
d、硫酸锌溶液与铜、锌都不反应,无法证明铜、锌金属活动性,故不符合题意;
e、硫酸铜溶液与锌反应置换出锌,证明锌的金属活动性比铜强,而且,反应前后天平平衡证明质量守恒定律,故符合题意;
(2) 将铜片放入硝酸银溶液中,银被置换出来,可以证明铜的金属活动性比银强,化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag;
铜和硝酸银反应的现象是:铜片表面有银白色固体析出,溶液由无色变为蓝色。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:初中化学 来源: 题型:
【题目】元素周期律和元素周期表是学习化学的重要工具,下表是元素周期表的部分信息。
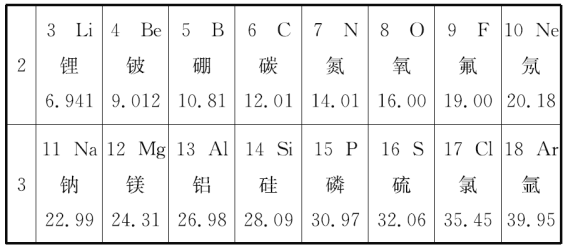
请认真分析表中信息,回答下列问题:
(1)空气中含量最多的元素名称是______,人体中含量最多的元素名称是______。
(2)![]() 所表示的粒子在反应中容易________(填“得到”或“失去”)电子。
所表示的粒子在反应中容易________(填“得到”或“失去”)电子。
(3)由原子序数为8和13的两种元素组成的化合物是___________(写化学式)。
(4)元素周期表同一横行元素的排列规律是从左至右_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列化学方程式:
(1) 铁在氧气中燃烧:________________________________;
(2) 用碳高温还原氧化铜生成铜和二氧化碳:__________________ ;
(3)实验室用双氧水、、氯酸钾制取氧气的原理:_______________、________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用加热氯酸钾和二氧化锰混合物的方法制取氧气时,反应过程中二氧化锰在混合物中的质量分数(n%)随时间(t)变化规律如下图所示,其中正确的是
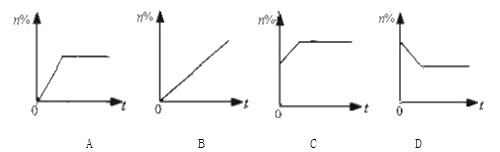
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“石头纸”就是用磨成粉末的石头为主要原料做成的。这种纸防水坚固不易燃烧,最重要的是不用砍树造纸,非常环保。日程表、便签纸等东西都是以碳酸钙为主要原料的低碳“石头纸”。为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表(假设纸张其他成分既不溶于水,也不与水和盐酸反应):
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
充分反应后生成气体的质量/g | 0.88 | 1.76 | X | 3.52 | 3.52 |
(1)表中X的值为________;
(2)在烧杯_______中碳酸钙完全反应;
(3)求样品中碳酸钙的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列反应的化学方程式。
(1)电解水____; (2)用石灰水检验二氧化碳____;
(3)铁和稀盐酸反应____; (4)铝和氧气反应____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列用化学符号表示
(1)2个氧原子________;
(2)3个硫酸根离子________;
(3)氢分子_______________;
(4)硫酸铝中铝元素显+3价______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合图所示实验装置回答有关问题:
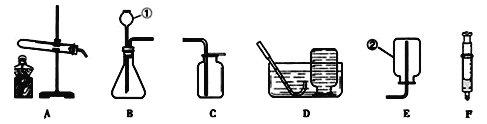
(1)写出装置图中标号仪器名称:①_____________;②______________。
(2)小强用高锰酸钾制取较纯净的氧气,他应选择的发生装置是______,收集装置是______,反应的化学方程式是________。证明氧气已收集满的方法是______。停止该实验的正确操作步骤是先_______________再_______,否则会导致______。
(3)检查装置B气密性的方法是:用注射器F检查装置B的气密性,步骤如下:
①向锥形瓶中加水至_______以形成液封;
②将注射器F连接到装置B的导管口处;
③缓慢往外拉动注射器F的活塞,观察到________,表示装置B的气密性良好。若实验室用该装置制取CO2气体,选择的固体药品是____________(填写物质名称)。
该装置的不足之处是:不能控制反应随时发生、随时停止。可对装置B加以改进,请写出一种改进方案:
友情提示:你可从图所示的用品中选取,也可自行选用其它仪器。
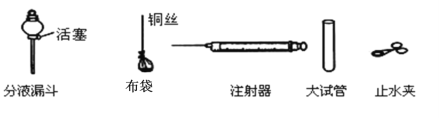
方案:_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等; 猜想2:相等。
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲 组 | 乙 组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生, 天平指针向右偏转 | 铁钉表面有红色物质析出, 溶液颜色发生改变, 天平指针没有偏转 |
结论 | 猜想1正确 反应的化学方程式:____ | 猜想2正确 |
(反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在_____中进行。
(优化装置)同学们对甲组左盘中的反应装置进行了如下两种改进,你认为最佳装置是_______(填序号)。
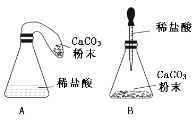
(得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想二正确。最终得出结论是:_____的各物质的质量总和等于反应后生成的各物质的质量总和。
(解释应用)解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com