
| 金属 | 空气 | 稀硫酸 | 硝酸银溶液 |
| 锌 | × | √ | √ |
| 铜 | × | × | √(A) |
| 镁 | √ | √ | √ |


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 某同学用如图所示的装置成功的探究了空气中氧气的含量(装置气密性良好,红磷足量,A、B中装有足量的水,且连接A、B的导管中事先也装满水).对于该实验有以下说法:
某同学用如图所示的装置成功的探究了空气中氧气的含量(装置气密性良好,红磷足量,A、B中装有足量的水,且连接A、B的导管中事先也装满水).对于该实验有以下说法:| A、1个 | B、2个 | C、3个 | D、4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:
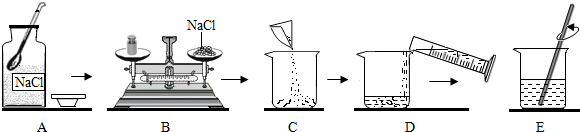
查看答案和解析>>
科目:初中化学 来源: 题型:
| 产 物 猜 想 | 甲 | 乙 | 丙 | 丁 |
| CO2、H2O | CO、H2O | NH3、CO2、H2O | CO2、CO、H2O |

查看答案和解析>>
科目:初中化学 来源: 题型:
 实验室制取O2或CO2气体的发生装置如图1,请回答下列问题:
实验室制取O2或CO2气体的发生装置如图1,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
 根据如图回答
根据如图回答查看答案和解析>>
科目:初中化学 来源: 题型:
| A、生活中的物质 | B、安全常识 | C、元素与人体健康 | D、日常生活经验 |
| 天然气的主要成分--甲烷 饮水机滤芯的吸附剂主要成分--活性炭 | 进入陌生溶洞前--先做灯火实验 炒菜时油锅着火--立即加水灭火 | 缺铁--易引起贫血 缺碘--易患甲状腺肿大 | 区别老陈醋与酱油--闻气味 区分羊毛纤维与合成纤维-灼烧后闻气味 |
| A、生活中的物质 |
| B、安全常识 |
| C、元素与人体健康 |
| D、日常生活经验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com