
| A. | K2CO3、HCl、CaCl2、KNO3 | B. | (NH4)2SO4、NaNO3、NaOH、KCl | ||
| C. | NaCl、Na2SO4、H2SO4、Ba(NO3)2 | D. | CuSO4、NaOH、NaNO3、NaCl |
分析 不用其他试剂,就能将组内物质鉴别出来,首先需考虑物质的颜色,然后将鉴别出来的物质与其他物质混合,根据现象的不同加以鉴别,若物质都是没有颜色,则让溶液之间两两混合,根据不同的实验现象加以鉴别.
解答 解:A、
| K2CO3 | HCl | CaCl2 | KNO3 | |
| K2CO3 | 无现象 | 气体 | 沉淀 | 无现象 |
| HCl | 气体 | 无现象 | 无现象 | 无现象 |
| CaCl2 | 沉淀 | 无现象 | 无现象 | 无现象 |
| KNO3 | 无现象 | 无现象 | 无现象 | 无现象 |
| (NH4)2SO4 | NaNO3 | NaOH | KCl | |
| (NH4)2SO4 | 无现象 | 无现象 | 气体 | 无现象 |
| NaNO3 | 无现象 | 无现象 | 无现象 | 无现象 |
| NaOH | 气体 | 无现象 | 无现象 | 无现象 |
| KCl | 无现象 | 无现象 | 无现象 | 无现象 |
点评 本题考查了常见物质的鉴别,不用其他试剂,应该采用供检物质两两混合的方式,根据物质的溶液颜色以及物质间反应实验现象进行,要求同学们掌握基础知识,以便灵活应用.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:初中化学 来源: 题型:解答题
 小明见妈妈买了些取暖袋,他很好奇,打开了一袋,发现里面是黑色的粉末.那么,取暖袋里是什么物质在发生反应、释放热量呢?
小明见妈妈买了些取暖袋,他很好奇,打开了一袋,发现里面是黑色的粉末.那么,取暖袋里是什么物质在发生反应、释放热量呢?| NaCl溶液 | Na2SO4溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 无明显变化 | 无明显变化 | 现象Ⅰ |
| 加入BaCl2溶液 | 无明显变化 | 产生白色沉淀 | 产生白色沉淀 |
| 加入AgNO3溶液 | 产生白色沉淀 | 溶液略呈浑浊 | 产生淡黄色沉淀 |
| 序号 | 加入试剂及操作 | 没有使用的暖袋 | 失效后的暖袋 |
| I | 加入足量水观察 | 无色溶液,大量固体在烧杯底部 | 无色溶液,大量固体在烧杯底部 |
| Ⅱ | 取I中上层清液,向其中滴加盐酸 | 无变化 | 无变化 |
| Ⅲ | 取I中上层清液,向其中滴加BaCl2溶液 | 无变化 | 无变化 |
| Ⅳ | 取I中上层清液,向其中滴加AgNO3溶液 | 白色沉淀 | 白色沉淀 |
| Ⅴ | 另取黑色粉末加入足量盐酸 | 大量气泡,溶液呈浅绿色 | 无气泡,溶液呈黄色溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
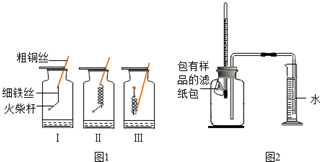
| 序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
| 1 | 1g铁粉、0.2g碳和10滴水 | 100 | 72 | 约120 |
| 2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 72 | 约70 |
| 3 | 1g铁粉和10滴水 | \ | \ | \ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
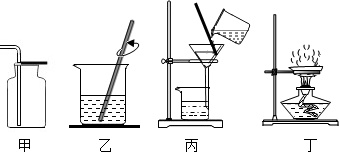
| A. | 用装置甲收集氧气 | |
| B. | 用装置乙溶解完全反应后的固体 | |
| C. | 用装置丙分离MnO2和KCl溶液 | |
| D. | 用装置丁蒸发分离后的溶液得KCl晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
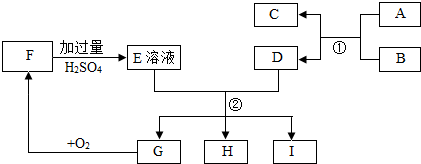
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 17.5g | B. | 15g | C. | 12.5g | D. | 6.25g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com