
����Ŀ��Ũ�������ǿ��ʴ�ԣ���̼��Ũ�����ϼ��������������С����Ϊ���������������CO��CO2��SO2���������е�һ�ֻ���֣�Ϊ�˽����ˣ�����̽����
���������ϣ�
��SO2��ʹƷ����Һ��ɫ��������������Һ��Ӧ�������գ���������������Һ��Ӧ����ʹ����ʯ��ˮ����ǣ�
��CO��CO2������ʹƷ����Һ��ɫ��Ҳ������������Һ��Ӧ��
��ʵ��̽����Ϊ��֤���������壬С������ʦ��ָ���£���Ʋ�������ͼ��ʾʵ�飺
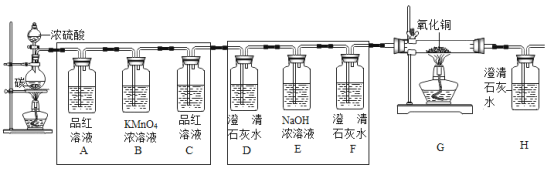
����������
ʵ������ | ʵ����� |
װ��A��Ʒ����Һ��ɫ | ��__���� |
__ | ��CO2���� |
װ��G������������ | __ |
����˼�����ۣ�
��1��װ��B�����Ը��������Һ��������__������װ��A��D�е��Լ�������__�����������������������ó���CO2�����Ľ��ۡ�
��2��д��̼��Ũ���ᷴӦ�Ļ�ѧ����ʽ__��
���𰸡�SO2 C��Ʒ����Һ����ɫ��D�г���ʯ��ˮ����� û��CO���� ����SO2����ֹ����CO2���� ���� C+2H2SO4��Ũ��![]() CO2��+2SO2��+2H2O
CO2��+2SO2��+2H2O
��������
ʵ��̽����
SO2��ʹƷ����Һ��ɫ�����A��Ʒ����Һ��ɫ��˵����SO2������
SO2��CO2����ʹD�г���ʯ��ˮ����ǣ�����C��Ʒ����Һ����ɫ��˵����SO2��D�г���ʯ��ˮ����ǣ�˵����CO2���������C��Ʒ����Һ����ɫ��D�г���ʯ��ˮ����ǣ�
�ڼ��ȵ������£�һ����̼��������ͭ��Ӧ����ͭ�Ͷ�����̼����װ��G������������˵��û��һ����̼���ɣ�
��˼�����ۣ�
��1��B�����Ը��������Һ������������SO2����ֹ����CO2���飻SO2��CO2����ʹD�г���ʯ��ˮ����ǣ����ж��Ƿ���CO2�������ʲ��ܽ�A��D���Լ�������
��2��C��Ũ�����ڼ��������£�����������ԭ��Ӧ���ɶ�����̼�����������ˮ������ʽΪ��C+2H2SO4��Ũ��![]() CO2��+2SO2��+2H2O��
CO2��+2SO2��+2H2O��


 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ���ҳ��õ�ʵ��װ�ã���ش��������⡣
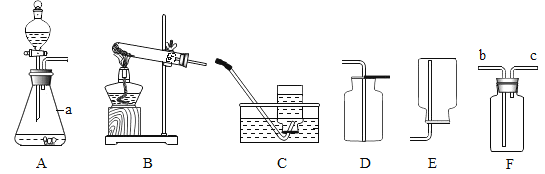
(1)�����a������:_________________��
(2)ʵ�����ø��������ȡ���ռ�һƿ�ϴ������������������________________(��װ����ĸ����)����д���÷�Ӧ�Ļ�ѧ����ʽ:_____________��
(3)ʵ���ҳ��ô���ʯ��ϡ���ᷴӦ��ȡ������̼������F�����ſ������ռ�������̼�����������̼�ռ����ķ�����______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ѧ��ȤС����ʵ�������ö������̺�Ũ�����ڼ�����������ȡ�����������й��������ʵ�ʵ��̽������ͼ��ʾ����
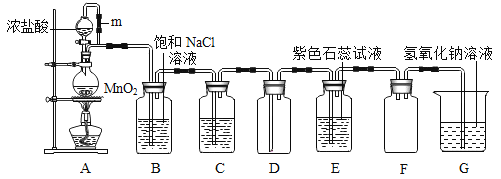
���������ϣ�
����������Cl2����һ�ֻ���ɫ���ж����壬������ˮ��������ˮ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ��![]() ��
��
������������ˮ���õ���ҺΪ��ˮ����ˮ���˾����������ã�HClO�������ᣩ������Ư�����ã�
����ϡ����Ͷ������̲�������Ӧ��
����������������������Һ��Ӧ��
�ش��������⣺
��1��A��m�ܵ�������_____��
��2��A����ȡ�����ķ���װ�ã���������������Ȼ��̣�����MnΪ+2�ۣ���һ�ֳ����������д���仯ѧ����ʽ_____��
��3��������װ��D�е������Ǵ�������ģ���װ��B�������Ȼ�����Һ����������_____��װ��C��ʢ�е���Һ��_____��
��4��װ��E��ʯ����Һ����ɫ�仯����Ϊ��_____��
��5����ʵ��װ��G��������_____��
��ͨ��������ʵ��ͼ��㷢�֣�ȡ������146g��Ũ����������Ķ������̷�Ӧ���õ�������Ϊ_____������ĸ����
A ��71g
B ����71g
C ����71g
D ����35.5g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����һ����̼��ԭ��������ʵ�飬���·���������ǣ���
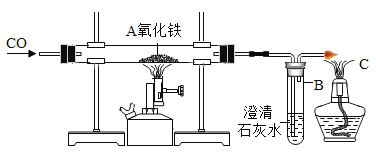
��֪�������ۡ�����������������������Ϊ��ɫ�����������������д��ԣ�
����������ԭ�������¶�Ӱ�������еģ�![]()
A.ʵ��ʱ��Ҫ��ͨ��һ����̼һ��ʱ�䣬���ܵ�ȼ�ƾ����
B.B ��ʯ��ˮ����ǿ���˵�� A ����Ӧ�Ѿ�����
C.C ����ȼ�ƾ��Ƶ������Ǵ���β����ֹ������Ⱦ
D.�� A ���������ұ�����������˵��������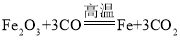 �ķ�Ӧ
�ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2017��5�£��ҹ������ȼ���Բɳɹ�����ȼ������Դ���ḻ�ĸ�Ч�����Դ�����ͷų����飬��ҵ�ϳ����ü������������÷�Ӧ����ʾ��ͼ��ͼ��ʾ������˵����ȷ���ǣ�������
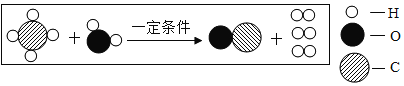
A.��Ӧǰ����ԭ�ӵĸ��������ı�
B.�÷�Ӧ���ڸ��ֽⷴӦ
C.���������������
D.�÷�Ӧ�Ļ�ѧ����ʽΪCH4+H2 CO+3H2��
CO+3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ���������˵�������ͨ������¿������Ӧ����������ѡ���У����ϸ�ͼҪ����ǣ� ��
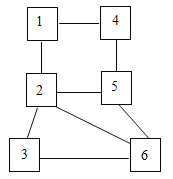
�� | �� | �� | �� | �� | �� | |
A | CO2 | NaOH��Һ | ϡHCl��Һ | Ca��OH��2��Һ | CuCl2��Һ | Fe |
B | CaO | ϡHCl��Һ | Fe | ϡH2SO4��Һ | Na2CO3��Һ | Ca��OH��2��Һ |
C | Fe | ϡH2SO4��Һ | BaCl2��Һ | Cu��NO3��2��Һ | Ca��OH��2��Һ | Na2CO3��Һ |
D | Zn | ϡHCl��Һ | CaCO3 | CuSO4��Һ | NaOH��Һ | FeCl3��Һ |
A.A
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧС����ͼ1װ����֤������̼��ˮ�ķ�Ӧ��

����Ũ�� | �۲쵽������ | |
���� | Ũ���ᣨ36.5%�� | B��ʯ����Һ����ɫ��ɺ�ɫ C��ʯ����Һû�б�Ϊ��ɫ |
���� | ϡ���ᣨ13.5%�� | B��ʯ����Һ����ɫ��Ϊ��ɫ C��ʯ����Һ��Ϊ��ɫ |
��1��A�з�Ӧ�Ļ�ѧ����ʽΪ_____��
��2������C�з�Ӧ�Ļ�ѧ����ʽΪ_____��
�������뽻����ͬѧ����Ϊ����C��ʯ����Һû�б�Ϊ��ɫ������ΪŨ����ӷ��������HCl����ʯ����Һ��
��������룩����Ļӷ�����Ũ���йء�
������ʵ�飩��ͼ2װ���о���ͬŨ������Ļӷ��ԡ������Ӵ������ⶨ�ձ���������Һ��������Ũ�ȣ�������Ũ�ȿ��Խ��Ʊ�ʾ�ӷ�����HCl��������ʵ�����ݼ��±���
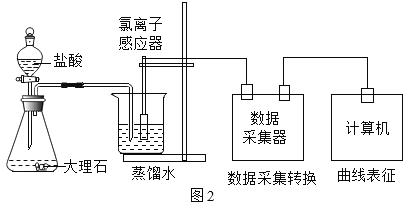
����Ũ����������Ũ�ȵĶ�Ӧ��ϵ����ͬʱ���ڲ�ã�
����Ũ�ȣ�%�� | 13.5 | 20 | 26.2 | 29.2 | 32.2 | 36.5 |
������Ũ�ȣ�mg/L�� | 1.1 | 1.4 | 3.7 | 19.0 | 59.8 | 209.2 |
���������������ܹ��ó�����Ļӷ�����Ũ�ȵĹ�ϵ��_____��
���ó����ۣ�������ȷ
��ʵ�鷴˼������ʯ����Һ��첻��֤��������̼��ˮ��Ӧ��
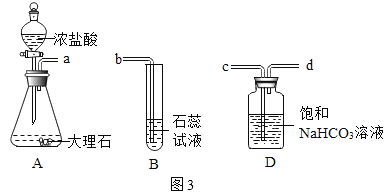
��ʵ��Ľ�������ͬѧ��װ��A��װ��B֮������װ��D������װ��֮�䵼�ܿڵ�����˳���ǣ�a��_____ ��_____��b��ѡ��NaHCO3��Һ���ӵ�ԭ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
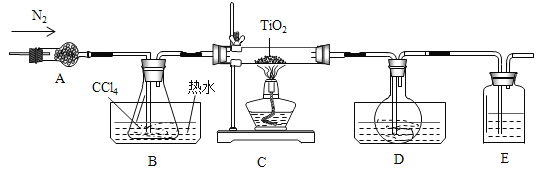
����Ŀ��ʵ�������÷�Ӧ��TiO2(s)+2CCl4(g)��TiCl4(g)+CO2(g)������ˮ���������£���ȡTiCl4ʵ��װ����ͼ��ʾ(s�������壬g��������)
�й��������±�
���� | �۵�/�� | �е�/�� | ���� |
CCl4 | ��23 | 76 | ��TiCl4���� |
TiCl4 | ��25 | 136 | ����ʪ������������ |
(1)װ��B��ˮ�ۡ���Ƥ�������ܺ�______(����������)��ɣ�
(2)װ��A��������______��װ��B����ˮ�¶�Ӧ_____�棻װ��Dˮ���е�������_____��װ��E�е��Լ���______��
(3)������������_______����Ӧ����ʱ���ν������²�������ֹͣͨ��������ȴ�����¢�Ϩ��ƾ��ơ���ȷ��˳��Ϊ__________(�����)��
(4)������D�е�Һ̬�����ɲ�ȡ�ķ�����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǽס��ҡ������ֹ������ʵ��ܽ�����ߣ������ͼʾ��գ�
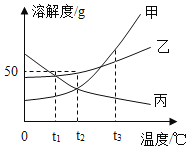
��1��t1��Cʱ���ס��ҡ����������ʵ��ܽ�ȴ�С��ϵ��_____��
��2��t2��Cʱ�������ʵı�����Һ�����ʡ��ܼ�������֮��Ϊ_____������������ȣ���
��3����������ͬ�����������ҡ���������Һ��Ӧ�����¶���_____��C��
��4����t2��Cʱ�ס��ҡ����������ʵı�����Һ���ֱ�����t1��C��������Һ���������������Ĵ�С��ϵ��_____��
��5��t2��C����40g������Ͷ��50gˮ�г���ܽ⣬������Һ������Ϊ_____g����ʹʣ����������ȫ�ܽ����ٻ����ˮ������Ϊ_____g��
��6�������к����������Һͱ�ʱ���ɲ���_____�������������������������ᾧ�ķ����ᴿ�����ʡ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com