
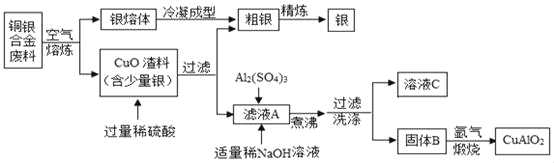
【题目】银铜合金广泛用于航空工业,以下为从航空切割废料中回收银并制备CuAlO2的工艺流程。
(资料)
Ⅰ.难溶性碱受热易分解为两种氧化物,Cu(OH)2、Al(OH)3完全分解的温度分别为80℃和450℃;
Ⅱ.CuAlO2高温易分解、受热易氧化,银在空气中不易被氧化。
请回答下列问题:
(1)可将铜丝浸入__________溶液中来验证铜、银两种金属的活动性强弱。
(2)固体B在煅烧时发生的其中一个反应方程式为4CuO+2Al2O3![]() 4CuAlO2+X↑,气体X的化学式为___________,CuAlO2中铜元素的化合价为__________。
4CuAlO2+X↑,气体X的化学式为___________,CuAlO2中铜元素的化合价为__________。
(3)煮沸过程中发生反应的化学方程式为__________。
(4)“煅烧”时温度须控制在1042﹣1085℃范围内且在氩气中进行,其原因是__________。
【答案】AgNO3;O2;+1;Cu(OH)2![]() CuO+H2O;防止温度过高CuAlO2分解和氧化。
CuO+H2O;防止温度过高CuAlO2分解和氧化。
【解析】
(1)要证明铜和银的活动性强弱,可以将铜丝浸入到硝酸银溶液中,如有银析出,说明铜比银活泼。
(2)4CuO+2Al2O3![]() 4CuAlO2+X↑,反应前含有4个Cu原子,10个O原子,4个Al原子,反应后含有4个Cu原子,4个Al原子,8个O原子,故X中含有2个O原子,其化学式为O2,设CuAlO2中铜元素的化合价为x,则有:x+(+3)+(﹣2)×2=0,x=+1。
4CuAlO2+X↑,反应前含有4个Cu原子,10个O原子,4个Al原子,反应后含有4个Cu原子,4个Al原子,8个O原子,故X中含有2个O原子,其化学式为O2,设CuAlO2中铜元素的化合价为x,则有:x+(+3)+(﹣2)×2=0,x=+1。
(3)氧化铜和硫酸反应生成硫酸铜和水,故得到的滤液A中含有硫酸铜和剩余的硫酸,加入氢氧化钠溶液和硫酸铝溶液,则氢氧化钠会与硫酸反应生成硫酸钠和水,氢氧化钠会与硫酸铜反应生成氢氧化铜,与硫酸铝反应生成氢氧化铝,煮沸则温度最高达到100℃,由于Cu(OH)2、Al(OH)3完全分解的温度分别为80℃和450℃故煮沸时发生的反应是氢氧化铜的分解反应,反应方程式为Cu(OH)2![]() CuO+H2O;
CuO+H2O;
(4)由于CuAlO2高温易分解、受热易氧化,故“煅烧”时温度须控制在1042﹣1085℃范围内且在氩气中进行,是为了防止温度过高CuAlO2分解和氧化。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】在0 ℃时,配成甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),如图所示。将烧杯中的水持续升温,固体物质质量变化情况如图Ⅱ所示。则下列说法正确的是( )

A. 甲溶液中溶质的质量分数随温度升高不断增大
B. t ℃时,甲、乙两物质的溶解度一定相等
C. 通过升温可以将甲的饱和溶液变为不饱和溶液
D. 乙物质的溶解度随温度升高而增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在点燃条件下,A和B反应生成C和D,反应前后变化的微观示意图如下所示。
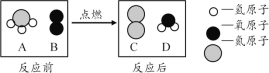
根据上述信息可得出( )
A. 该反应不满足质量守恒定律 B. 原子在化学反应中不可再分
C. 该反应的类型是化合反应 D. 反应前后分子不发生改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,在试管中的滤纸条上A、B、C三处各滴上一滴无色酚酞,再在试管口放一团棉花。

(1)用仪器X吸取浓氨水,滴在棉花上,X的名称是什么_________?
(2)实验中,往往在试管下放一张白纸,其作用是什么_________?
(3)张华同学在做此实验时,发现滤纸条上没有变色,而试管中所塞的棉花却变成了红色,写出导致产生这种现象的错误操作_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学常见六种物质之间的关系图(物质是溶液的只考虑溶质)。图中用“﹣”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质(部分反应物或生成物及反应条件已略去)。A中含有人体中含量最多的金属元素,B、C中不含相同元素。C、D中所含元素种类相同。
(1)请分别写出A、C物质的化学式(或溶质的化学式):A.____________C.______;
(2)写出转化①的化学方程式_________________(写一个);
(3)写出Fe2O3与足量B反应的实验现象_________________。
(4)D在生活中的一种用途______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学进行“物质溶解的吸热或放热”的探究实验.他取三支试管,向试管中分别注入![]() 水,测得水的初温为
水,测得水的初温为![]() ,再分别向三支试管中各加入
,再分别向三支试管中各加入![]() 、
、![]() 、
、![]() 固体,振荡.
固体,振荡.
![]() “振荡”试管的目的是________.
“振荡”试管的目的是________.
![]() 用温度计分别测三支试管中溶液的温度,高于
用温度计分别测三支试管中溶液的温度,高于![]() 的是________溶液,这是因______.
的是________溶液,这是因______.
![]() 装有
装有![]() 溶液的试管外壁有水珠产生,原因是________.
溶液的试管外壁有水珠产生,原因是________.
![]() 由此探究实验可知________溶于水温度没有明显的变化.
由此探究实验可知________溶于水温度没有明显的变化.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】![]() 月
月![]() 日是“世界水日”.水与人类的生活和生产密切相关.
日是“世界水日”.水与人类的生活和生产密切相关.
![]() 天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化.其中净化程度最高的是________.
天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化.其中净化程度最高的是________.
![]() 硬水给生活和生产带来很大不利影响,生活中可用________来区分硬水和软水.
硬水给生活和生产带来很大不利影响,生活中可用________来区分硬水和软水.
![]() 生活中通过________可以降低水的硬度.
生活中通过________可以降低水的硬度.
![]() 日常生活中你经常采用的节水措施有________.
日常生活中你经常采用的节水措施有________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行探究。
(提出问题)①三种溶液的酸碱性?②它们与酸反应时溶液的pH如何变化?
(查阅资料)
pH | 2~3 | 4~6 | 7 | 8~9 | 10~11 | 12~14 |
紫甘蓝汁液显示的颜色 | 紫红 | 浅紫 | 紫色 | 蓝色 | 绿色 | 黄色 |
(实验1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 紫色 | 蓝色 | 绿色 | 黄色 |
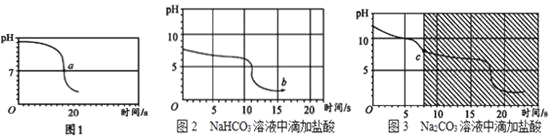
(实验2)向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图1所示。
(实验3)向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图2、图3所示。将图2与图3的阴影部分进行叠加,发现两者基本重合。
(解释与结论)
(1)实验1得出三种溶液中碱性最强的为______________溶液。
(2)实验2证明了氢氧化钠能与盐酸发生反应,其理由是______________,该反应的化学方程式为______________。若取出少量a点的溶液,向其中滴加紫甘蓝汁液,观察到的现象是______________。
(3)实验3中,b点的溶质为______________,实验3中,c点后发生反应的化学方程式为_____________。
(4)依据实验3,加入足量的盐酸,产生二氧化碳的量______________。
A.碳酸氢钠多 B.碳酸钠多
C.两者一样多 D.不能确定哪个多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在“粗盐中难溶性杂质的去除”的实验课上,同学们制得了“白色的盐”,小刚很高兴,并大声地说:“我制得了纯净的NaCl。”老师否定了他的说法,并解释说:“同学们制得的白色的盐中除了含有NaCl外,还含有MgCl2、CaCl2、Na2SO4等可溶性杂质。”于是,同学们为了得到更纯的NaCl,设计了如下的实验方案:
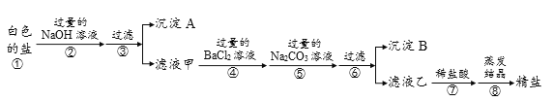
请回答下列问题:
(1)沉淀A的化学式是_________。
(2)若将步骤④和⑤顺序颠倒会引发的后果是_____________________。
(3)沉淀B中除了含有CaCO3以外还含有_______________。(填化学式)
(4)滤液乙中含有的阴离子是__________。(填离子称号)
(5)小刚向滤液乙中,滴入几滴稀盐酸后就进行蒸发操作。丽丽马上制止,并设计实验, 探究蒸发皿内溶液中除了NaCl以外,是否还含有其他溶质。于是,取少量该溶液于试管中,接下来进行的操作是______________,观察到的现象是___________________________________。
由此得出该溶液中溶质成分为NaCl和Na2CO3。如果用该溶液蒸发结晶,则得不到更纯的NaCl。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com