
【题目】小明同学取14%的硫酸溶液70g于烧杯中,然后向烧杯中慢慢加入10g氧化铜粉末并不断搅拌,测得烧杯中溶液的质量与加入氧化铜粉末的质量关系如图所示。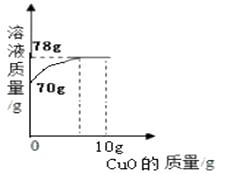
求:
(1)完全反应时共消耗氧化铜的质量为g;
(2)配制14%的硫酸溶液70g,需要98%的硫酸溶液g;
(3)反应后所得溶液中溶质的质量分数为多少?(写出计算过程,最后结果保留到小数点后1位)
【答案】
(1)8
(2)10
(3)解:设生成硫酸铜的质量为x。
CuO + | H2SO4 = | CuSO4+H2O |
80 | 98 | 160 |
8g | x |
![]()
x = 16g
反应所得溶液中溶质的质量分数= 16g÷78g×100% =20.5%
答: 反应所得溶液中溶质的质量分数为20.5%。
【解析】根据质量守恒定律知(1)完全反应时共消耗氧化铜的质量为78g-70g=8g. (2)配制14%的硫酸溶液70g,需要98%的硫酸溶液质量为x
70g×14%=98%×x,x=10g.(3)反应后所得溶液中溶质的质量分数为
解:设生成硫酸铜的质量为x。
CuO + | H2SO4 = | CuSO4+H2O |
80 | 98 | 160 |
8g | x |
![]() =
= ![]() ,x=16g.
,x=16g.
反应后所得溶液中溶质的质量分数为 ![]() ×100%=20.5%.
×100%=20.5%.
答∶(1)完全反应时共消耗氧化铜的质量为8g.(2)配制14%的硫酸溶液70g,需要98%的硫酸溶液是10g.⑶反应所得溶液中溶质的质量分数为20.5%。
点睛∶本题主要考查质量守恒定律的应用和根据化学方程式进行计算。
(1)由氧化铜和硫酸反应生成硫酸铜和水这个反应可知,反应后溶液质量增加的量就是氧化铜的质量
(2)利用氧化铜的质量结合化学方程式可计算硫酸铜的质量,溶质质量分数=溶质质量![]() 溶液质量×100%
溶液质量×100%


科目:初中化学 来源: 题型:
【题目】实验室利用反应所得CuSO4、稀H2SO4混合液制备CuSO45H2O,其主要流程如下:
(1)试剂X应选用 (选填序号)。
a.Cu b.CuO c.Fe
写出混合液中加入过量X后发生的反应方程式。
(2)操作A中,所用玻璃仪器有、玻璃棒、烧杯。
(3)操作B为蒸发浓缩、过滤。
(4)操作C为洗涤、低温干燥,其中洗涤剂不可选用 (选填序号)。
a.热水 b.冰水 c.饱和CuSO4溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铬(Cr)是银白色光泽的金属,含铬、镍的钢称为不锈钢,具有极强的抗腐蚀性。
(1)纯铁与不锈钢相比较,硬度较大的是_____。
(2)已知铬能与稀盐酸反应生成+2价的化合物,请写出该反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源。下列有关水的说法错误的是
A.水在固态时分子是静止不动的B.保持水的化学性质的微粒是水分子
C.可用肥皂水区分硬水和软水D.水是由氢元素和氧元素组成的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用如图所示装置可以进行金属性质的探究。

(1)若装置A中盛放硫酸铜溶液,可观察到什么现象?
(2)若将铁片浸入装置A的溶液中,观察到铁片表面有气泡产生,写出有关反应的化学方程式(写出一个即可)。
(3)利用装置B探究Fe、Cu、Ag三种金属的活动性顺序时,装置B中金属片和溶液中的溶质应分别选择什么物质(写出一组即可)?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】绿水青山就是金山银山。下列做法不符合这一理念的是
A.无纸化办公,低碳出行,减少资源消耗
B.推广使用滴、喷灌技术,高效利用水资源
C.生活垃圾深埋处理,减少对地表的污染
D.退耕还草,植树造林,提高植被覆盖率
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质的用途与性质对应关系错误的是
A | B | C | D | |
物质 | 一氧化碳 | 稀有气体 | 干冰 | 石墨 |
用途 | 冶炼金属 | 保护气 | 人工降雨 | 电极 |
性质 | 还原性 | 通电后能发出有色光 | 易升华吸热 | 导电性 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com