
【题目】实验探究、科学精神是我们应具备的学科素养。化学兴趣小组的同学对实验室制取二氧化碳进行探究,请你一起参与。
(查阅资料)(1)稀硫酸能与大理石反应,生成的硫酸钙微溶于水;
(2)稀盐酸显酸性,可使紫色石蕊溶液变红。
(选用药品)按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如下图所示:
实验编号 | 药品 |
Ⅰ | 块状大理石、10%H2SO4溶液 |
Ⅱ | 块状大理石、7%HCl溶液 |
Ⅲ | 大理石粉末、7%HCl溶液 |
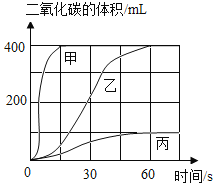
图中丙对应实验_________(选填” Ⅰ”、” Ⅱ”或” Ⅲ”)。确定用乙对应的药品制备二氧化碳,相应的化学方程式是___________;不选择甲对应的药品,理由是______________。
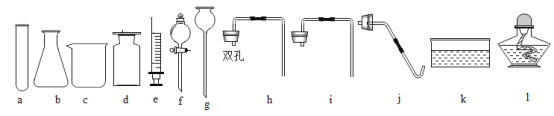
(选择仪器)小组同学从图 2 所示仪器中组装一套可控制反应速率的制取装置,你认为他们选择的仪器是__________(填序号)
(收集气体)用如图装置收集二氧化碳,空气从_____________(选填”X”或”Y”)端排出。
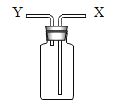
(检验气体)检验产生的气体为二氧化碳的方法是_________________。
(拓展创新)实验结束后,小组同学对装置中的废液产生了兴趣,有同学认为可能稀盐酸有剩余,欲证明该猜想是正确的,可向废液中加入______________,会出现_________的现象。
【答案】I CaCO3+2HCl=CaCl2+H2O+CO2↑ 反应速率太快,不易收集 bdfh Y 将生成的气体通入澄清石灰水中,澄清石灰水变浑浊 碳酸钠(合理均可) 产生气泡
【解析】
碳酸钙和硫酸反应生成的硫酸钙微溶于水,会阻碍反应的继续进行,所以图中丙对应实验I;碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;甲反应生成二氧化碳的速率太快,所以不选择甲对应的药品,理由是:反应速率太快,不易收集;
[选择仪器]
分液漏斗可以控制液体的滴加速度,制取二氧化碳反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,所以选择的仪器是bdfh;
[收集气体]
二氧化碳密度比空气大,所以用图 3 装置收集二氧化碳,二氧化碳从X端进入,空气从Y端排出;
[检验气体]
二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以检验产生的气体为二氧化碳的方法是:将生成的气体通入澄清石灰水中,澄清石灰水变浑浊;
[拓展创新]
盐酸和碳酸钠反应会生成二氧化碳气体,会看到有气泡产生,所以有同学认为可能稀盐酸有剩余,欲证明该猜想是正确的,可向废液中加入碳酸钠,会出现产生气泡的现象。


科目:初中化学 来源: 题型:
【题目】如图所示,下列说法错误的是( )
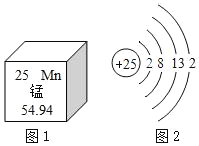
A. 锰元素属于金属元素
B. 它的化学性质与氦元素的相似
C. 锰是第四周期元素
D. 锰元素的相对原子质量是54.94
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】保险粉(化学式Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在NaCl存在的条件下,Na2S2O4在水中的溶解度显著下降。Na2S2O4 制备流程如下图所示:
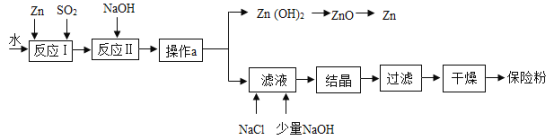
(1)反应I的原理为: ![]() , 该反应类型为_____。
, 该反应类型为_____。
(2)操作a的名称为_____。
(3)滤液中含有Na2S2O4, 往滤液中加入NaCl和少量NaOH的原因分别是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“五一”假期,聪聪同学和家入到故宫去参观,发现故宫内许多铜制品表面有一层绿色物质。绿色物质是什么?它是怎样形成的?化学活动课上,同学们设计实验对这种绿色物质进行了如下探究活动。
[查阅资料]
①铜在空气易生成铜锈,它为绿色,其主要成分是Cu2(OH)2CO3;
②白色的硫酸铜粉末遇水能变为蓝色。
探究活动一:验证铜锈的组成。
[进行实验1]
同学们设计了如图所示装置并进行实验。
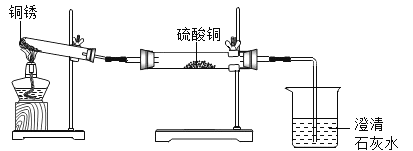
实验操作 | 实验现象 | 实验结论 |
①按上图组装仪器,装入药品。 ②加热铜锈,直至不再有气体产生。 | 绿色固体变为黑色,硫酸铜粉末变为蓝色,烧杯中液体变浑浊 | 加热铜锈生成的物质有CuO、_____,烧杯中发生反应的化学方程式为___________ |
③冷却后,向试管中黑色固体加入适量稀硫酸。 | 黑色固体溶解,溶液变为蓝色 |
探究活动二:探究铜生锈的条件。
[进行实验2]
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显。
序号 | 实验内容 | 实验现象与结论 |
实验1 |
| 在干燥环境中,铜不生锈 |
实验2 |
| 铜仅与氧气和水接触,不生锈 |
实验3 |
| 铜仅与二氧化碳和水接触,不生锈 |
实验4 |
| 铜生锈,它生锈的条件是___________________ |
/span>
[反思与拓展]
(1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其目的是__________________。
(2)如果要除去铜制品表面的铜锈,可以用稀盐酸浸泡,写出反应的化学方程式___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】华为公布了全球首款柔性屏幕的 5G 折叠手机,国内 5G 通信芯片用氮化镓材料制成。如图是氮元素在元素周期表中的信息及镓原子的结构示意图。下列说法不正确的是
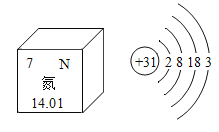
A.氮原子核内质子数为7B.镓原子属于金属原子
C.镓原子核内中子数为31D.氮原子的相对原子质量为14.01
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】宏观辨识与微观探析是化学学科的重要核心素养,某反应的微观示意图如下,下列有关说法正确的是
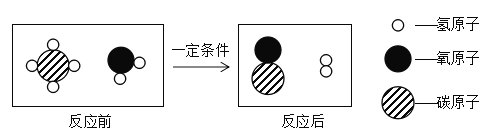
A.该反应的反应物都是氧化物
B.该反应不遵守质量守恒定律
C.该反应中原子的种类和个数不变
D.该反应的化学方程式中CO和H2的化学计量数之比为1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定量的氢氧化钠和碳酸钠的混合溶液中逐滴滴加稀盐酸,甲图为溶液的pH变化情况,乙图为生成气体质量情况。下列说法正确的是
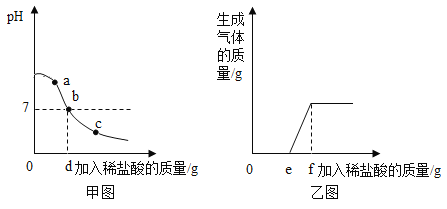
A.甲图中的c点表示溶液显碱性
B.加入的稀盐酸只与碳酸钠发生反应
C.甲图中的a点表示溶液中只含有Na+、 Cl-、OH-
D.甲图中的d与乙图中的f表示的数值相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象与对应实验相符合的是
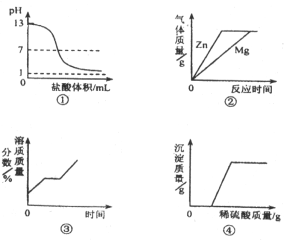
A.图①表示向pH=13的氢氧化钠溶液中逐滴加入pH=1的 盐酸
B.图②表示向溶质质量分数相同、等质量的稀硫酸中分别加入足量的金属镁和锌
C.图③表示将一定质量的不饱和硝酸钾溶液恒温蒸发至有晶体析出
D.图④表示向氢氧化钠与氯化钡的混合溶液中逐滴加入稀硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图所示为实验室 中常见气体制备、干燥、收集和性质实验的部分仪器装置(组装实验装置时,可重复选择)。某学校两个化学实验探究小组的同学欲用它们完成各自的探究实验,试根据题目要求,回答下列问题:
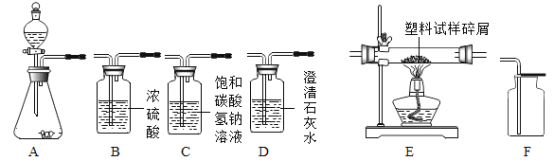
(1)第一组的同学以石灰石和稀盐酸为原料,在实验室制备、收集干燥纯净的二氧化碳气体。 (提示:挥发出的少量HCI气体可用饱和碳酸氢钠溶液吸收)
①所选仪器的连接顺序为_____(填写仪器装置序号字母)。
②写出实验室制取二氧化碳的反应方程式_____。
(2)第二组的同学以过氧化氢溶液为原料(MnO2 为催化剂)制备氧气,并对某种塑料的组成元素进行分析探究(资料显示该塑料含C、H、O三种元素),设计的装置顺序为“A→E→B→D→碱石灰干燥管”。
①装置D中的明显实验现象是_____。
②装置E的玻璃管中放入的塑料碎屑质量为wg,塑料试样充分燃烧后,测得仪器B的质量增加mg,装置D增重ng,则该塑料试样中碳元素的质量为_____(用分数形式表示),按上面设计的装置顺序测算出的该塑料试样中氢元素元素与碳元素的质量比与实际值相比将_____ (填“偏小”“偏大” “基本一致”之一)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com