
【题目】盐城的城市建设可谓是日新月异,在城市建设、生产、生活中材料有着广泛的应用。
(1)下列生活用品,主要利用金属具有良好导热性的是________(填序号),一般铜导线外面包有聚乙烯绝缘层,聚乙烯属于________材料。

(2)铁制品在空气中会发生锈蚀,其原因是铁与空气中的___________共同作用的结果。为防止钢铁制品的锈蚀,厨房中的铁锅和菜刀通常需做的防护是_____________(要求一种方法即可)。
(3)化学小组为了验证铁、铜、镁、汞的金属活动性顺序,设计了如下实验方案:
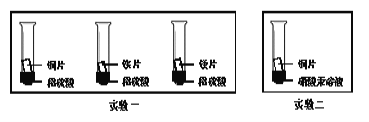
根据实验一判断出镁的金属活动性比铁强,依据的现象是___________;根据实验二的现象应得出的结论是__________。
(4)苗苗同学向含有FeSO4和CuSO4两种溶质的溶液中,加入一定质量镁粉,充分反应后过滤,滤液呈浅绿色,再向滤液中放入一枚洁净的铁钉,足够时间后取出,铁钉表面无变化。根据此现象作出了下列判断,你认为正确的是_____________(填序号)。
A. 滤纸上一定有Fe,可能有Mg、Cu
B. 滤纸上一定有Cu,可能有Fe,一定没有Mg
C. 滤液中一定有FeSO4,可能有MgSO4 、CuSO4
D. 滤液中一定有MgSO4、FeSO4,一定没有CuSO4
(5)为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如表:
第I组 | 第Ⅱ组 | 第Ⅲ组 | |
稀硫酸的质量/g | 50 | 100 | 150 |
溶解固体的质量/g | 10.0 | 16.0 | 16.0 |
根据实验及有关数据进行分析与计算:
①第I组实验中反应物___________(填“氧化铜“、“稀硫酸”或“氧化铜与稀硫酸”)反应完。
②20g样品中含氧化铜的质量分数分别为____________。
③计算所用的稀硫酸溶质的质量分数为____________(写出计算过程)
④将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图。
 ___________________
___________________
【答案】 A 合成 O2\H2O 洗净擦干(合理即可) 镁与稀硫酸反应产生气泡的速率快 Cu的活动性比Hg强 B D 稀硫酸 80% 24.5% 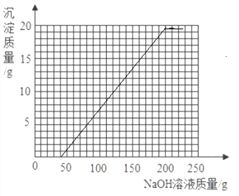
【解析】(1)铁锅主要利用金属具有良好导热性;铜导线主要利用了金属的延性和导电性;铝箔主要利用了金属的展性;铁锤主要利用金属的硬度、强度大的性质;聚乙烯属于塑料的一类,属于有机高分子合成材料;(2)铁制品在空气中会发生锈蚀,其原因是铁与空气中的氧气、水共同作用的结果。为防止钢铁制品的锈蚀,厨房中的铁锅和菜刀通常需做的防护是用完后及时擦干;(3) 金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。判断出镁的金属活动性比铁强,依据的现象是镁与稀硫酸反应产生气泡的速率比铁快;实验二的现象是铜的表面有银白色固体生成,溶液由无色变成蓝色,说明铜能与硝酸汞反应,应得出的结论是Cu的活动性比Hg强;(4)向含有FeSO4和CuSO4两种溶质的溶液中,加入一定质量镁粉,镁先与硫酸铜反应,然后再与硫酸亚铁反应。充分反应后过滤,滤液呈浅绿色,说明硫酸亚铁有剩余、镁粉一定完全反应;再向滤液中放入一枚洁净的铁钉,足够时间后取出,铁钉表面无变化,说明硝酸铜完全反应。故反应后溶液中的溶质有剩余的硫酸亚铁和生成的硫酸镁;固体中一定有铜,可能有铁;选BD;(1)由题中的数据分析可知,20g样品中含氧化铜的质量16g,样品中氧化铜的质量分数:16g÷20g×10%=80%;由题中数据分析知,10g氧化铜一定能将50稀硫酸中的溶质完全反应。
(2)设:稀硫酸的溶质质量分数为x
CuO+H2SO4═CuSO4+H2O
8098
10g50gx
80/10g=98/50gx
x=24.5%
答:所用稀硫酸的溶质质量分数为24.5%.
(3)设和16g氧化铜反应的稀硫酸质量为y,生成的硫酸铜的质量为z.
CuO + H2SO4 ═ CuSO4+H2O
80 98 160
16g 24.5%y z
80/98=16g/24.5%y y=80g
80/160=16g/z z=32g z=32g
设和(100g-80g)稀硫酸反应的氢氧化钠溶液的质量为m.
H2SO4 + 2NaOH=Na2SO4+2 H2O
98 80
(100g-80g)×24.5% 10%m
![]()
解得m=40g因为向有稀硫酸和硫酸铜的溶液中滴加氢氧化钠溶液时,可以看成氢氧化钠溶液先和硫酸反应,再和硫酸铜反应,所以我们得到起点坐标(40,0).
设和生成的硫酸铜反应的氢氧化钠溶液的质量为n,反应生成的沉淀的质量为w.
CuSO4 + 2NaOH = Cu(OH)2↓+Na2SO4
160 80 98
32g10%n w
![]()
解得n=160g,w=19.6g
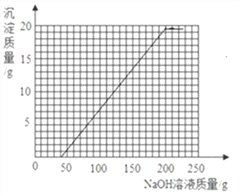
和剩余的稀硫酸以及硫酸铜反应的氢氧化钠溶液的质量总和是40g+160g=200g,所以我们得到折点坐标(200,19.6),故绘制图象如下图.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:初中化学 来源: 题型:
【题目】通过一年的化学学习,相信你已经掌握了一些化学知识与技能。请结合下列实验装置图回答问题。
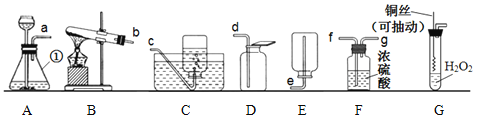
(1)写出图中①的仪器名称:_____________。
(2)实验室用过氧化氢制取氧气的化学方程式为______________________________,若要将产生的气体进行干燥,则应将a与F中的_________(选填小写字母)相连接。
(3)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂。现有一根洁净的铜丝,实验前先将其烧成螺旋状,再经过加热处理。改进捕捉发生装置如图G所示。与装置A比较,改进后装置的优点是____________。
(4)甲烷是一种无色、无味、难溶于水、密度小于空气的气体,实验室若用加热无水醋酸钠和碱石灰的固体混合物的方法制取纯净的甲烷,选用的发生装置和收集装置为___________、_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是一切生物生存所必须的宝贵资源,我们应该了解有关水的一些知识。
(1)为了防止水的污染,下列做法有利于保护水资源的是_____(填序号):
①抑制水中所有动、植物的生长 ②不任意排放工业废水 ③大量使用化肥农药 ④生活污水经过净化处理后再排放
(2)有一种环保型消毒液发生器,其中发生的反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式为_____;从能量变化角度看,该反应将电能转化为_____能。
(3)溶液在生产生活中有广泛的应用。某同学配置溶液时,在用量筒量取所需水的过程中,他俯视读数,这样配置得到的溶液溶质质量分数会_____(填“偏大”、“偏小”或“无影响”).10%的CaCl2溶液可用作路面保湿剂,欲配置100kg该路面保湿剂,需要水的质量_____kg。
(4)人们常饮用的一种矿泉水的标签如图所示,其中所含镁离子的离子符号为_____,该矿泉水是_____(填“中性”“酸性”或“碱性”),人体吸收该矿泉水中含有的某一元素可以防止佝偻病,这种元素是_____(填元素符号)。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示的溶解度曲线(
A. B都为固态物质),判断下列说法中正确的是( )
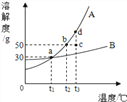
A.t1℃时,A和B饱和溶液的质量分数都为30%
B. t3℃时,A的溶解度比B大,故A溶液的质量分数也一定比B溶液大
C. B的浓溶液的质量分数一定比A的稀溶液大
D. 把c点对应A的溶液降温至t2℃可得A的饱和溶液,继续降温可析出A晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】食品与健康、能源与环境是我们共同关注的社会问题.
(1)紫薯营养丰富,具有特殊的保健功能。紫薯中富含淀粉、维生素C、维生素B、铁、钙、硒等。
①这里的“铁”、“钙”是指_________(填字母序号)
A.原子 B.分子 C.元素 D.单质
②人体缺“铁”,会导_________病症;③紫薯中能给人体提供能量的物质是__________;
(2)天然气是汽车使用的燃料之一,其主要成分燃烧反应的化学方程式是_____________ 。
(3)二氧化碳是造成温室效应的主要气体,从“低碳”的角度分析,应尽量减少二氧化碳的排放。
①在氢气、煤、石油中,最理想的燃料是___________;
②将排放出的二氧化碳吸收并转化为可再利用的物质是科学家研究的方向。检验吸收后的气体中是否含有二氧化碳,依据反应的化学方程式是_____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测得工业纯碱中碳酸钠的质量分数(常含少量NaCl),小明同学设计的实验装置如图甲,准确称取一定量的纯碱样品,从分液漏斗中滴入稀硫酸。已知碱石灰既能吸收水也能吸收二氧化碳。

(1)图甲中仪器a内发生的化学方程式为______________________。
(2)小红觉得小明的实验装置会导致较大的误差,故设计了图乙的装置,请你写出图乙装置的优势(写出两点即可):_________________、______________。
(3)小红用图乙装置进行实验,步骤为:①准确称取盛有碱石灰的干燥管的质量为158.0 g,再准确称取11.0 g纯碱样品并全部放入A中;②组装全部反应装置并检查气密性,关闭d;由e逐滴加入稀硫酸至不再产生气泡为止;③打开d,慢慢鼓入空气10 min;④再称干燥管的总质量为162.4 g。该产品中碳酸钠的质量分数为_______________(结果精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们巳经在全球范围内的碳循环的研究方面取得了不少进展,以下是利用二氧化碳的操作流程图,能让化学反应更好地为人类造福 。
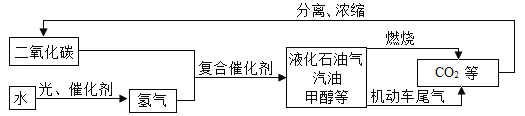
(1)从图中分析得出的下列结论中 正确的是 (填序号)_______。
A.该技术与我们大力提倡的低碳生活理念相符合。
B.水制取氢气的催化剂定是二氧化锰
C.该技术有助于缓解全球面临的能源危机
D.液化石油气、汽油 、 甲醇燃烧后的产物只有二氧化碳
(2)二氧化碳与氢气在催化剂、高温条件下,除生成甲醇( CH3OH )外,还生成种常温下为液态的化合物,写出反应的化学方程式:________________________________。
(3)控制条件可以使CO2和物质R反应制得尿素[CO(NH2)2]外,发生反应的化学方程式为![]() ,物质 R 的化学式为_____________________。
,物质 R 的化学式为_____________________。
(4)液化石油气 、汽油 、 甲醇燃烧时氧气浓度越大,燃烧越剧烈,试从微观角度解释其原因:________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋中有丰富的资源,海水晒盐后,分离出食盐的海水称为苦卤水,其中含有丰富的MgCl2。工业上以苦卤水为原料制取金属镁(Mg)的流程如下:
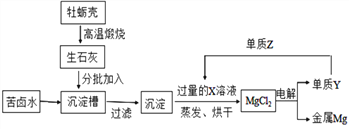
(1)从海水中析出食盐的结晶方法是______________
(2)Y与 Z 反应后的产物溶于水可得 X 溶液,从而实现了 Y 的循环利用,则 Z 的化学式为_____________
(3)烘干后得到的MgCl2中可能含有的杂质是_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com