
【题目】“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气 等。化学兴 趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如下图所示。同学们 对这包久置的“双吸剂”固体 样品很好奇,设计实验进行探究。

(提出问题)久置“双吸剂”固体的成分是什么?
(查阅资料)
①铁与氯化铁溶液在常温下反应生成氯化亚铁:Fe+2FeCl3=3FeCl2;
②碱性的 Na2CO3溶液可以与中性的 CaCl2 溶液发生复分解反应。
(作出猜想)久置固体中可能含有 Fe、Fe2O3、CaO、Ca(OH)2 和 CaCO3。
(定性研究)小明取少量样品放入试管中,加入一定量的稀盐酸,发现,试管中固体质量逐渐减少,生成一种 能使澄清石灰水变浑浊的气体,得到浅绿色溶液,他初步判断:样品中一定含有_____,一定不含 Fe2O3。
(实验质疑)小组同学谈论认为上述实验并不能得出一定不含 Fe2O3的结论,理由是_____,(用化学方程式表示)。为进一步确定这包久置的“双吸剂”固体的成分进行如下定量实验。
(定量研究)取 3g 样品研碎,并用磁铁充分吸引后,得到剩余固体 2. 6g,按照如图流程进行实验,请回答相 关问题:
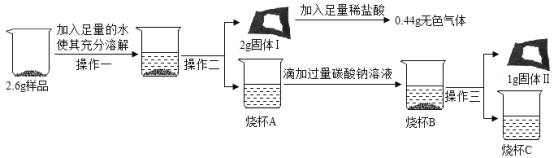
(1)操作二、操作三名称是_________________________。
(2)固体 I 的成分是_______________________。(填物质化学式,下同);
(3)写出生成固体Ⅱ的化学方程式_______________________。
(4)根据定性、定量研究中现象的分析及有关数据计算判断,这包久置“双吸剂”固体的成分中氧化钙的质量小于__________________。
(实验反思)结合上面的实验,下列说法正确的是______________________(填字母序号)
A对物质成分的研究有时需要定性和定量相结合
B在原样品中加入足量盐酸有 4 个反应发生
C定量研究烧杯 C 中的溶质为 NaOH 和 Na2CO3
【答案】CaCO3、Fe Fe2O3+6HCl=2FeCl3+3H2O;Fe+2FeCl3=3FeCl2 过滤 CaCO3、Fe2O3 Na2CO3+Ca(OH)2=2NaOH+CaCO3↓ 0.56g AC
【解析】
定性研究:小明取少量样品放入试管中,加入一定量的稀盐酸,发现,试管中固体质量逐渐减少,生成一种能使澄清石灰水变浑浊的气体,二氧化碳气体能使石灰水变浑浊,则样品中一定含有碳酸钙,碳酸钙与稀盐酸反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑;稀盐酸与铁反应得到浅绿色氯化亚铁溶液和氢气,反应原理为:Fe+2HCl=FeCl2+H2↑,初步判断:样品中一定含有:CaCO3和Fe,一定不含 Fe2O3。
实验质疑:小组同学谈论认为上述实验并不能得出一定不含 Fe2O3的结论,理由是:盐酸与氧化铁反应生成棕黄色氯化铁溶液和水,反应原理为:Fe2O3+6HCl=2FeCl3+3H2O,氯化铁溶液可以继续和铁反应生成氯化亚铁溶液:Fe+2FeCl3=3FeCl2,所得氯化亚铁溶液依然为浅绿色;
(1)操作二、操作三都是分离不溶性固体和液体,操作名称为:过滤;
(2)固体 I 的成分是;CaCO3和Fe2O3;因为2g固体中加入足量盐酸生成0.44g气体,
若生成的0.44g气体全部为二氧化碳,设:碳酸钙的质量为x,
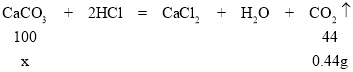
![]() x=1g,小于固体质量Ⅰ中的2g,则固体中不止含有碳酸钙,还有氧化铁固体;
x=1g,小于固体质量Ⅰ中的2g,则固体中不止含有碳酸钙,还有氧化铁固体;
(3)烧杯A中只有氢氧化钙溶液,加入足量的碳酸钠溶液,氢氧化钙与碳酸钠反应原理为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(4)根据定性、定量研究中现象的分析及有关数据计算判断,这包久置“双吸剂”固体的成分中氧化钙的质量小于0.56g:因为固体Ⅱ中碳酸钙的质量为1g,则碳酸钙中钙元素质量为1g×![]() ×100%=0.4g,假设这些钙元素全部由氧化钙提供,则需要氧化钙的质量为0.56g,而固体溶于水减少的质量是0.6g>0.56g,所以样品中一定还含有氢氧化钙,所以氧化钙的质量一定小于0.56g;
×100%=0.4g,假设这些钙元素全部由氧化钙提供,则需要氧化钙的质量为0.56g,而固体溶于水减少的质量是0.6g>0.56g,所以样品中一定还含有氢氧化钙,所以氧化钙的质量一定小于0.56g;
实验反思:
A、对物质成分的研究有时需要定性和定量相结合,此说法正确;
B、根据定性研究并结合以上分析可知:在原样品中加入足量盐酸,存在的5种物质有碳酸钙、铁、氧化铁、氧化钙、氢氧化钙,都能和稀盐酸反应生反应,至少能发生5种化学反应:①CaCO3+2HCl=CaCl2+H2O+CO2↑;② Fe+2HCl=FeCl2+H2↑;③Fe2O3+6HCl=2FeCl3+3H2O;④CaO+2HCl=CaCl2+H2O;⑤Ca(OH)2+2HCl=CaCl2+2H2O
C、定量研究烧杯 C 中的溶质为 NaOH 和 Na2CO3,此说法正确;烧杯中有过量的碳酸钠溶液,碳酸钠与氢氧化钙溶液反应后悔产生氢氧化钠溶液和碳酸钙沉淀,其反应原理为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
结合上面的实验,说法正确的是AC。


科目:初中化学 来源: 题型:
【题目】测定工业废气中的SO2含量。
【查阅资料】
①溴水(Br2溶于水中)为黄色溶液,可与SO2反应,其化学方程式: Br2 + SO2 + 2H2O ═ H2SO4 + 2HBr
②某地规定工业排放的废气中SO2含量不得超0.4 mgm-3。
探究小组进行如下实验,测定步骤:
Ⅰ.向试管中加入含质量0.01 g Br2的溴水。
Ⅱ.在指定地点抽取工业废气缓慢通入上述溴水中(如下图)。
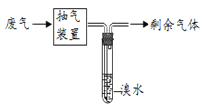
Ⅲ.当通入溴水中的工业废气总量达5 m3时,溶液恰好由黄色变成无色(Br2完全反应,废气中的SO2被完全吸收,且不发生其他反应)。 求该废气中SO2含量________________(mgm-3)?该废气是否符合排放标准________﹙“是”还是“不”﹚?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是一种重要的资源。
(1)电解水揭示了水的组成,实验中得到氢气的是电源的____极(填“正”或“负”)。
(2)自来水厂净水过程中用到活性炭,其作用是_______________________________。
(3)海水淡化可缓解淡水资源匮乏的问题。下图为太阳能海水淡化装置示意图。水变成水蒸气的过程中,不发生变化的有__________。(填序号)
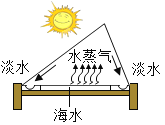
A 分子质量 B.分子间隔 C.分子种类
(4)小明发现家里的锅底有很多水垢,根据所学知识,他判断出家里的水是硬水,为了将硬水软化,他可以通过_________的方式达到目的。
(5)很多地区的人们面临着巨大的淡水危机,这要求我们要保护水资源。为节约用水,你能做到的一件事是_________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习完本单元的实验活动后,化学实验小组成员一起来解决下列问题:
(1)小红同学从某一歉收农田里取回一份土壤样品,如果检测结果呈酸性,从经济和可行性方面考虑,如果要改良此土壤的酸性,应向农田里施用________(填俗名)。
(2)小明同学用如图总结了NaOH的四条化学性质(NaOH与四类物质能够发生化学反应)。
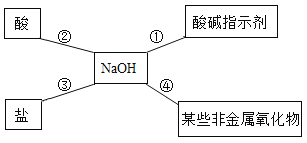
Ⅰ.为了验证反应①和反应②,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成________;接着往其中滴入稀硫酸,边滴加边振荡,又发现溶液的颜色______________,后者变色原因可用化学方程式表示为__________________。
Ⅱ.依据反应④说明NaOH必须密封保存,否则在空气中容易发生变质,其反应的化学方程式为____________。
Ⅲ.为了验证反应③能够发生,你选择的物质是__________ (填字母)。
A Na2CO3 B HCl C CuSO4 D SO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活密切相关,化学使我们的生活更加美好:
⑴ 出行使用电动自行车,有利于减少环境污染,电动自行车行驶时电池将_________能转化为电能。
⑵ 建筑外墙的复合保温材料采用铝合金锁边,金属铝耐腐蚀是因为__________。
⑶ 丝织品等深受人们的喜爱,如何把它们和化纤制品区分开? _________。
⑷ 长期饮用硬水对人们健康不利,在生活中降低水的硬度常用的方法是________。
⑸ 尿素是一种常用的化肥,工业上生产尿素反应的微观示意图如下:
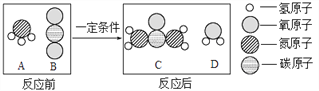
该反应的化学方程式为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A﹣H都是初中常见的物质,其中D为蓝色沉淀,A、E是组成元素相同的两种气体,F、H为黑色固体,他们之间转化关系如下图(反应条件及部分反应物和生成物略去)
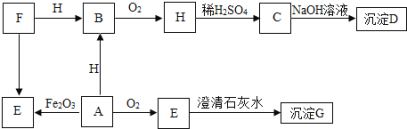
(1)G的化学式是______,写出该物质的一种用途______________。
(2)写出物质C与NaOH溶液反应生成沉淀D的化学方程式_________________。
(3)写出![]() 化学方程式________________。
化学方程式________________。
(4)以上化学反应,未涉及到的基本反应类型有_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向烧杯里100.0g稀硫酸中加入一定量铜锌合金粉末,等不再有气泡冒出后用导管向烧杯中通入氧气并加热,粉末逐渐减少、消失,溶液由无色变为蓝色。测得溶液质量与实验时间的关系如图。

下列说法错误的是( )
A.从a点到b点,产生0.4g H2
B.从b点到c点,说明Cu不能置换出硫酸中的氢
C.从c点到d点,发生的反应为2Cu+2H2SO4+O2 ![]() 2CuSO4+2H2O
2CuSO4+2H2O
D.从d点到e点,溶液中的溶质至少有二种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为某反应的微观示意图,其中白色小球和黑色小球分别代表两种不同元素的原子。下列说法正确的是( )
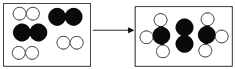
A.图中共有4种分子B.有两种分子参加反应且个数比为3:1
C.各元素的化合价反应后都比反应前升高D.该化学反应属于置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组用图1 装置进行实验时发现,烧杯中饱和石灰水先变浑浊,后逐渐澄清。
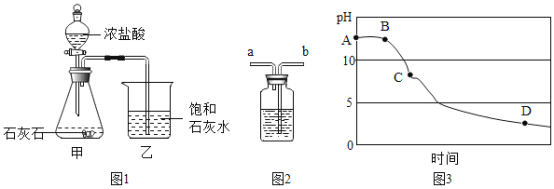
(1)写出甲装置中发生反应的化学方程式_______。
(2)为探究“饱和石灰水浑浊后变澄清的原因”,该小组同学开展了如下活动:
(查阅文献)碳酸钙(碳酸钠等)与二氧化碳、水反应生成可溶于的碳酸氢钙(碳酸氢钠等)。
(提出假设)假设 1:挥发出的HCl使浑浊变澄清;假设2:______。
(设计实验)同学们设计实验证明假设1正确。为证明假设2,他们如下设计:为除去CO2中的HCl,小华在图1中甲、乙装置之间增加图2装置,装置的连接顺序是甲→____→____→乙(填字母序号);其中存放的试剂合理的是_______(填选项序号)。
A 浓硫酸 B 饱和Na2CO3溶液 C 饱和NaHCO3溶液
(实验现象)饱和石灰水浑浊后,继续通入足量 CO2 ,沉淀部分溶解但最终并未完全澄清。
(得出结论)由以上探究可得出结论是___________。
(3)该兴趣小组在老师指导下,用 pH 传感器测得图 1烧杯中溶液的 pH 随通入时间的变化曲线如图3。D点所得溶液的成分除 H2O外还有_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com