
【题目】下图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:
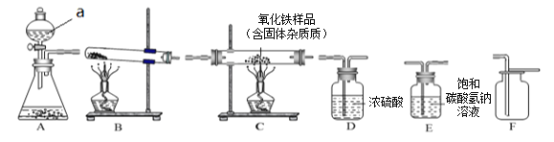
(1)若以石灰石和稀盐酸为原料制取二氧化碳,因盐酸会挥发出少量的氯化氢气体,导致制取的气体不纯,可用饱和碳酸氢钠溶液吸收。现要制备、收集一瓶干燥的、不含氯化氢的二氧化碳气体。
①所选仪器的连接顺序为__________________________(填写仪器序号字母)
②仪器a的名称是_________________
③生成二氧化碳时,A中所发生反应的化学方程式为______________________________
④将少量的CO2气体通入盛有大量澄清Ca(OH)2溶液的大烧杯中,烧杯中溶液的质量与之前相比会__________ (填“增大”“减小”“不变”之一)。
(2)小强同学欲用一氧化碳气体测定某不纯氧化铁样品的纯度(杂质不参与任何反应),小强同学取2.5g氧化铁样品设计了实验方案:气体流向是从左向右,选择的仪器按“一氧化碳气体→C→尾气处理装置”顺序连接,然后进行实验(假设有关反应均反应完全)。若其他操作正确,反应结束后测得C装置减少了0.48g(不考虑空气中成分对装置质量的影响),则此氧化铁样品中氧化铁的质量分数为______________。
【答案】A-E-D-F 分液漏斗 CaCO3+2HC1=CaCl2+H2O+CO2↑ 减小 64%
【解析】
本题考查了气体的制取装置、收集装置和洗气装置的选择,同时也考查了化学方程式的书写和有关的计算,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)①实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,不需要加热,发生装置选A,要收集一瓶干燥、纯净的二氧化碳气体,要把杂质氯化氢气体和水蒸气除去,氯化氢气体与和碳酸氢钠溶液反应生成氯化钠、水和二氧化碳,可以除去氯化氢气体,水蒸气用浓硫酸除去,除去水蒸气放在最后,二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集。所以所选仪器的连接顺序为A-E-D-F;
②仪器a的名称是分液漏斗;
③生成二氧化碳时,A中所发生反应的化学方程式为CaCO3+2HC1=CaCl2+H2O+CO2↑;
④将二氧化碳通入澄清石灰水中,二氧化碳和氢氧化钙反应生成了碳酸钙沉淀,溶液中的溶质减少,溶液的质量减小;
(2)设氧化铁的质量为x,玻璃管内减小的质量就是氧元素的质量,所以
Fe2 O3 +3CO![]() 2Fe+3CO2 固体减小质量
2Fe+3CO2 固体减小质量
160 48
X 0.48g
![]() x=1.6g
x=1.6g
氧化铁样品中氧化铁的质量分数=![]() ×100%=64%。
×100%=64%。


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:初中化学 来源: 题型:
【题目】请阅读下列短文,并回答问题。
酸雨是指pH小于5.6的雨雪或其他形式的降水。酸雨主要是人为向大气中排放大量酸性物质所造成的。雨、雪等在形成和降落过程中,吸收并溶解了空气中的二氧化硫或氮氧化物等物质,形成了pH低于5.6的酸性降水。
酸雨中的阴离子主要是硝酸根和硫酸根离子,根据两者在酸雨样品中的浓度可以判定降水的主要影响因素是二氧化硫还是氮氧化物。二氧化硫主要来自于矿物燃料(如煤)的燃烧,氮氧化物主要来自于汽车尾气等污染源。
含有硫的煤燃烧生成二氧化硫,二氧化硫与水反应生成亚硫酸(H2SO3),H2SO3在空气中被氧化成硫酸。
雷雨闪电时,大气中也会产生少量硝酸。闪电时,氮气与氧气化合生成一氧化氮(NO),NO不稳定,在空气中被氧化成二氧化氮(NO2)。NO2是一种红棕色、具有刺激性气味的气体,它可与水反应生成硝酸。
酸雨对环境、工农业生产、建筑、森林、植物等危害巨大。
依据文章内容,回答下列问题:
(1)NO2的物理性质有________。
(2)NO与NO2化学性质不同的原因是_________。
(3)H2SO3被空气中的氧气氧化为硫酸的化学方程式为________。
(4)氮气与氧气化合生成一氧化氮的化学方程式为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在天平左右两盘中各放一个等质量的烧杯,烧杯中分别盛有等质量的足量的稀硫酸,天平平衡。向左盘烧杯中加入27g10%的氯化钡溶液,向右盘烧杯中加入铁粉,若天平最终平衡,则加入铁粉的质量为
A. 56g B. 28g C. 27g D. 数据不足,无法计算
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(三)铁的冶炼和探究
取24.0g Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。
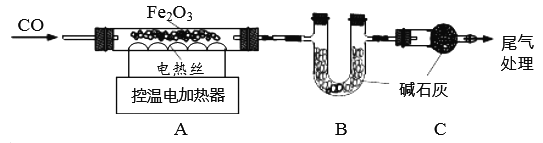
资料:碱石灰可吸收H2O和CO2。
【1】连接装置,先______________________,再装入药品。
【2】实验时先通入CO,目的是______________________________。
【3】控制A中温度在700℃至固体全部变黑,继续通CO至冷却。
(1)通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是____。
(2)现直接测得装置A中剩余固体质量为19.2g。则装置B中固体应增重________________g。
【4】经分析A中剩余固体19.2g为Fe和FexOy的混合物,向其中加入足量的稀H2SO4充分反应,得H2 0.3g。
(1)固体中Fe质量为__________________g。
(2)FexOy的化学式为__________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室里有氯酸钾、二氧化锰、石灰石和稀盐酸以及如图所示的装置,回答下列问题:
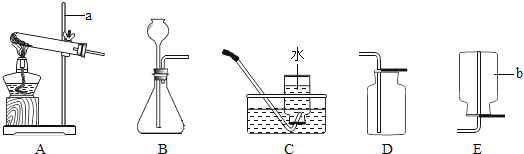
(1)写出图中仪器a和b的名称:a ;b .
(2)利用如图所示的装置和药品制取并收集二氧化碳,应选择的装置是 (填字母).
(3)利用如图所示的装置和药品制取并收集氧气,应选择的装置是 (填字母).
(4)组装仪器时连接玻璃管和胶皮管的操作:先把玻璃管口 ,然后稍稍用力即可把玻璃管插入胶皮管.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年入冬以来,我们见识到了“空气杀手”——雾霾,直观的感受到雾霾天气给我们的生活带来的困扰。
对于一线城市来说,汽车尾气排放是雾霾天气形成的重要因素之一。科学分析表明,汽车尾气中含有多种污染物,如固体悬浮微粒、一氧化碳、二氧化碳、碳氢化合物、氮氧化合物(NOx)、铅及硫氧化合物等。目前最有效的汽车尾气治理方法是在发动机排气系统中加装催化转化器,其基本原理是通过催化剂的作用和一系列的氧化还原反应,使CO、NOx、碳氢化合物转化为对人体无害的二氧化碳(CO2)、氮气(N2)和水蒸气(H2O),该催化剂能同时对汽车尾气中的CO、NOx、碳氢化合物三种有害物起催化净化作用,因此这种催化剂被称为三效催化剂(TWC)。
TWC通常是以贵金属铂、铑、钯为活性组分,通过浸渍的方法分散在大比表面积的γ-Al2O3活性涂层上,并将γ-Al2O3涂附在熔点达1350℃的堇青石载体上制成。依据文章内容和下图,回答下列问题:
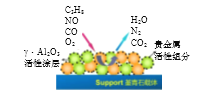
(1)三效催化剂主要由三部分组成,分别是_______________________。
(2)三效催化剂的成分之一堇青石的物理性质:____________________________。
(3)在三效催化剂发挥作用的一系列氧化还原反应中,有一步反应是:在催化剂的作用下,CO和NO反应生成CO2和N2,请写出该反应的化学方程式______________
(4)三效催化剂以γ-Al2O3活性涂层为活性组分的载体的原因是______________。
(5)科学家一直积极致力于开发新型的活性组分,如采用Mn、Fe、Cu等过渡金属为主要活性组分来取代贵金属,你认为该研发方向的优势是_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(2分)右图是NaCl、MgSO4的溶解度曲线.下列说法正确的是( )
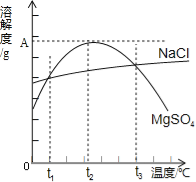
A. 只有在t1℃时,NaCl和MgSO4的溶解度才相等
B. t1℃~t3℃,MgSO4的溶解度随温度升高而增大
C. 在t2℃时,MgSO4饱和溶液的溶质质量分数最大
D. 把MgSO4饱和溶液的温度从t3℃降至t2℃时,有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是用木炭还原氧化铜的实验装置图,回答下列问题。
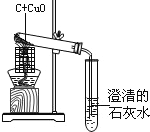
(1)酒精灯加灯网罩的目的______;
(2)该反应中______有还原性,______有氧化性;
(3)刚开始预热,试管②中立即产生气泡,但石灰水不变浑浊,原因是______;
(4)继续加热,黑色粉末中出现______色物质,同时观察到石灰水逐渐变______,请你写出碳粉还原氧化铜的化学方程式:______;
(5)停止加热前,应先将导管从试管②中撤出,原因是______;并用弹簧夹夹紧橡皮管,待试管①冷却后再把试管里的粉末倒出。原因是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用红磷燃烧测定空气中氧气的含量,得到的结论是______。还可以推断出氮气___(填“易”或“难”)溶于水和其化学性质______(填“活泼”或“不活泼”)的结论。氧气很活泼,可以与多种物质进行反应,在氧气中燃烧产生蓝紫色火焰的反应符号表达式是_______;在氧气中燃烧生成能使澄清石灰水变浑浊的气体的符号表达式是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com